Clear Sky Science · pt
Nanozima mimética da granzima B para aplicações anticâncer direcionadas por nanovesículas
Reinventando os Assassinos do Corpo contra o Câncer
Nosso sistema imunológico possui células especializadas que conseguem localizar e destruir cânceres, mas em muitos tumores sólidos elas têm dificuldade para penetrar, se esgotam rapidamente ou atacam alvos errados. Este estudo descreve um sistema totalmente artificial, em escala nanométrica, que imita uma das armas mais potentes do sistema imune e a entrega diretamente dentro das células tumorais. O trabalho é relevante porque aponta para tratamentos contra o câncer que se comportam como células imunes vivas, porém são feitos de materiais estáveis e controláveis em vez de células humanas frágeis.
Transformando um Assassino Natural em um Projeto
Células T citotóxicas, um tipo de glóbulo branco, matam células perigosas usando uma enzima chamada granzima B. Depois de reconhecerem um alvo, perfuram a membrana e injetam a granzima B, que ativa programas de suicídio dentro da célula. Essa estratégia fundamenta terapias modernas como as células CAR-T, que podem curar alguns cânceres do sangue. Contudo, em tumores sólidos, as CAR-T frequentemente falham porque não alcançam todas as regiões do tumor, se esgotam ou atingem tecidos saudáveis por engano. Os autores perguntaram se seria possível construir um dispositivo nanométrico não vivo que reproduzisse a função-chave da granzima B — ativar a máquina de autodestruição da célula — sem depender de células T vivas.
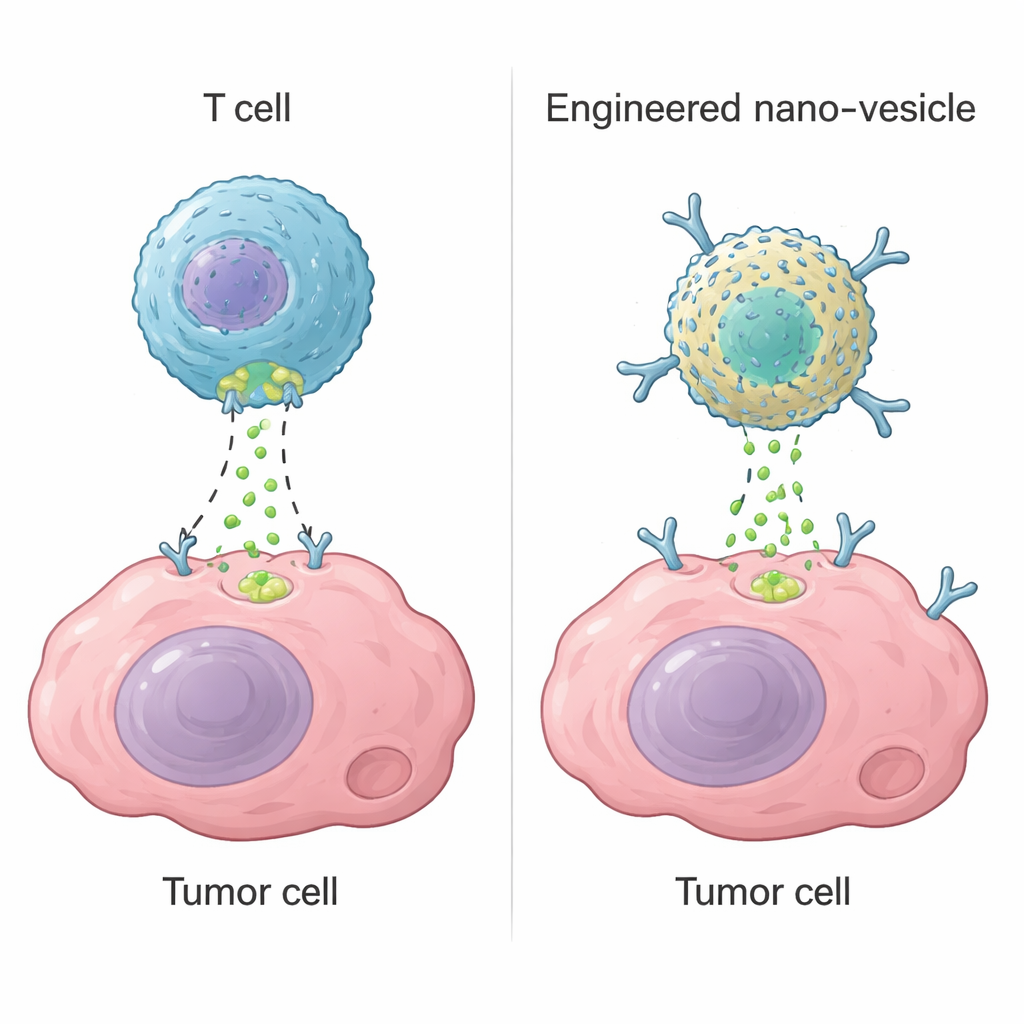
Projetando uma Enzima Artificial Minúscula
A equipe partiu da ferritina, uma proteína natural que forma nanocápsulas ocas e é fácil de produzir em grandes quantidades. Ao ligar íons de paládio à ferritina humana, eles criaram um “nanozima” com comportamento semelhante ao de uma enzima. Estudos estruturais cuidadosos revelaram que dois átomos de paládio se acomodam em um bolso específico na superfície da proteína, mantidos por aminoácidos contendo enxofre e nitrogênio e por moléculas de água. Esse centro metálico binuclear atua como um sítio artificial de clivagem que reconhece a mesma sequência curta usada pela granzima B em um alvo crucial conhecido como caspase-3. Em testes de laboratório, o nanozima cortou eficientemente a caspase-3 na posição correta, ativando-a, enquanto ignorava proteínas intimamente relacionadas. A enzima artificial foi ligeiramente menos eficiente que a granzima B natural, mas notavelmente mais estável em uma ampla faixa de temperaturas e acidez.
Contrabandeando o Nanozima para Dentro das Células Tumorais
Enzimas como a granzima B só funcionam se alcançarem o interior das células tumorais. Para isso, os pesquisadores embalaram seu nanozima paládio–ferritina dentro de nanovesículas lipídicas — pequenas bolhas macias feitas de moléculas semelhantes a gorduras. Em seguida, revestiram essas vesículas com fragmentos de anticorpos que reconhecem HER2, uma proteína frequentemente superexpressa em células de câncer de mama e bexiga. Quando essas vesículas camufladas encontram células ricas em HER2, elas se ligam firmemente e se fundem com a membrana celular, permitindo que a carga do nanozima deslize diretamente para o citoplasma em vez de ficar presa e digerida em compartimentos de reciclagem celular. Microscopia mostrou as vesículas demorando na superfície celular enquanto o nanozima difundia para o interior, preparando o cenário para uma autodestruição controlada de dentro para fora.
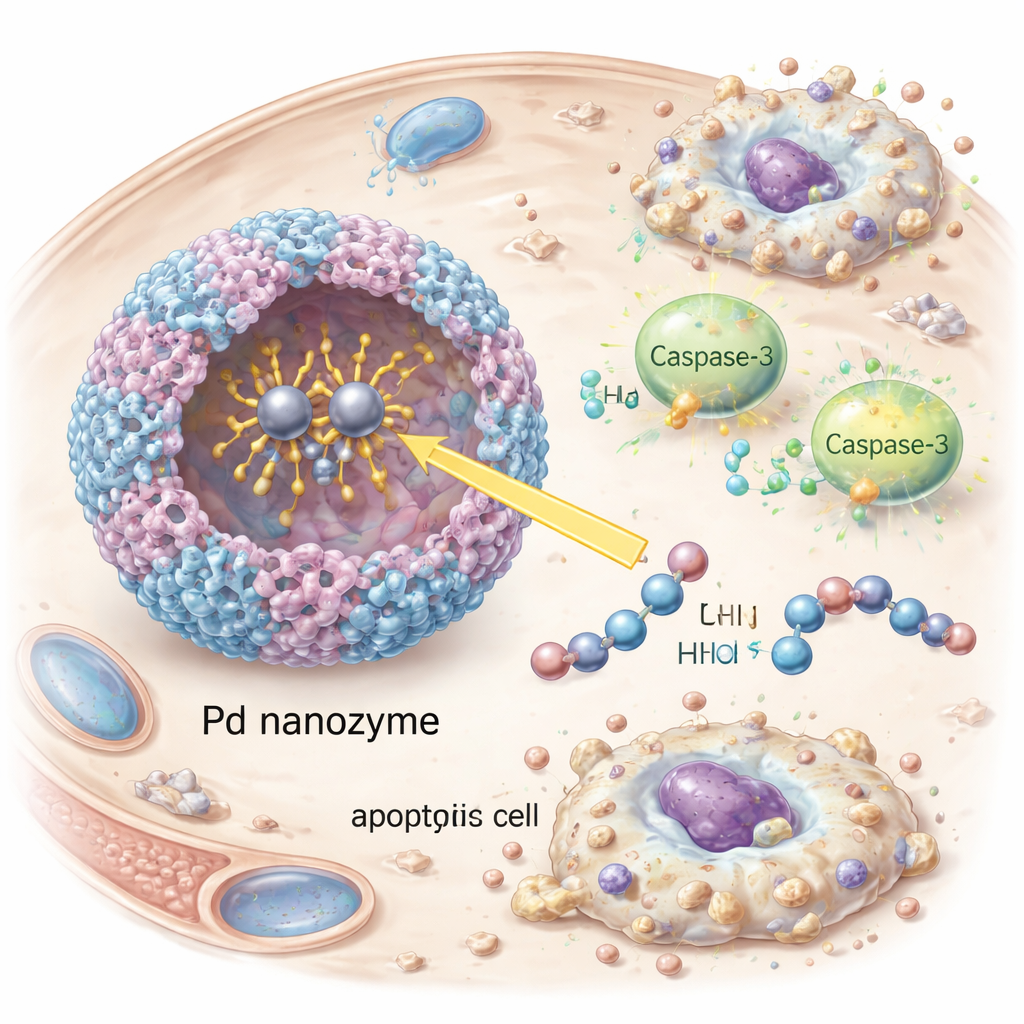
Desencadeando o Suicídio das Células Cancerosas com Precisão
Uma vez dentro das células cancerosas, o nanozima ativou a caspase-3, um executor central da morte celular programada. Os pesquisadores observaram o aparecimento da caspase-3 ativada e de seu alvo a jusante PARP, assim como sinais claros de apoptose — células encolhendo e fragmentando — em células tumorais cultivadas HER2-positivas. Silenciar a caspase-3 por interferência de RNA reduziu drasticamente a morte celular, confirmando que o efeito dependia dessa via e não de dano não específico. Em camundongos portadores de tumores HER2-positivos, as vesículas decoradas com anticorpos circularam por mais tempo na corrente sanguínea, acumularam-se mais fortemente nos tumores e retardaram o crescimento tumoral de forma mais eficaz do que vesículas que não continham os anticorpos de direcionamento ou a carga de nanozima. Importante, os animais tratados não mostraram perda de peso óbvia, anormalidades sanguíneas ou danos teciduais em órgãos principais, sugerindo um perfil de segurança favorável nesses testes iniciais.
O Que Isso Pode Significar para o Cuidado Oncológico Futuro
Para não especialistas, a mensagem central é que os pesquisadores construíram um dispositivo minúsculo e não vivo que se comporta como uma peça-chave da maquinaria imune de destruição do câncer. Em vez de engenharia de células T vivas, eles desenvolveram um nanoenzima estável que ativa o mesmo interruptor de suicídio dentro das células tumorais e o envolveram em uma cápsula de entrega inteligente que se dirige a certos cânceres. Embora ainda reste muito trabalho antes do uso em humanos, essa abordagem oferece uma plataforma flexível: em princípio, o revestimento de anticorpos poderia ser trocado para mirar em diferentes marcadores tumorais, e a enzima artificial poderia ser otimizada. O estudo demonstra uma rota promissora para imunoterapia sem células, em que nanomateriais projetados com precisão, em vez de células imunes vivas, são usados para localizar e destruir tumores sólidos.
Citação: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Palavras-chave: nanomedicina contra o câncer, imunoterapia, granzima B, nanozima, tumores HER2-positivos