Clear Sky Science · pt
Química bioortogonal ativada por espécies reativas de oxigênio em sistemas vivos viabilizada por dihidrotetrazinas protegidas por boronato
Transformando o estresse celular em um interruptor preciso
Muitas doenças, do câncer a problemas cardíacos, são marcadas por células sob estresse oxidativo, produzindo altos níveis de espécies reativas de oxigênio, como o peróxido de hidrogênio. Este estudo mostra como químicos podem aproveitar esse próprio estresse como um interruptor embutido para ativar terapias potentes apenas onde são necessárias. Ao projetar componentes de fármacos que reagem somente nesses ambientes estressados, os pesquisadores pretendem eliminar células tumorais ou destruir proteínas nocivas ao mesmo tempo em que preservam tecidos saudáveis.
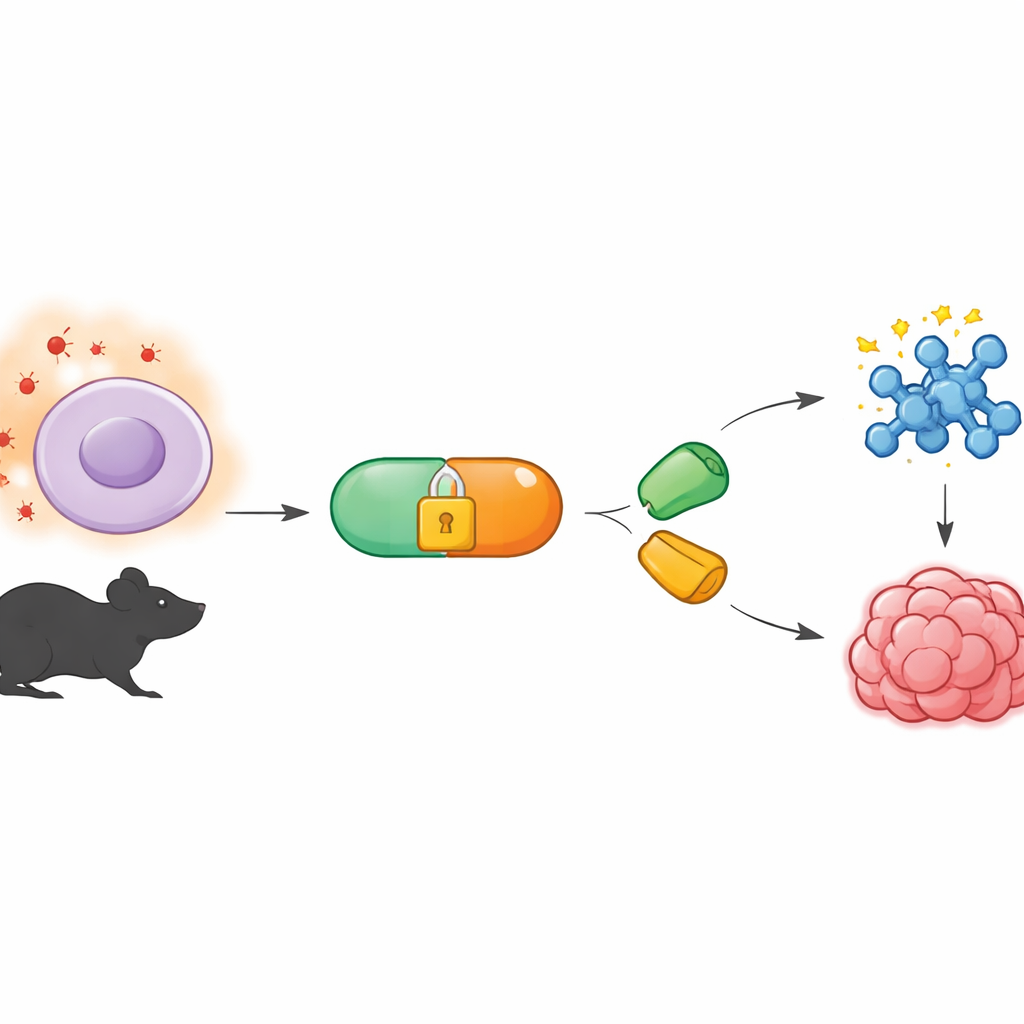
Uma ferramenta química que atua discretamente nos bastidores
O trabalho se baseia em um campo chamado química bioortogonal, que desenvolve reações capazes de funcionar dentro de organismos vivos sem perturbar a biologia normal. Uma versão popular usa pares especiais de moléculas que se encaixam como peças de um quebra‑cabeça, mesmo no interior congestionado de uma célula. Um parceiro, chamado tetrazina, reage muito rapidamente com um parceiro complementar em anel, conhecido como dienófilo. Até agora, muitas dessas reações foram controladas por iluminação ou pela adição de enzimas. Os autores, em vez disso, queriam um sistema que ouvisse os próprios sinais químicos do corpo — especificamente, os níveis incomumente altos de espécies reativas de oxigênio encontrados em tumores e outros tecidos doentes.
Construindo um gatilho químico sensível a ROS
Para isso, a equipe criou precursores de tetrazina que chamam de BTz, que são quimicamente “protegidos” para permanecerem inertes em tecidos normais. A proteção é formada por um grupo boronato ligado a uma forma reduzida da tetrazina. Quando o peróxido de hidrogênio é escasso, o BTz é estável em água e em cultura celular por muitas horas. Mas quando o peróxido de hidrogênio é abundante — em níveis semelhantes aos medidos em tumores — o grupo boronato é oxidado e se desfaz por uma sequência de autodestruição, revelando a tetrazina ativa. Em experimentos em tubo de ensaio, o aumento gradual da concentração de peróxido de hidrogênio levou a um incremento correspondente na quantidade de tetrazina ativa gerada, confirmando que a reação é seletiva e fortemente dependente da dose.
Usando o estresse celular para destruir uma proteína que impulsiona o câncer
Os pesquisadores primeiro usaram seu interruptor para controlar uma estratégia moderna de fármacos chamada degradação proteica direcionada. Eles ligaram BTz à talidomida, uma pequena molécula que pode recrutar um complexo enzimático responsável por marcar proteínas para eliminação. Em células cancerosas, esse BTz–talidomida permaneceu dormente até que os níveis de peróxido de hidrogênio aumentassem, momento em que a proteção se abriu para formar uma tetrazina ativa. Essa tetrazina então se acoplou com um parceiro correspondente ligado a um fármaco que se une ao BRD4, montando uma “quimera” maior que conduz a proteína relacionada ao câncer BRD4 para a maquinaria de degradação da célula. Em linhas celulares de câncer de pulmão e cervical, os níveis de BRD4 caíram acentuadamente apenas quando todas as partes estavam presentes e o peróxido de hidrogênio estava disponível; bloquear as espécies reativas de oxigênio impediu a degradação, ressaltando que o processo é realmente ativado pelo estresse.
Entregando um fármaco tóxico apenas onde é necessário
Em seguida, a equipe transformou a mesma química em um sistema de entrega preciso para a doxorrubicina, uma quimioterapia potente porém cardiotóxica. Eles ligaram a doxorrubicina a um parceiro de anel tensionado de modo que ficasse trancada em uma forma pró‑droga inativa. Quando essa pró‑droga encontrou BTz em um ambiente rico em peróxido de hidrogênio, a tetrazina recém‑formada reagiu com o anel em um processo de “click‑to‑release”, juntando as peças e ejetando a doxorrubicina livre. Em células de câncer colorretal cultivadas em placas, esse sistema em duas etapas matou as células quase tão eficazmente quanto o fármaco livre, mas somente quando o peróxido de hidrogênio estava presente; sem ele, as células permaneceram em grande parte intactas. Uma pró‑droga mais simples sensível ao peróxido de hidrogênio foi menos eficaz e menos seletiva nesses testes, destacando a vantagem de separar detecção e liberação em dois passos coordenados.
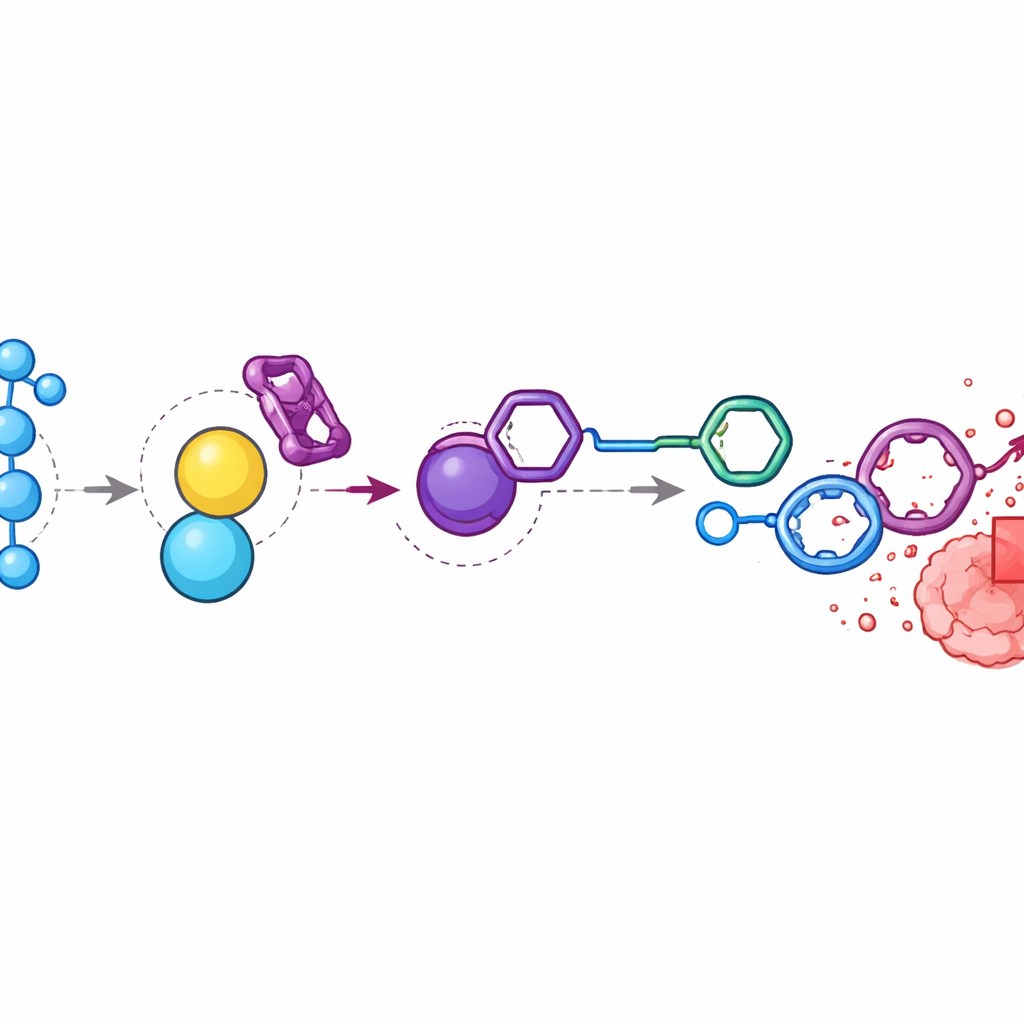
Focalizando a quimioterapia dentro dos tumores
Em camundongos com tumores colorretais, os pesquisadores descobriram que os níveis de peróxido de hidrogênio nos tumores eram quase nove vezes maiores do que no músculo circundante. Eles injetaram a pró‑droga de doxorrubicina e o BTz em sequência cronometrada para que ambos se acumulassem perto do tumor. A análise química mostrou que os componentes desapareceram em grande parte da corrente sanguínea e dos órgãos, mas geraram altos níveis de doxorrubicina livre dentro dos tumores. Em comparação com animais tratados com doxorrubicina padrão, aqueles submetidos ao sistema ativado mostraram redução semelhante ou melhor do tumor, mantendo peso corporal estável e evitando a toxicidade severa observada em doses mais altas do fármaco. Quando a equipe interrompeu o sinal de peróxido de hidrogênio injetando catalase, uma enzima que remove o peróxido de hidrogênio, a liberação do fármaco e o acúmulo seletivo no tumor foram grandemente reduzidos, confirmando que o estresse oxidativo no local do tumor é o motor chave.
Do sinal de estresse à terapia de precisão
Em conjunto, este estudo demonstra uma plataforma química versátil que transforma uma marca da doença — o excesso de oxigênio reativo — em um botão de controle preciso para reações potentes dentro de sistemas vivos. Ao manter a alça reativa da tetrazina bloqueada até encontrar peróxido de hidrogênio, a abordagem permite que pesquisadores montem terapias complexas dentro do corpo apenas onde são necessárias, seja para desmontar uma proteína que promove o câncer ou para liberar um fármaco tóxico dentro de um tumor. Como o estresse oxidativo também desempenha papéis no envelhecimento, inflamação, diabetes e distúrbios neurodegenerativos, reações sensíveis ao estresse semelhantes poderiam, em última instância, ser adaptadas para muitas condições em que precisão e segurança são fundamentais.
Citação: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
Palavras-chave: química bioortogonal, espécies reativas de oxigênio, ligação de tetrazina, liberação direcionada de fármacos, PROTAC