Clear Sky Science · pt
Análise microfluídica eletroquímica alimentada por membranas homotípicas de vesículas extracelulares para diagnóstico preciso do câncer
Transformando a própria armadura do câncer em uma ferramenta diagnóstica
As membranas que envolvem as células cancerígenas estão repletas de “bandeiras” moleculares distintivas. Este estudo mostra como cientistas podem remover essa armadura, espalhá‑la sobre pequenos chips de ouro e então usá‑la para pescar partículas indicativas no sangue. O resultado é um exame sanguíneo altamente sensível que pode revelar não apenas se há câncer de mama, mas qual é o seu subtipo — informação crucial para escolher o tratamento adequado.
Por que o subtipo do câncer de mama importa
O câncer de mama não é uma única doença. Os tumores são agrupados em subtipos como receptor de estrogênio–positivo (ER+), HER2‑positivo e triplo‑negativo, cada um respondendo de forma diferente à terapia hormonal, a drogas alvo e à quimioterapia. Hoje, os médicos geralmente determinam o subtipo a partir de uma biópsia de tecido retirada diretamente do tumor. Esse procedimento é invasivo, não pode ser realizado com frequência e pode deixar de detectar mudanças que ocorrem à medida que a doença evolui. Um teste sanguíneo capaz de acompanhar essas assinaturas de subtipo ao longo do tempo permitiria que os médicos ajustassem a terapia mais cedo e com maior precisão.
Mensageiros minúsculos flutuando no sangue
As células cancerígenas liberam constantemente bolhas em escala nanométrica chamadas vesículas extracelulares (VE) na corrente sanguínea. As VE transportam proteínas, lipídios e material genético que se assemelham de perto aos de suas células de origem, tornando‑as candidatas atraentes para “biópsias líquidas”. Mas há um desafio: as VE de diferentes subtipos de câncer de mama podem parecer muito semelhantes se você considerar apenas uma ou duas proteínas. Testes existentes ou visam marcadores compartilhados — dificultando a distinção entre subtipos — ou dependem de ensaios genéticos complexos que são lentos e podem fornecer resultados enganosos. Os autores buscaram ler a impressão digital molecular mais completa na superfície das VE de maneira simples e robusta.
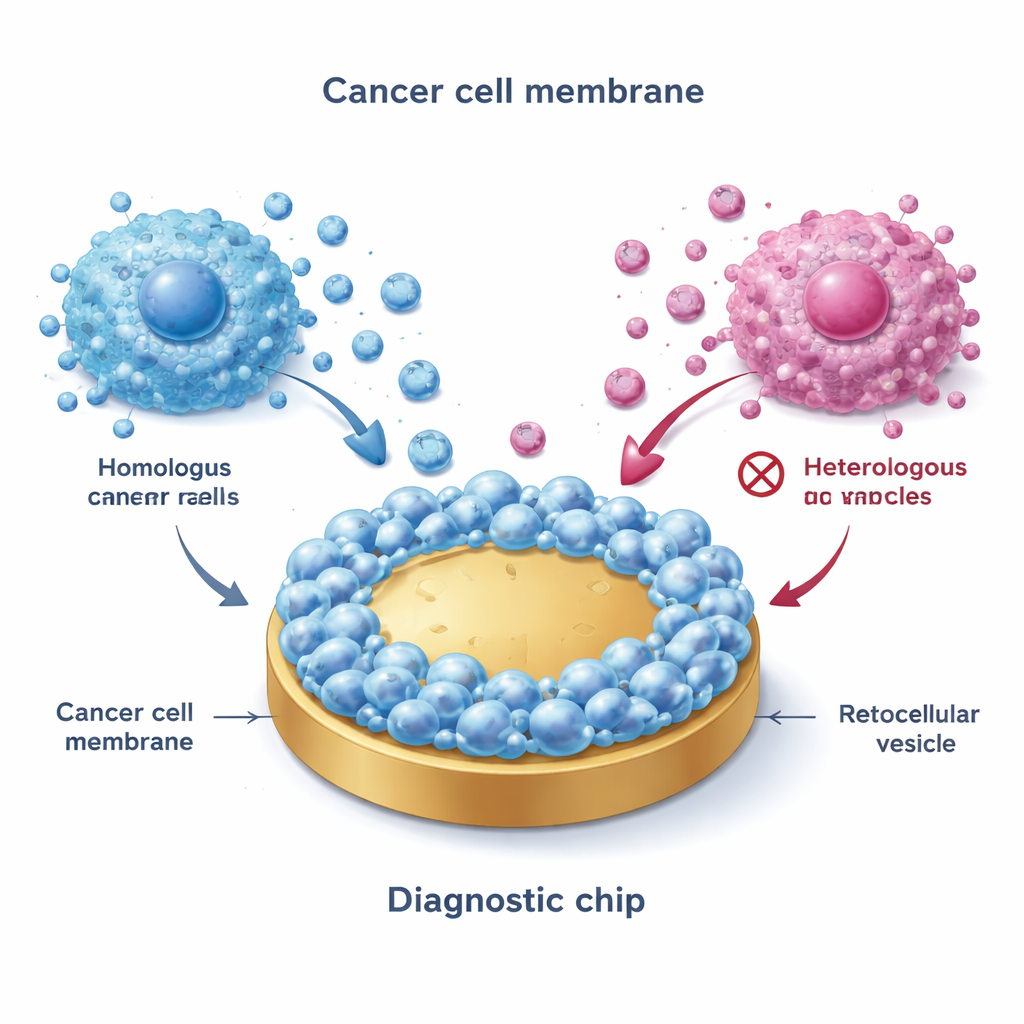
Construindo uma rede de pesca biomimética
A equipe começou colhendo membranas de células de câncer de mama cultivadas que representam os principais subtipos: ER+ (como MCF‑7), HER2‑positivo e triplo‑negativo. Usando um processo de congelamento e descongelamento, eles romperam as células, isolaram as membranas externas e então fundiram essas membranas em superfícies planas de ouro. Isso criou uma “interface biomimética” que imita de perto o exterior das células cancerígenas originais. Notavelmente, quando VE foram fluídas sobre essas superfícies revestidas, somente as vesículas de subtipos correspondentes, ou intimamente relacionados, aderiram fortemente — um fenômeno denominado ligação homotípica. Imagens avançadas e medições elétricas confirmaram que as superfícies recobertas por membrana eram mais rugosas, mais hidrofílicas e muito menos propensas a aderência inespecífica do que o ouro nu, tornando‑as adequadas para medições limpas em fluidos complexos como o sangue.
Convertendo a captura de vesículas em um sinal elétrico
Para transformar a ligação em um sinal legível, os pesquisadores miraram uma proteína abundante chamada CD47 na superfície das VE. Eles ligaram anticorpos contra CD47 a nanopartículas de prata usando uma pequena ponte de DNA, criando minúsculas etiquetas eletroativas. Depois que a superfície revestida por membrana capturou suas VE preferenciais, essas etiquetas se ligaram ao CD47 nas vesículas presas. Quando expostas a uma solução ácida e então medidas eletroquimicamente, a prata produziu uma corrente nítida e facilmente quantificável. A intensidade desse sinal crescia de forma linear em uma ampla faixa de concentrações de VE, até poucas centenas de vesículas por mililitro — muito mais sensível que métodos comuns como kits ELISA ou rastreamento de nanopartículas. Cada tipo de membrana cancerígena produziu um sinal forte somente com suas VE correspondentes, mesmo na presença de vesículas de outros subtipos, plaquetas ou células não relacionadas.
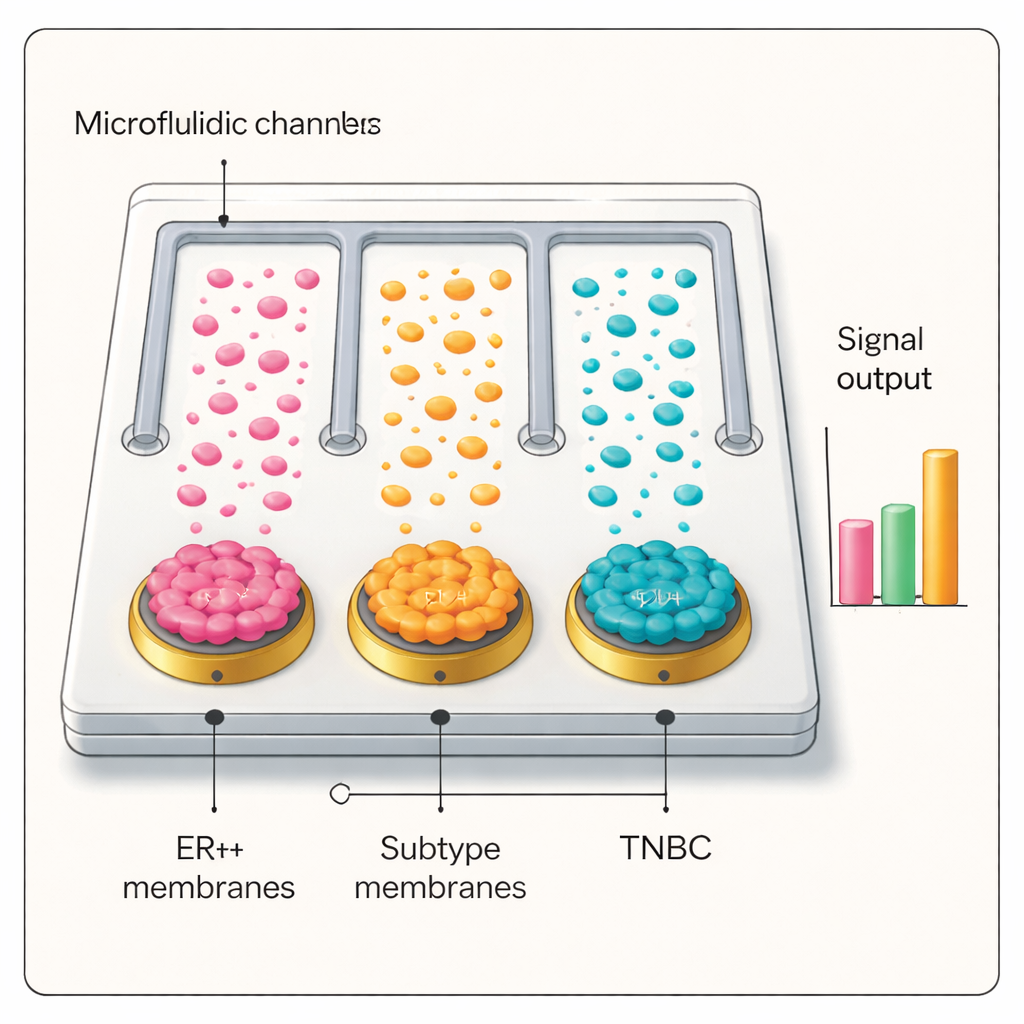
Do banco de laboratório às amostras de sangue de pacientes
Munida dessa interface seletiva e sensível, a equipe construiu um chip microfluídico contendo canais paralelos, cada um revestido com uma membrana de célula de câncer de mama diferente, além de um controle não revestido. Quando plasma de pacientes foi passado pelo chip e sondado com as etiquetas prata‑anticorpo, somente o canal cuja membrana correspondia ao subtipo tumoral do paciente produziu um sinal elétrico alto. Em testes cegos com dezenas de pessoas — incluindo pacientes com câncer de mama ER+ e triplo‑negativo, indivíduos com doença benigna da mama, pacientes com câncer de pulmão e voluntários saudáveis — a plataforma distinguiu com precisão câncer de não‑câncer e identificou corretamente subtipos de câncer de mama. O desempenho diagnóstico igualou ou superou a patologia padrão em muitos casos e mostrou potencial para estadiamento da doença e monitoramento de sua progressão.
O que isso pode significar para o futuro do cuidado contra o câncer
Em termos simples, os pesquisadores transformaram a própria casca externa do câncer em uma isca altamente seletiva para as partículas minúsculas que os tumores liberam no sangue. Ao ler a assinatura elétrica de qual canal “acende”, os médicos poderiam um dia determinar não apenas se há câncer, mas que tipo é, usando apenas uma amostra de sangue. Embora o sistema ainda precise de aperfeiçoamentos — como adicionar mais marcadores e mais tipos de membranas, e integrar análise de dados inteligente — ele aponta para um futuro em que testes sanguíneos rotineiros e minimamente invasivos auxiliem a guiar tratamentos personalizados contra o câncer e a monitorar como os tumores mudam ao longo do tempo.
Citação: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Palavras-chave: subtipos de câncer de mama, biopsia líquida, vesículas extracelulares, diagnósticos microfluídicos, sensores de membrana celular