Clear Sky Science · pt
Uma quimera de antígeno tandem estabilizada que provoca intensa atividade redutora da transmissão da malária
Por que interromper a transmissão por mosquitos importa
As vacinas contra a malária atualmente em uso podem reduzir muito as formas graves da doença e o número de óbitos em crianças pequenas, mas deixam uma falha importante: pessoas que não se sentem doentes ainda podem portar parasitas que infectam mosquitos e mantêm a transmissão. Este estudo apresenta um projeto de vacina de próxima geração que não tem como objetivo apenas proteger um indivíduo, mas cortar a cadeia de infecção entre humanos e mosquitos. Ao engenheirar com precisão como proteínas-chave do parasita são exibidas ao sistema imune, os pesquisadores visam gerar anticorpos que tornem os mosquitos hospedeiros pouco propícios para a malária, ajudando comunidades a se aproximarem da eliminação.
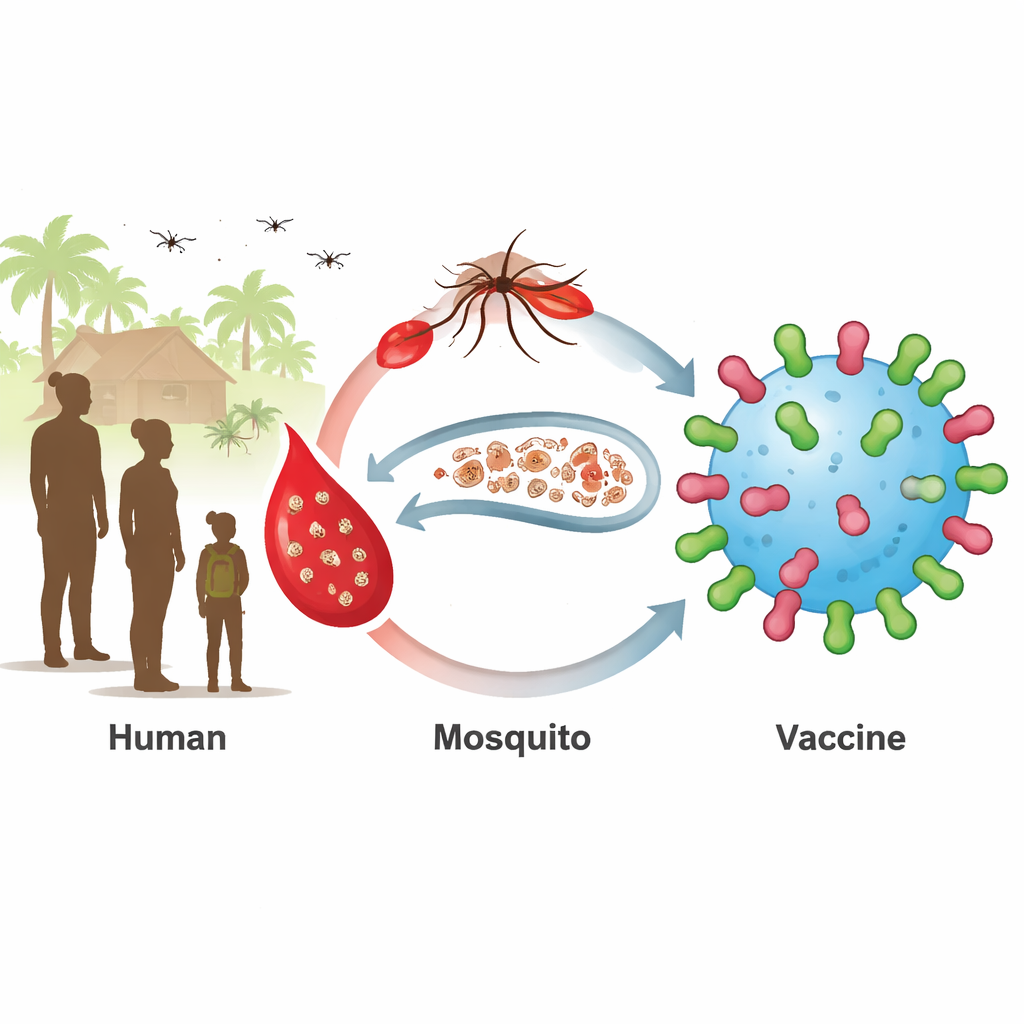
Um reservatório oculto que mantém a malária viva
As vacinas atuais contra a malária focam o estágio inicial da infecção no fígado e no sangue. Funcionam melhor em crianças pequenas, mas crianças mais velhas e adultos frequentemente abrigam parasitas em estágio sexual maduro, chamados gametócitos, sem sintomas. Quando mosquitos picam essas pessoas, eles capturam os parasitas e os disseminam adiante. Duas proteínas de superfície do parasita, conhecidas como Pfs230 e Pfs48/45, estão presentes nesses estágios sexuais e são alvos atraentes para as chamadas vacinas bloqueadoras de transmissão. Vacinas dirigidas a fragmentos dessas proteínas chegaram a ensaios clínicos, mas tiveram dificuldades para induzir respostas de anticorpos fortes e duradouras em todos os receptores.
Construindo um engodo mais inteligente para o sistema imune
Para melhorar os desenhos anteriores, os autores adotaram uma abordagem de biologia estrutural, examinando em detalhe atômico como anticorpos humanos potentes se ligam a Pfs230 e Pfs48/45. Eles identificaram pequenas regiões, ou epítopos, que são especialmente eficazes em bloquear o desenvolvimento do parasita dentro dos mosquitos. Igualmente importante, mapearam epítopos "não funcionais" que atraem anticorpos que se ligam mas não impedem a transmissão—basicamente desperdiçando esforço imune. Usando modelagem computacional e ferramentas de engenharia de proteínas, fundiram a região mais potente de Pfs230 (seu primeiro domínio) com a região-chave de Pfs48/45 (seu terceiro domínio) em uma única proteína cuidadosamente disposta que chamam de quimera de antígeno tandem estabilizada, ou STAC.
Escondendo os alvos inúteis, mantendo os úteis
O desafio foi apresentar esses dois domínios juntos de forma que imitasse como eles se situam no parasita, enquanto fisicamente ocultavam as superfícies não funcionais que normalmente ficam enterradas na proteína intacta. A equipe redesenhou iterativamente o curto elo e a interface entre os dois domínios, testando cada versão quanto à estabilidade, dobra correta e se ainda se ligava a um painel de anticorpos bem caracterizados. Software avançado de projeto sugeriu mutações que apertaram a interface e melhoraram a expressão em células cultivadas. Estudos estruturais usando cristalografia de raios X, espalhamento de raios X em ângulo pequeno e criomicroscopia eletrônica confirmaram que, na construção final do STAC, os epítopos desejados são exibidos com alta fidelidade, enquanto os sítios conhecidos como inúteis ficam bloqueados estéricamente.
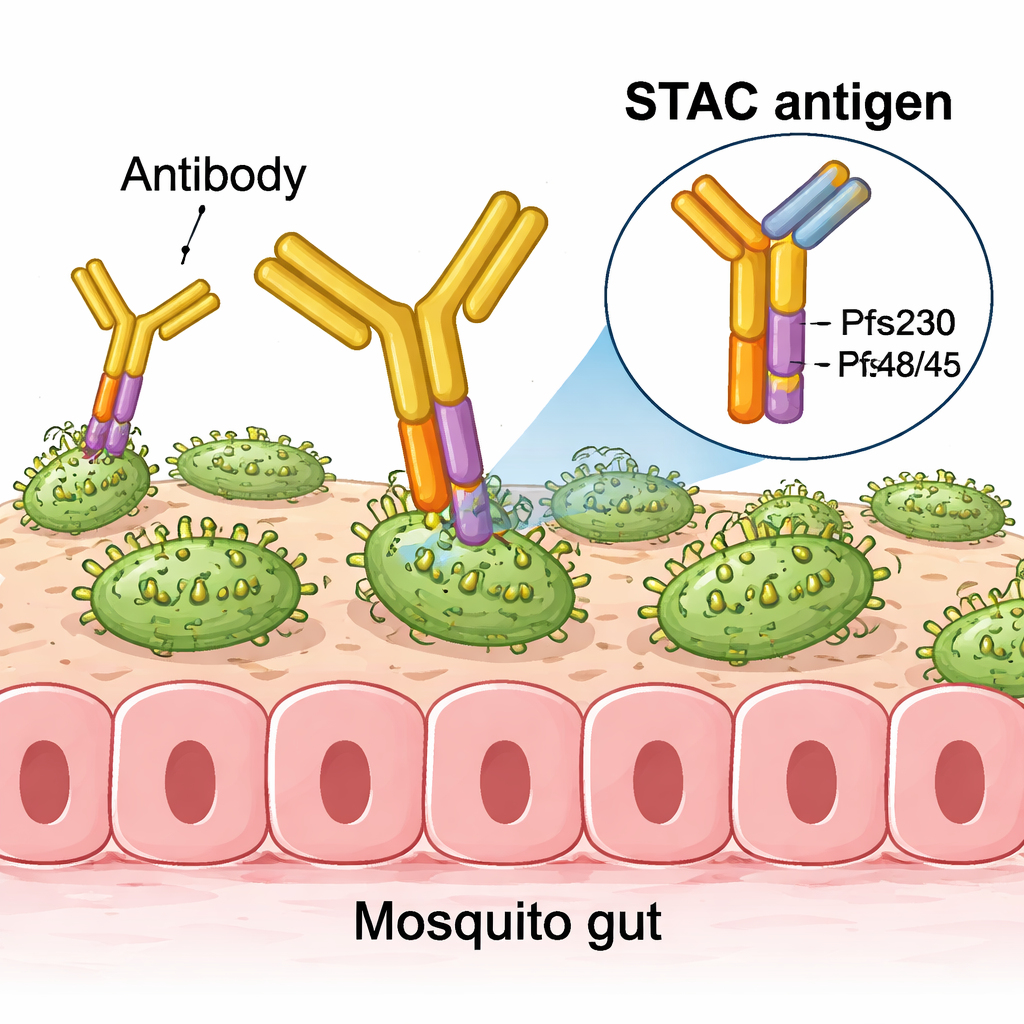
De moléculas únicas a nanopartículas poderosas
Testes em camundongos demonstraram que quando o STAC foi ligado a lipossomas especializados ou a nanopartículas proteicas autoajustáveis, ele desencadeou respostas de anticorpos fortes capazes de reduzir drasticamente o desenvolvimento do parasita em ensaios padrão de alimentação de mosquitos. Em doses iguais ou menores, o STAC frequentemente igualou ou superou vacinas que usavam fragmentos de Pfs230 e Pfs48/45 separadamente, seja administrados sozinhos, misturados ou exibidos juntos na mesma partícula. Em testes altamente sensíveis que diluem o soro de camundongo muitas vezes, os anticorpos induzidos por nanopartículas decoradas com STAC mantiveram a atividade redutora de transmissão melhor do que os oriundos de outras formulações, indicando respostas particularmente potentes e focadas.
O que isso pode significar para o controle da malária
Para não especialistas, a ideia chave é que o STAC é um engodo construído sob medida que mostra ao sistema imune exatamente as partes do parasita da malária que mais importam para bloquear a disseminação, enquanto oculta regiões que distraem e não ajudam. Em modelos animais, esse desenho gera anticorpos que dificultam que os parasitas completem seu ciclo de vida em mosquitos, mesmo quando os níveis de anticorpos são relativamente baixos. Se resultados semelhantes se confirmarem em humanos, o STAC poderia se tornar um parceiro poderoso das vacinas contra malária existentes: protegendo indivíduos vacinados da doença ao mesmo tempo em que reduz o reservatório infectante na comunidade. Mais amplamente, o trabalho demonstra como percepção estrutural detalhada e engenharia de proteínas podem ser usadas para criar vacinas multicomponentes que são potentes, estáveis e potencialmente mais baratas de fabricar.
Citação: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
Palavras-chave: vacinas contra malária, bloqueio de transmissão, Pfs230, Pfs48/45, imunógeno em nanopartícula