Clear Sky Science · pt
Papel essencial do eixo NONO-HOXA1-Wnt na diferenciação de cardiomiócitos
Por que as minúsculas células do coração importam para todos nós
Cada batimento cardíaco depende de bilhões de células musculares especializadas formadas no útero. Quando esse processo falha, bebês podem nascer com defeitos cardíacos graves. Este estudo usa células-tronco humanas para revelar um sistema de controle crucial — formado por moléculas chamadas NONO e HOXA1 e por um sinal bem conhecido chamado Wnt — que ajuda as células iniciais a se comprometerem com o destino de se tornarem músculo cardíaco saudável. Compreender essa circuitaria oculta pode, no futuro, orientar diagnósticos e tratamentos melhores para cardiopatias congênitas.
De células em branco aos construtores iniciais do coração
Os pesquisadores partiram de células-tronco pluripotentes induzidas humanas — células versáteis que podem ser direcionadas para quase qualquer tipo celular. Usando uma receita padrão, eles conduziram essas células para se tornarem cardiomiócitos, as células pulsantes do coração. Quando o gene NONO foi removido, muito menos células adotaram com sucesso uma identidade cardíaca. Marcadores iniciais-chave que normalmente aparecem quando as células deixam o estado primitivo e seguem para a linhagem cardíaca foram fortemente reduzidos. O sequenciamento de RNA em célula única mostrou que muitas células deficientes em NONO ficaram estagnadas na metade do caminho, presas em um estado imaturo semelhante a mesendoderma em vez de progredirem para músculo cardíaco completamente desenvolvido.
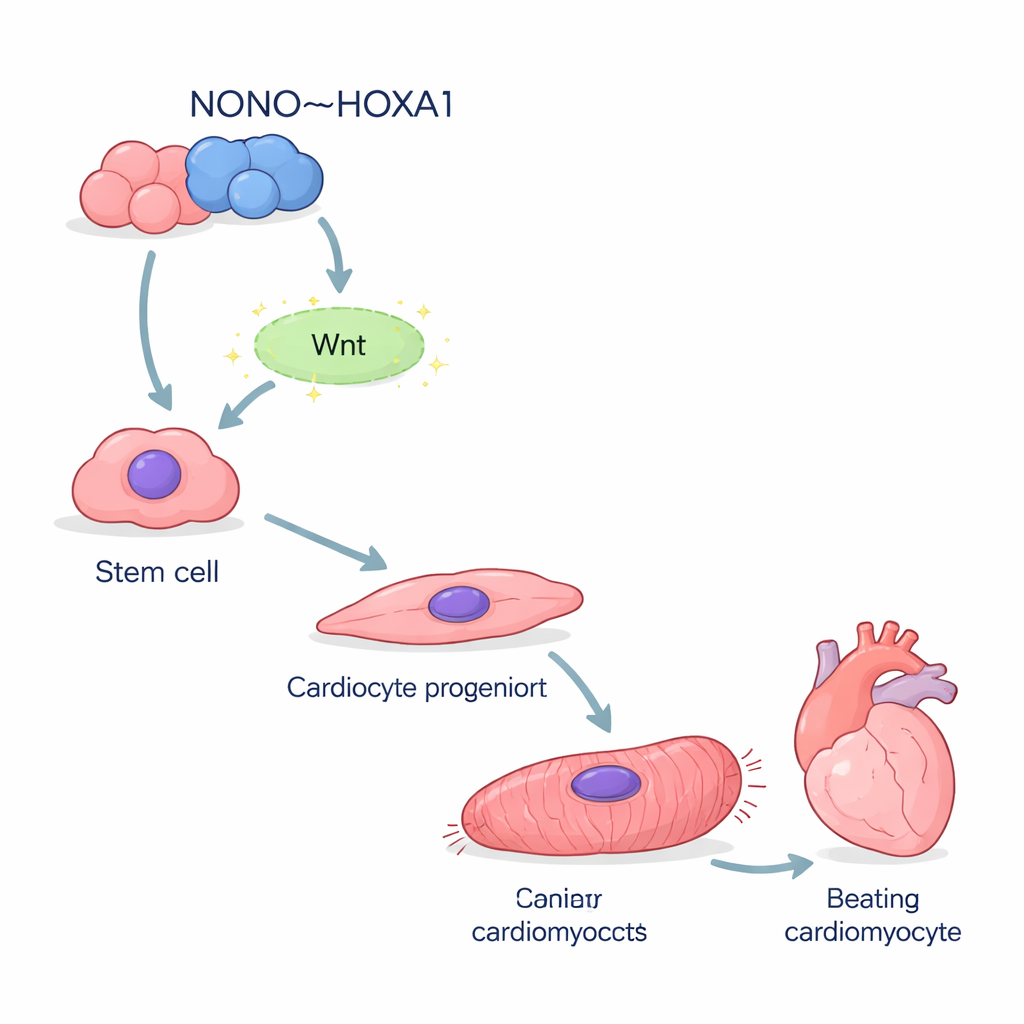
Quando o andaime falta, as células cardíacas fraquejam
Aquelas células que se tornaram cardiomiócitos sem NONO estavam longe de ser saudáveis. Expressaram níveis muito mais baixos de proteínas estruturais que formam o sarcômero, a maquinaria microscópica que impulsiona a contração. Ao microscópio, a maioria das células mutantes apresentou fibras contráteis desorganizadas e fragmentadas, em vez das faixas ordenadas observadas em células normais. Microscopia eletrônica confirmou que os habituais “degraus” do disco Z da escada contrátil estavam ausentes ou malformados. Funcionalmente, essas células batiam mais lentamente e de forma irregular. Medições de surtos de cálcio — eventos elétricos que desencadeiam cada batimento — revelaram formas de onda erráticas com picos atrasados e recuperação lenta, refletindo os defeitos de expressão gênica nos canais de manuseio de cálcio.
Resgatando o desenvolvimento e expondo a parceria NONO–HOXA1
Para testar se esses problemas realmente decorriam da perda de NONO, a equipe reintroduziu NONO de forma controlada e induzível por droga durante os dois primeiros dias de diferenciação. Esse pulso breve de NONO restaurou em grande parte a elevação dos genes cardíacos iniciais, aumentou a proporção de células cardíacas batentes e reconstruiu sarcômeros e discos Z organizados. O perfil de expressão gênica confirmou que muitos genes de contração muscular e desenvolvimento cardíaco retornaram em direção a níveis normais. Em contraste, versões mutadas de NONO derivadas de pacientes não conseguiram resgatar, apoiando a ideia de que tais variantes causam doença ao perturbar esse programa inicial. Experimentos de interação de proteínas revelaram então que NONO se liga fisicamente a um fator de transcrição chamado HOXA1, e que esse contato estabiliza HOXA1 e ajuda na formação dos dímeros necessários para se prender ao DNA.
Ligar o sinal Wnt para comprometer-se com o destino cardíaco
O mapeamento de onde essas proteínas se posicionam no genoma mostrou que NONO e HOXA1 frequentemente ocupam as mesmas regiões regulatórias, incluindo aquelas que controlam genes importantes do coração inicial e da via Wnt. Quando NONO estava ausente, a ligação de HOXA1 em muitos desses sítios enfraqueceu, especialmente em genes que promovem o mesoderma pré-cardíaco — o tecido formador do coração mais inicial. A via downstream Wnt/β-catenina, que normalmente ajuda a lançar o mesoderma e o desenvolvimento cardíaco, também foi atenuada: menos β-catenina se acumulou no núcleo e testes de repórteres responsivos a Wnt caíram. Fortalecer os sinais Wnt com uma dose maior de um fármaco ativador de Wnt durante os primeiros dias de diferenciação pôde, em parte, contornar a ausência de NONO, restaurando mais células cardíacas e aumentando a expressão de genes cardíacos.
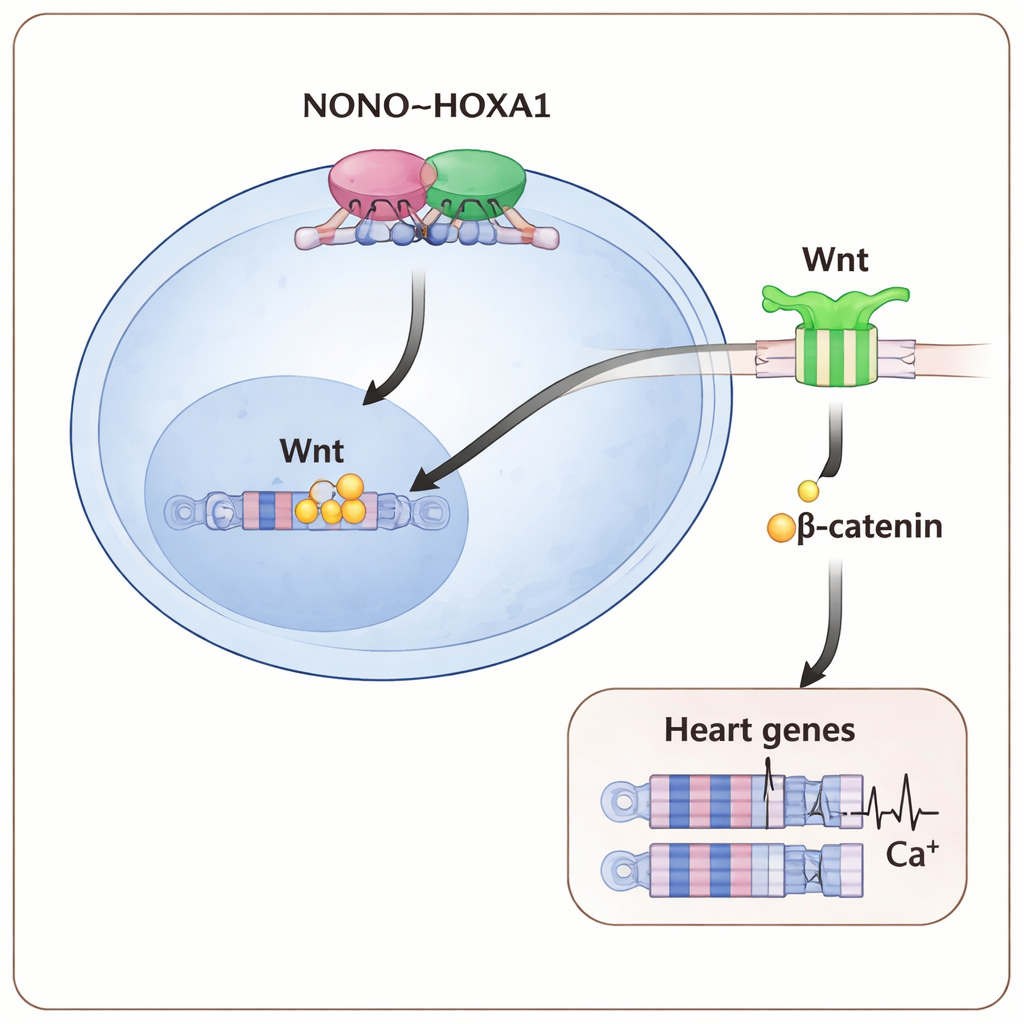
O que isso significa para entender defeitos congênitos
Para não especialistas, a mensagem central é que uma pequena equipe molecular — NONO trabalhando lado a lado com HOXA1 para ajustar finamente os sinais Wnt — atua como um “controlador de tráfego” precoce que diz às células jovens para se tornarem músculo cardíaco e as equipa para bater adequadamente. Quando qualquer parte desse eixo NONO–HOXA1–Wnt é perturbada, as células hesitam, genes cardíacos-chave permanecem desligados e os cardiomiócitos resultantes são estrutural e eletricamente frágeis. Essas percepções oferecem uma explicação molecular mais clara de por que mutações em NONO estão ligadas à cardiopatia congênita, e indicam maneiras de manipular essa via em modelos com células-tronco ou, um dia, em terapias destinadas a prevenir ou reparar malformações cardíacas.
Citação: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
Palavras-chave: cardiopatia congênita, diferenciação de cardiomiócitos, via de sinalização Wnt, modelos cardíacos com células-tronco, regulação gênica