Clear Sky Science · pt
Base estrutural para a reversão de forquilha e regulação de RAD51 pelo complexo ligase de ubiquitina SCF da helicase F-box 1
Como as células salvam uma máquina de cópia do DNA emperrada
Cada vez que uma célula se divide, ela precisa copiar bilhões de letras de DNA com rapidez e precisão. Mas essa máquina de cópia frequentemente encontra problemas — danos no DNA, sequências difíceis de copiar ou tratamentos com drogas podem fazer o processo parar. Quando isso acontece, as células dependem de equipes de reparo de emergência para estabilizar e reiniciar as forquilhas de replicação. Este artigo revela, com detalhes estruturais sem precedentes, como um desses líderes de equipe — um complexo proteico centrado na helicase FBH1 — remodela o DNA parado e mantém outro reparador chave, o RAD51, sob controle rigoroso. Compreender essa coreografia ajuda a explicar como as células evitam quebras perigosas no genoma e por que alterações nesses fatores estão associadas ao câncer.
Um engarrafamento na rodovia do DNA
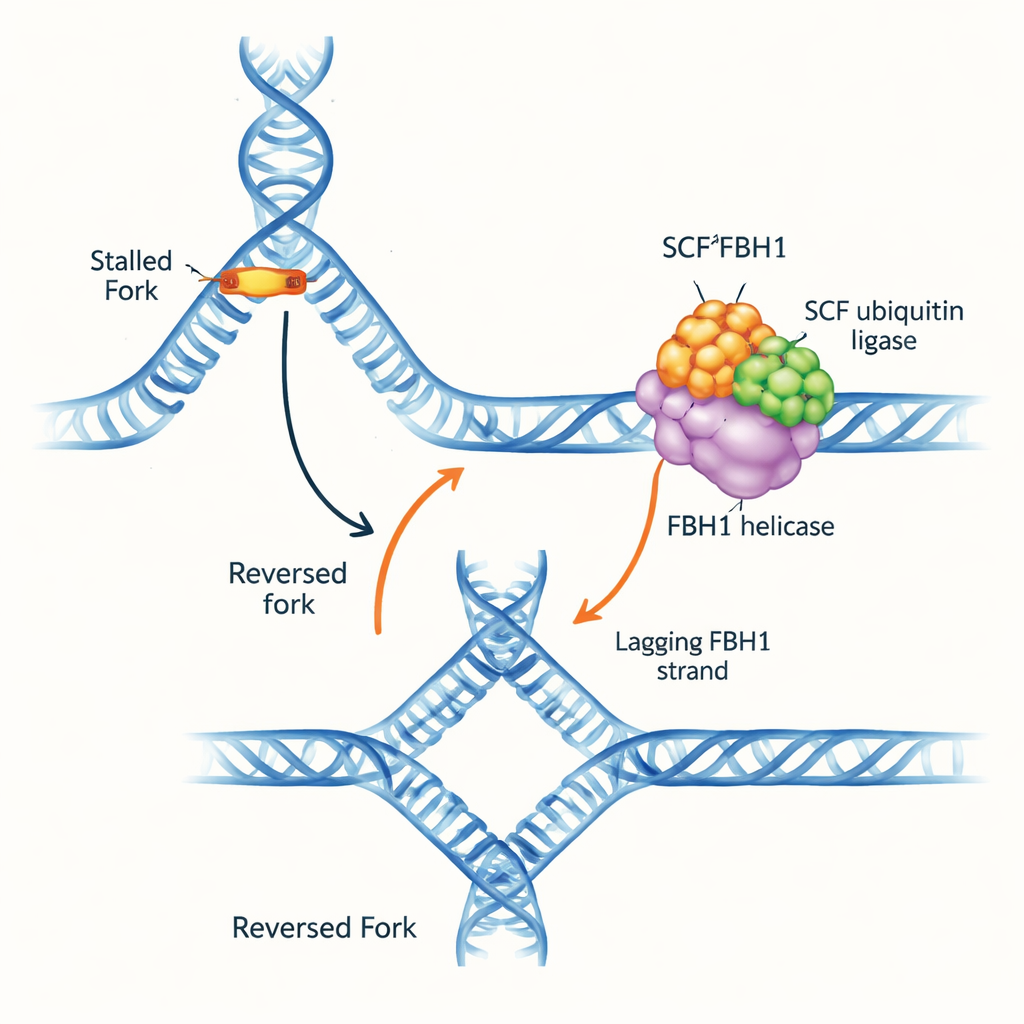
As forquilhas de replicação do DNA são estruturas em forma de Y onde a dupla hélice é desenrolada e copiada. Quando a forquilha encontra obstáculos, ela pode inverter a direção: as fitas parentais se reassociam e as fitas recém-sintetizadas pareiam entre si, formando uma junção de DNA em quatro vias. Essa “reversão de forquilha” pode comprar tempo para reparar danos e reiniciar a replicação com segurança, mas se mal gerida também cria DNA frágil que pode se romper. Vários motores moleculares são conhecidos por empurrar as forquilhas para trás ao se prender ao DNA de dupla fita à frente da forquilha. O FBH1, no entanto, se destacou por se comportar de forma diferente e por ser frequentemente alterado em tumores, sugerindo que opera via uma via distinta e de importância médica.
Um especialista em forquilhas com um lado preferido
Os autores purificaram o complexo humano SCFFBH1, que combina a helicase FBH1 com um módulo de marcação por ubiquitina (SCF). Eles primeiro investigaram que formas de DNA o FBH1 prefere. Usando ensaios de ligação e desenovelamento, mostraram que o SCFFBH1 favorece fortemente estruturas semelhantes a forquilhas reais, especialmente onde há um curto trecho de DNA fita simples na fita molde “atrasada” — o lado copiado em pequenos fragmentos. Nessas estruturas, o FBH1 desenrola o DNA centenas de vezes mais rápido do que em uma extremidade simples solta, indicando que o engajamento adequado na junção da forquilha superalimenta sua atividade motora. Experimentos de pinças magnéticas de molécula única confirmaram que o complexo pode desenrolar e então deslocar-se ao longo de DNA fita simples por milhares de bases sem se desprender, agindo como um motor potente e processivo.
Revertendo a forquilha puxando por trás
Para descobrir como esse motor realmente reverte forquilhas, o grupo testou substratos artificiais de forquilha com ou sem lacunas de fita simples. Ao contrário de outros remodeladores de forquilha, o SCFFBH1 não conseguiu agir numa forquilha totalmente pareada; ele exigia uma lacuna na fita molde atrasada e movia-se na direção 3′–5′ ao longo dessa fita simples. Esse movimento de “puxar por trás” impulsiona as fitas parentais a se reassociarem enquanto a enzima permanece presa na junção da forquilha. Uma estrutura por crio-microscopia eletrônica do SCFFBH1 ligado a uma forquilha parada mostra como: uma região especial carregada positivamente, um “motivo de ligação à junção” em um subdomínio do FBH1, encaixa-se exatamente no ponto de ramificação onde os três braços de DNA se encontram. Quando os pesquisadores mutaram dois aminoácidos chave nesse motivo, a reversão de forquilha caiu cerca de 25 vezes em ensaios in vitro, embora o motor básico de desenovelamento ainda funcionasse razoavelmente bem. Em células, a mesma mutação impediu o desaceleração normal das forquilhas de replicação em resposta a uma droga que induz estresse — uma marca registrada de falha na reversão de forquilha.
Um papel duplo: remodelar o DNA e remover RAD51
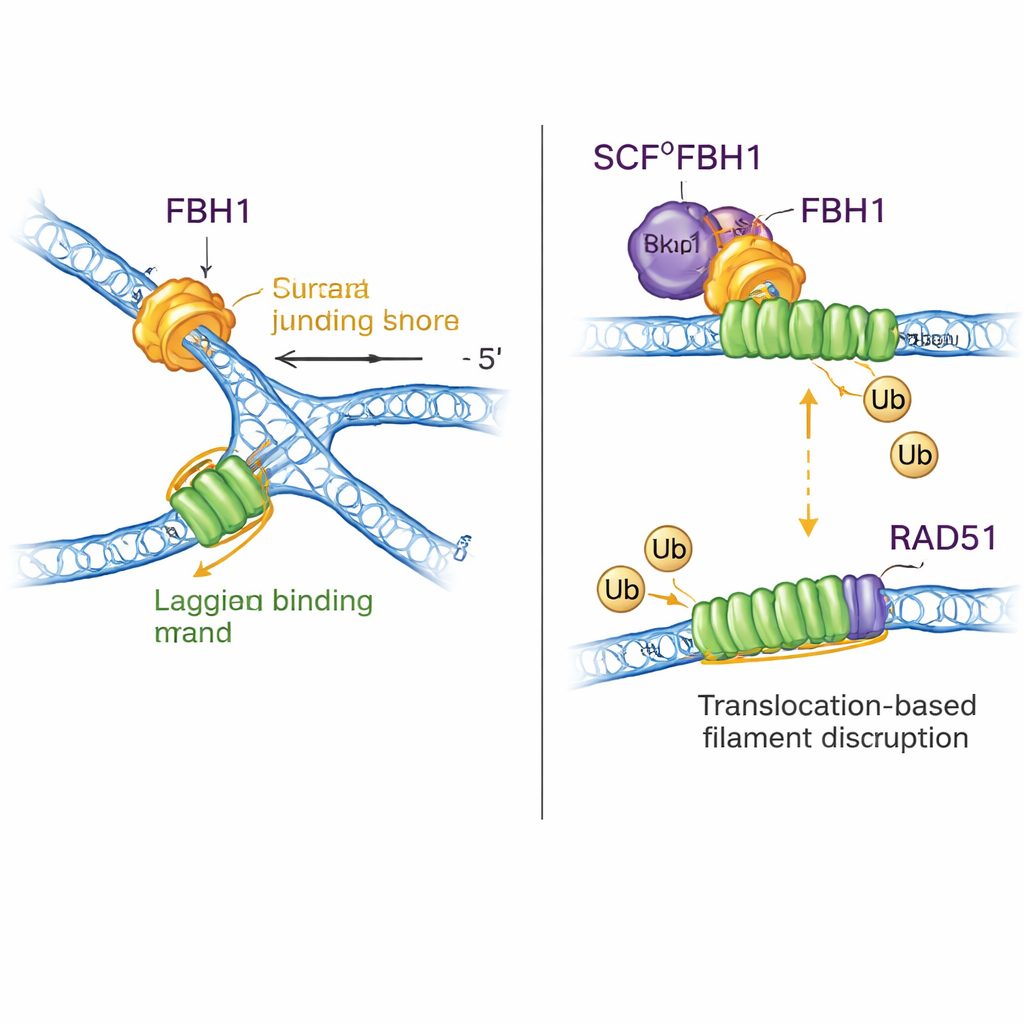
O FBH1 não é apenas um motor; por meio do complexo SCF ele também ajuda a anexar pequenas marcas de ubiquitina a proteínas. As novas estruturas montam quase todo o complexo SCFFBH1–DNA e mostram que a “cabeça” de transferência de ubiquitina da ligase fica a menos de 45 angstroms da fita atrasada de DNA emergindo do FBH1. Ao encaixar estruturas conhecidas de outras ligases de ubiquitina, os autores propõem que essa geometria posiciona o RAD51 — uma enzima que forma filamentos no DNA para promover recombinação — bem na linha de fogo na fita atrasada de uma forquilha parada. Trabalhos anteriores mostraram que o FBH1 pode remover mecanicamente o RAD51 do DNA e também marcá-lo com ubiquitina para que não se religue com facilidade. O novo modelo unifica essas ideias: enquanto o FBH1 puxa ao longo da fita atrasada para remodelar a forquilha, o módulo SCF próximo pode marcar subunidades de RAD51, ajudando a desmontar ou prevenir filamentos excessivos de RAD51 que poderiam bloquear o processamento adequado da forquilha.
O que isso significa para a estabilidade do genoma e o câncer
Em conjunto, o estudo mostra que o SCFFBH1 reverte forquilhas de replicação de DNA paradas usando um mecanismo distinto de outros remodeladores conhecidos: ele prende fortemente o ponto de ramificação enquanto se transloca ao longo do molde atrasado por trás, promovendo a religação segura do DNA parental sem formar uma junção móvel de quatro vias de longa duração. Ao mesmo tempo, sua ligase de ubiquitina embutida está estrategicamente posicionada para remover o RAD51 da mesma fita, prevenindo recombinação desenfreada durante o estresse de replicação. Como o FBH1 é frequentemente perdido ou mutado em cânceres, essas percepções estruturais e mecanísticas ajudam a explicar como esses tumores acumulam danos no DNA e por que podem responder de forma diferente a drogas que induzem estresse de replicação ou que visam vias relacionadas.
Citação: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
Palavras-chave: estresse na replicação do DNA, reversão de forquilha, helicase FBH1, regulação de RAD51, estabilidade do genoma