Clear Sky Science · pt
Um atlas proteogenômico de 1.032 metástases cerebrais identifica subtipos moleculares, paisagens imunes e vulnerabilidades terapêuticas
Por que os cânceres se espalham e afetam o cérebro
À medida que o tratamento do câncer melhora, mais pessoas vivem tempo suficiente para que seus tumores se espalhem para novos locais, incluindo o cérebro. Essas metástases cerebrais são hoje uma complicação comum e muitas vezes devastadora, mas os médicos ainda as tratam, em grande parte, segundo o órgão de origem—pulmão, mama, pele, cólon—em vez de como o câncer se adaptou ao ambiente cerebral. Este estudo construiu um “atlas” detalhado de mais de mil metástases cerebrais para entender sua biologia oculta, como interagem com as próprias células e o sistema imunológico do cérebro, e onde podem existir novas oportunidades de tratamento.
Construindo um mapa gigante dos tumores cerebrais
Os pesquisadores coletaram dados de 1.032 metástases cerebrais originadas de diferentes cânceres primários, junto com dezenas de tumores primários correspondentes e alguns tumores cerebrais primários agressivos para comparação. Eles combinaram várias abordagens de ponta: sequenciamento de DNA e RNA, medidas em grande escala de proteínas e metabólitos, mapeamento unicelular e espacial de células tumorais e imunes, e organoides derivados de pacientes cultivados em laboratório. Ao integrar todas essas camadas, o objetivo não era apenas listar genes, mas ver como sistemas biológicos inteiros se comportam nas metástases cerebrais.
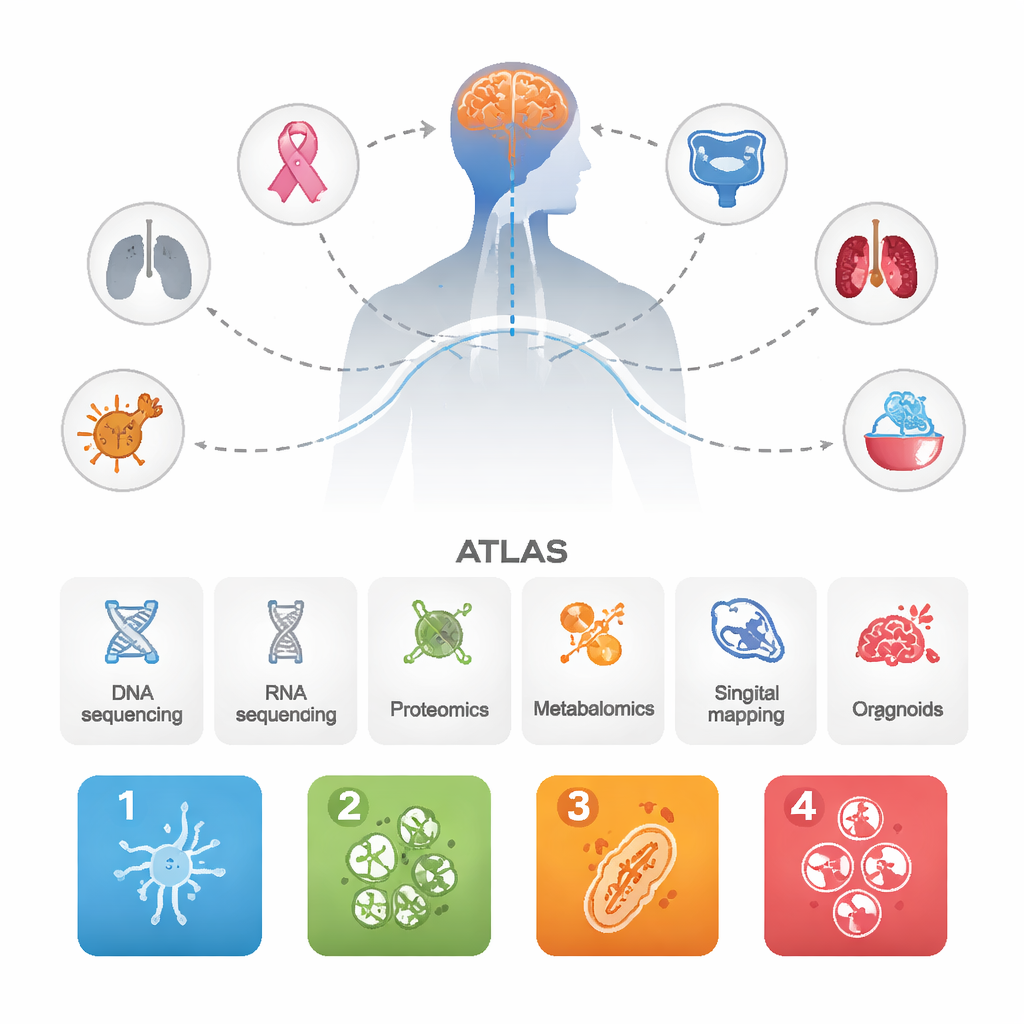
Quatro “personalidades” recorrentes das metástases cerebrais
Apesar de provenirem de muitos órgãos, as metástases cerebrais se agruparam repetidamente em quatro subtipos moleculares principais. Um, chamado BrMS1, parece “semelhante a neural”: células tumorais e o tecido circundante expressam muitos programas próprios do cérebro e de neurônios, e mostram vigilância imune relativamente ativa. BrMS2 é “ricamente infiltrado por imunidade”, cheio de células imunes, especialmente linfócitos T, e apresenta um programa conhecido como transição epitélio–mesênquima, que afrouxa as adesões celulares e remodela o ambiente local. BrMS3 é “metabólico”, dominado por células cancerosas altamente ativas que reprogramam seu uso de energia—queimando combustível por vias como o metabolismo de ácidos graxos e fosforilação oxidativa. BrMS4 é “proliferativo”, marcado por divisão celular rápida, características semelhantes a células-tronco e alta instabilidade genômica, mas notavelmente com poucas células imunes.
O que o microambiente tumoral revela
Ao ampliar a análise em resolução unicelular e espacial, a equipe mostrou que cada subtipo ocupa um bairro distinto dentro do cérebro. Lesões BrMS1 são ricas em células de suporte cerebral, como astrócitos e neurônios, sugerindo que o tumor imita e coapta de perto o tecido cerebral normal. Tumores BrMS2, em contraste, apresentam aglomerados densos de linfócitos T, incluindo muitos T “exauridos” que expressam moléculas de ponto de controle como PD-1, além de vasos sanguíneos ativados e sinais inflamatórios. Lesões BrMS3 estão em zonas metabolicamente ativas, enquanto as BrMS4 formam ilhas de células em rápida divisão rodeadas por territórios relativamente pobres em imunidade. De forma geral, o estudo descobriu que, nas metástases cerebrais—mas não nos tumores primários—a forte ativação da transição epitélio–mesênquima tende a ocorrer junto com maior infiltração de células T, sugerindo que esse programa pode ajudar a abrir a porta para a entrada de células imunes.
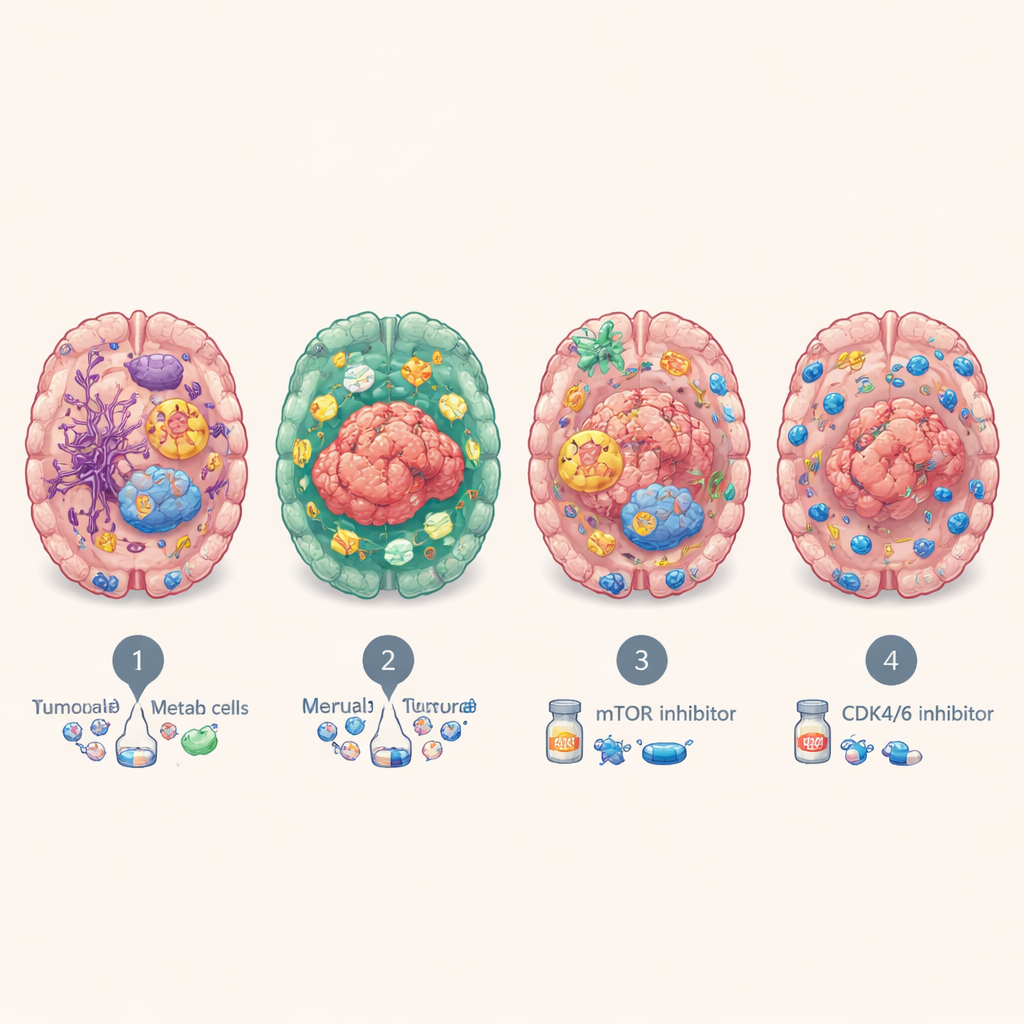
Pistas para tratamento e desfechos dos pacientes
Essas personalidades moleculares não foram apenas acadêmicas. Pacientes com o subtipo imuno-infiltrado BrMS2 tenderam a viver mais do que aqueles com o subtipo proliferativo BrMS4, que teve consistentemente os piores desfechos. Testando drogas em organoides derivados de pacientes, a equipe descobriu que tumores metabólicos BrMS3 foram especialmente sensíveis ao bloqueio da via de sinalização mTOR, que ajuda a controlar crescimento e metabolismo celular, e que os tumores de divisão rápida BrMS4 eram mais vulneráveis a inibidores de CDK4/6, drogas que retardam o ciclo celular. Análises separadas sugeriram que tumores BrMS1 podem responder melhor à radioterapia, enquanto o ambiente inflamado e rico em pontos de controle de BrMS2 poderia torná-lo mais propenso a se beneficiar de imunoterapias que reinvigoram linfócitos T exauridos—embora isso precise ser confirmado diretamente em pacientes com metástases cerebrais.
O que isso significa para pessoas com metástases cerebrais
Este atlas mostra que, uma vez que células cancerosas alcançam o cérebro, elas tendem a convergir para alguns estados biológicos compartilhados que atravessam sua origem anatômica. Entender se a metástase cerebral de uma pessoa é neural-like, rica em imunidade, metabólica ou altamente proliferativa pode, no futuro, orientar tratamentos mais personalizados—como escolher entre radioterapia, imunoterapia ou drogas que miram o metabolismo ou a divisão celular. Embora o trabalho ainda não mude o cuidado padrão, ele fornece um roteiro detalhado para pesquisas futuras e ensaios clínicos destinados a transformar essas vulnerabilidades moleculares em terapias melhores e mais precisas para pacientes com metástases cerebrais.
Citação: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Palavras-chave: metástase cerebral, subtipos tumorais, microambiente tumoral, imunoterapia contra o câncer, metabolismo do câncer