Clear Sky Science · pt
A composição de fosfolipídios afeta fortemente a montagem de proteínas em barril β nas membranas externas bacterianas purificadas
Por que as camadas bacterianas importam
Os “superbactérias” resistentes a medicamentos representam uma ameaça crescente porque muitos antibióticos simplesmente não conseguem ultrapassar suas defesas externas resistentes. Este estudo analisa de perto uma parte chave dessa defesa em bactérias Gram‑negativas como E. coli: um revestimento externo protetor repleto de proteínas em forma de barril e lipídios especializados. Ao separar como a mistura desses lipídios controla a montagem do revestimento externo, os autores revelam pontos fracos que poderão ser explorados no desenvolvimento de futuros antibióticos.
O escudo de dupla camada
Bactérias Gram‑negativas são incomuns porque possuem duas membranas. A membrana interna cuida das funções celulares diárias, enquanto a membrana externa atua como uma capa resistente que impede a entrada de muitas toxinas e antibióticos. Essa camada externa é composta por dois tipos de lipídios: fosfolipídios comuns no lado interno e um lipídio açúcar‑gordura rígido chamado lipopolissacarídeo (LPS) no lado externo. Perfurando essa casca existem muitas proteínas em “beta‑barril” — cilindros ocos que formam poros e portas para nutrientes. Uma máquina molecular chamada BAM (abreviação de barrel assembly machine) é responsável por dobrar essas proteínas na forma correta e inseri‑las na membrana externa.
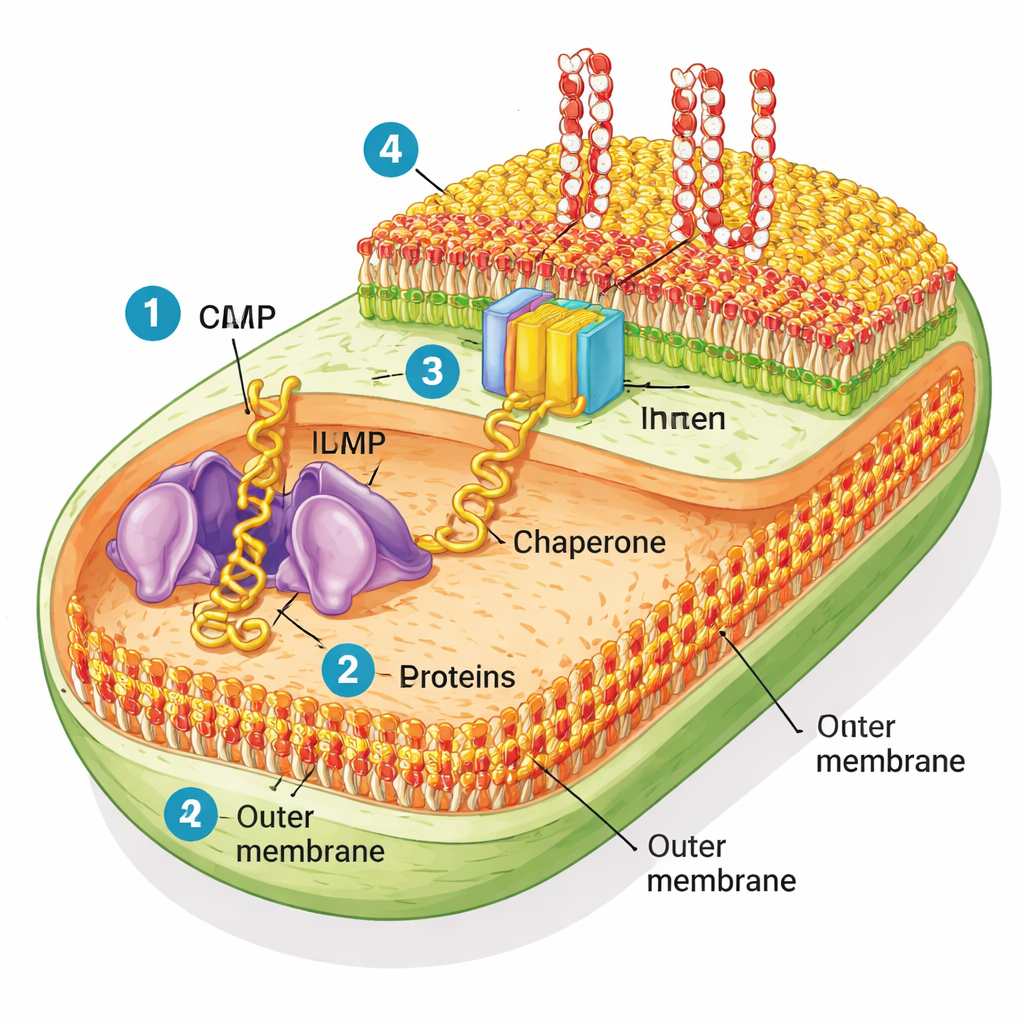
Recriando o revestimento bacteriano em um tubo de ensaio
Para ver quão bem o BAM funciona em um contexto realista, os pesquisadores purificaram pedaços da membrana externa de E. coli, criando pequenas bolhas que chamam de “OMs nativas”. Ao contrário de membranas artificiais simples usadas em muitos estudos de laboratório, essas membranas nativas mantêm sua mistura completa de proteínas e lipídios. A equipe então usou uma fábrica de proteínas sem células para construir novas proteínas de membrana externa do zero e observou se o BAM nessas bolhas nativas conseguia dobrá‑las e inseri‑las. Eles se concentraram em uma proteína modelo em beta‑barril chamada EspP, junto com algumas outras. Quando a proteína auxiliar SurA estava presente, o BAM nas membranas nativas dobrava EspP de forma eficiente, e esse processo foi bloqueado por um antibiótico conhecido que mira o BAM chamado darobactina — evidência clara de que a máquina natural permaneceu ativa.
Quando a mistura de gorduras dá errado
Os autores então perguntaram o que acontece quando o equilíbrio lipídico da membrana externa é perturbado. Eles estudaram linhagens mutantes de E. coli desprovidas de sistemas-chave que normalmente corrigem fosfolipídios deslocados na folha externa. Um sistema, MlaA, recolhe fosfolipídios errantes de volta para a membrana interna; outro, a enzima PldA, os degrada. Usando membranas nativas desses mutantes, a equipe descobriu que a montagem de EspP dirigida pelo BAM caiu de forma perceptível em linhagens sem MlaA e ficou gravemente prejudicada quando PldA estava ausente. Esses efeitos não provieram da perda do próprio BAM ou de outras proteínas principais, que ainda estavam presentes em níveis normais, apontando em vez disso para o ambiente lipídico alterado como a causa.
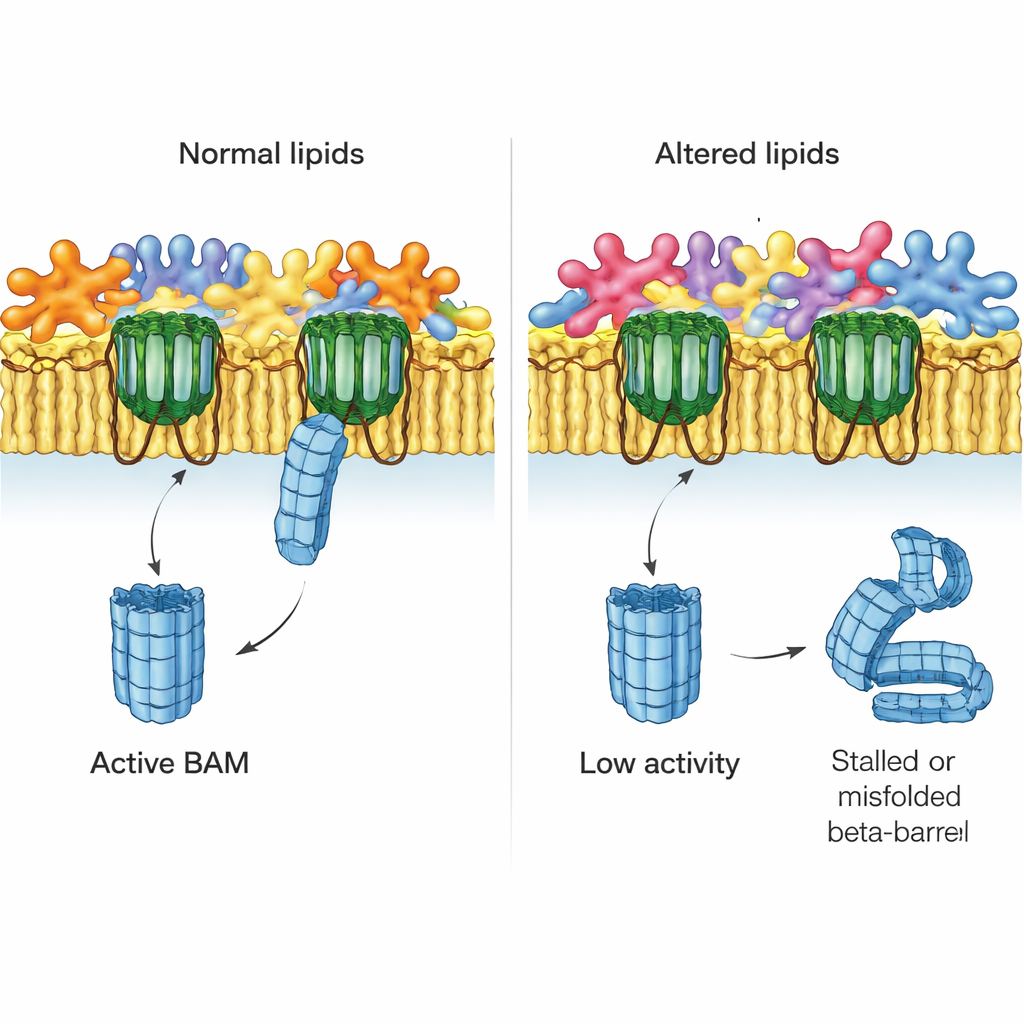
Mapeando o panorama lipídico em detalhe
Para ligar função à química, os pesquisadores desenvolveram um método sensível de espectrometria de massa para catalogar centenas de fosfolipídios individuais em células inteiras e em membranas externas purificadas. Em E. coli normal, eles confirmaram que um tipo de lipídio (fosfatidiletanolamina, ou PE) é enriquecido na membrana externa, enquanto outros (fosfatidilglicerol e cardiolipina) são relativamente empobrecidos ali. Também descobriram que “liso‑lipídios”, que têm apenas uma cauda graxa e tendem a curvar membranas, estão surpreendentemente concentrados na membrana externa. Em linhagens mutantes, especialmente aquelas sem PldA, esses padrões foram embaralhados: as diferenças usuais entre membrana interna e externa diminuíram ou até se inverteram, e os comprimentos e tipos das caudas graxas mudaram. As linhagens com os perfis lipídicos mais perturbados foram as mesmas em que o BAM funcionou pior.
Implicações para estratégias antibióticas
Em conjunto, o trabalho mostra que a membrana externa não é apenas um andaime passivo para proteínas. Sua composição precisa de fosfolipídios influencia fortemente o quão bem o BAM pode construir os poros em beta‑barril que mantêm a bactéria viva. Quando o equilíbrio lipídico é perturbado, menos complexos BAM funcionam corretamente, e alguns trabalham mais lentamente. Embora bactérias vivas possam compensar tais mudanças de maneiras que um sistema in vitro não consegue, este estudo ressalta como ajustar ou perturbar lipídios específicos poderia enfraquecer o revestimento bacteriano. Essa percepção abre novas possibilidades para fármacos que atacam o BAM diretamente ou desestabilizam sutilmente os lipídios da membrana externa, tornando até mesmo as bactérias Gram‑negativas mais resistentes mais vulneráveis.
Citação: Nilaweera, T.D., Brandes, N.T., LaCroix, I.S. et al. Phospholipid composition strongly affects the assembly of β barrel proteins into purified bacterial outer membranes. Nat Commun 17, 1915 (2026). https://doi.org/10.1038/s41467-026-68743-3
Palavras-chave: Bactérias Gram-negativas, proteínas da membrana externa, montagem de beta-barril, lipídios bacterianos, resistência a antibióticos