Clear Sky Science · pt
A quinurenina mede a toxicidade intestinal induzida por quimioterapia por meio da modulação do microbiota intestinal
Por que isso importa para pessoas em quimioterapia
A quimioterapia salva vidas, mas frequentemente vem acompanhada de efeitos colaterais severos no intestino — dor, diarreia, perda de peso — que podem forçar os médicos a reduzir doses ou interromper o tratamento precocemente. Este estudo revela uma reação em cadeia oculta entre uma substância presente no sangue, células do sistema imune e micróbios intestinais que ajuda a explicar por que um fármaco comum contra o câncer, oxaliplatina, pode ser tão agressivo para o intestino, além de apontar novas formas de proteger os pacientes sem enfraquecer a terapia antitumoral.
Um elo químico entre o tratamento e o dano intestinal
Os pesquisadores começaram com pacientes de câncer colorretal recebendo quimioterapia à base de oxaliplatina. Eles compararam amostras de sangue de pessoas que desenvolveram efeitos intestinais graves com as de quem tolerou melhor o tratamento. Usando perfilagem química direcionada, encontraram vários produtos da degradação do aminoácido triptofano elevadas no grupo com alta toxicidade, com uma molécula — L‑quinurenina — destacando‑se como a mais fortemente aumentada. Pacientes com mais L‑quinurenina no sangue também mostraram mais sinais de inflamação e contagens mais baixas de leucócitos, sugerindo que essa molécula pode estar ligada diretamente ao dano relacionado ao tratamento.
Provando causalidade em camundongos
Para ir além da correlação, a equipe recorreu a modelos murinos. Quando camundongos saudáveis receberam altas doses de oxaliplatina, desenvolveram sinais clássicos de lesão intestinal: perda de peso, cólons encurtados, inchaço da parede intestinal, menos células em divisão e mais células morrendo no revestimento intestinal. Esses animais também apresentaram um aumento acentuado de L‑quinurenina no sangue, espelhando os dados humanos. Quando os pesquisadores administraram L‑quinurenina adicional a camundongos tratados com oxaliplatina, o dano intestinal tornou‑se ainda mais grave — porém o poder de matar o tumor do fármaco permaneceu intacto. Por outro lado, quando removeram ou bloquearam a enzima IDO1, que converte triptofano em L‑quinurenina, os camundongos ficaram bem mais resistentes à toxicidade intestinal enquanto ainda se beneficiavam da quimioterapia.
Células imunes e micróbios intestinais no fogo cruzado
Aprofundando, os cientistas perguntaram quais células eram responsáveis por produzir o excesso de L‑quinurenina durante o tratamento. Concluíram que a oxaliplatina estimula certas células imunes (linfócitos T CD8) a liberarem a proteína sinalizadora interferon‑gama, que então ativa a IDO1 em células mieloides próximas — uma classe de glóbulos brancos. Camundongos geneticamente alterados para que apenas suas células mieloides não expressassem IDO1 produziram muito menos L‑quinurenina e foram protegidos da lesão intestinal, enquanto deletar IDO1 apenas nas células do revestimento intestinal teve pouco efeito. Ao mesmo tempo, a composição do microbiota intestinal mudou. Em camundongos normais, oxaliplatina e níveis altos de L‑quinurenina foram associados à perda de uma bactéria benéfica, Lactobacillus johnsonii. Em contraste, animais com L‑quinurenina reduzida mantiveram níveis maiores de L. johnsonii. Quando as bactérias intestinais foram eliminadas com antibióticos, o efeito protetor da baixa L‑quinurenina desapareceu, e quando bactérias de camundongos com baixos níveis de quinurenina foram transplantadas para camundongos normais, esses receptores ficaram mais resistentes ao dano intestinal causado pela oxaliplatina.
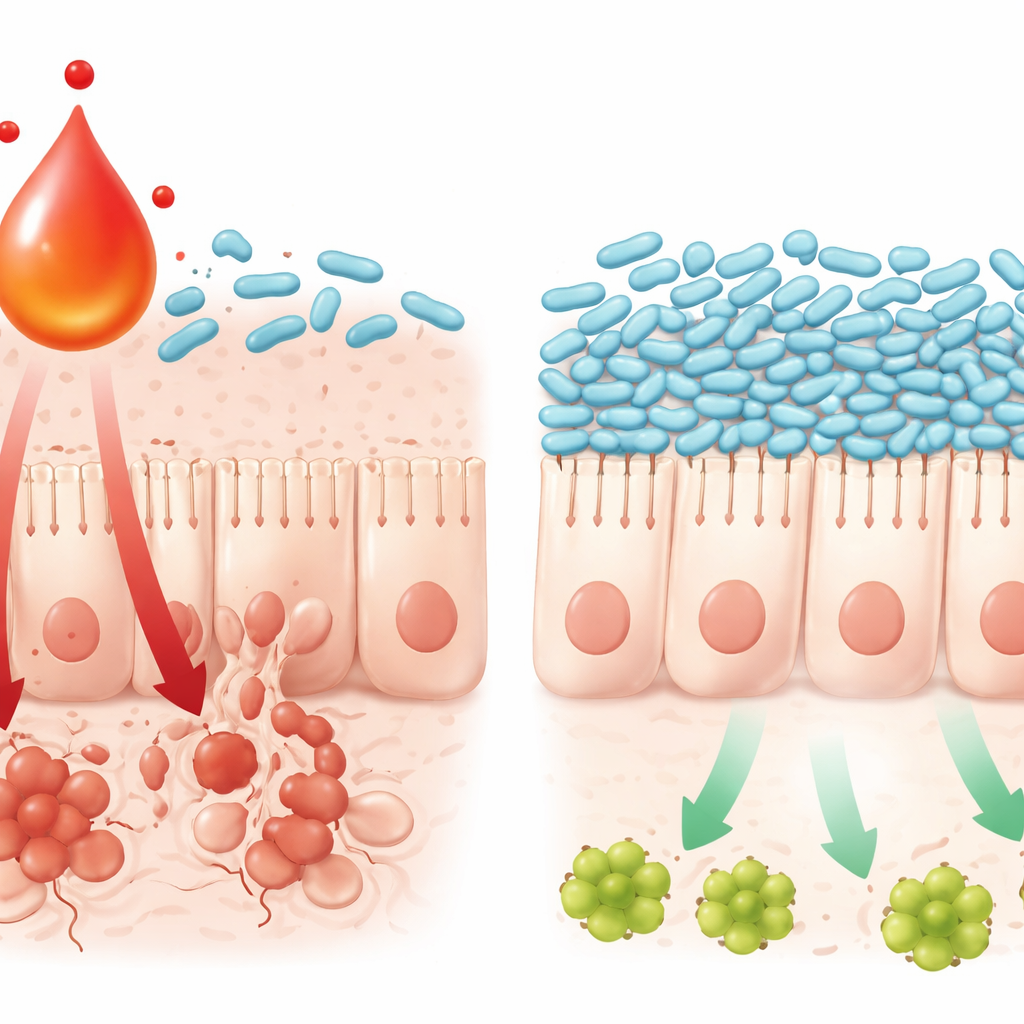
Como um metabólito promove a morte celular no intestino
O estudo também traçou como essa interação química–microbiana danifica o revestimento intestinal. Níveis altos de L‑quinurenina estiveram associados a maior atividade de uma via inflamatória conhecida no tecido intestinal, a via TNFα/JNK, que empurra as células rumo à morte programada. Em culturas celulares, a combinação de oxaliplatina com L‑quinurenina tornou as células intestinais mais propensas a ativar essa via e morrer, enquanto a adição da bactéria L. johnsonii atenuou o sinal e preservou a sobrevivência celular. A própria L‑quinurenina podia retardar o crescimento e prejudicar os mecanismos de sobrevivência de L. johnsonii em placas de cultura, ajudando a explicar por que a bactéria desaparece quando o metabólito se acumula. Juntos, esses achados delineiam um ciclo auto‑reforçador: a quimioterapia desencadeia sinalização imune, as células imunes elevam a L‑quinurenina, isso desestabiliza bactérias amigas como L. johnsonii, e a comunidade microbiana alterada amplia sinais inflamatórios que matam as células do intestino.
Novas formas de proteger pacientes durante o tratamento
De forma encorajadora, o trabalho também aponta estratégias práticas. Tratar camundongos com um fármaco chamado Epacadostat, que inibe a IDO1, reduziu os níveis de L‑quinurenina e diminuiu significativamente a lesão intestinal induzida pela oxaliplatina sem reduzir o controle tumoral. Numa abordagem complementar, a equipe engenheirou uma cepa inofensiva de E. coli para superproduzir uma enzima que degrada L‑quinurenina no intestino. Camundongos recebendo essas bactérias modificadas foram igualmente protegidos da toxicidade intestinal, novamente sem comprometer os efeitos anticâncer da quimioterapia. Suplementar L. johnsonii também aliviou sintomas e preservou a estrutura intestinal.
O que isso significa para pessoas com câncer
Em conjunto, este estudo revela que um único metabólito induzido pelo tratamento — a L‑quinurenina — atua como um intermediário chave entre a quimioterapia, o sistema imune, os micróbios intestinais e a lesão intestinal. Ao demonstrar que bloquear sua produção, aumentar sua degradação ou restaurar bactérias protetoras pode atenuar o impacto da quimioterapia no intestino, a pesquisa abre caminho para terapias complementares que mantenham os pacientes mais fortes e confortáveis enquanto enfrentam o câncer.
Citação: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
Palavras-chave: efeitos colaterais da quimioterapia, microbioma intestinal, metabolismo do triptofano, L-quinurenina, câncer colorretal