Clear Sky Science · pt
Acoplamento eletroquímico C–N via modulação de adsorção: síntese seletiva de aminas a partir de 5‑hidroximetilfurfural derivado de biomassa
Transformando açúcares vegetais em medicamentos úteis
Medicamentos modernos, agroquímicos e materiais avançados dependem fortemente de aminas — moléculas contendo nitrogênio presentes desde remédios para azia até protetores de culturas. Hoje, muitas aminas são produzidas usando altas temperaturas, altas pressões e agentes redutores perigosos derivados de combustíveis fósseis. Este estudo explora uma rota mais limpa: usar eletricidade e catalisadores de prata para converter um derivado de açúcar de origem vegetal chamado 5‑hidroximetilfurfural (HMF) em uma amina valiosa usada na produção farmacêutica, enquanto direciona cuidadosamente a reação para evitar subprodutos indesejados.
Um caminho mais limpo da biomassa às aminas
O HMF pode ser obtido a partir de carboidratos na biomassa, tornando‑o um ponto de partida atraente para a química sustentável. Combinar HMF com metilamina pode gerar um intermediário chave conhecido como MAMF, importante na fabricação do medicamento ranitidina e compostos relacionados. A “aminação redutora” convencional do HMF emprega hidrogênio molecular ou outros redutores químicos fortes, que consomem muita energia e geram subprodutos indesejados. Aqui, os autores substituem esses reagentes por elétrons fornecidos por uma fonte externa de energia, realizando a transformação eletroquimicamente em soluções aquosas e perto da temperatura ambiente. A questão central é como projetar o eletrodo metálico para que a ligação C–N desejada se forme eficientemente enquanto reações concorrentes — simples hidrogenação e dimerização C–C — são suprimidas.
Por que a forma da superfície importa
A equipe foca na prata (Ag) como material do eletrodo porque ela adsorve o HMF nem fraca nem fortemente demais, um equilíbrio importante para a seletividade. Mas a prata não é apenas uma superfície única: em escala atômica, ela pode expor diferentes “faces” com arranjos de átomos distintos. Os pesquisadores sintetizam dois catalisadores de prata bem definidos: nanopartículas quase esféricas que apresentam principalmente a face (111) e nanocubos dominados pela face (100). Usando microscopia eletrônica e técnicas de raios X, eles confirmam essas formas e superfícies. Quando esses catalisadores são testados em uma célula eletroquímica contendo HMF e metilamina, a diferença é marcante. As nanopartículas ricas em (111) alcançam uma eficiência faradaica de cerca de 89% e seletividade em torno de 90% para a amina alvo em tensões modestas, superando claramente os nanocubos ricos em (100), que tendem a gerar mais subprodutos hidrogenados e dimerizados.
Observando moléculas aterrissarem e reagirem
Para entender por que uma forma funciona melhor, os autores observam como o HMF e intermediários reacionais se ligam às superfícies de prata em tempo real. Eles usam espectroscopia Raman in situ, que rastreia impressões vibracionais de moléculas na interface do eletrodo, e comparam esses experimentos com cálculos quântico‑químicos detalhados (DFT). Nas nanopartículas dominadas por (111), o HMF adota uma configuração em que o carbono carbonílico reativo fica próximo à superfície de prata sem ser excessivamente estabilizado. Esse arranjo torna o grupo carbonila mais positivamente polarizado e mais fácil para a metilamina atacar, formando um intermediário “imina” de curta duração que é então rapidamente reduzido à amina desejada. Nos nanocubos dominados por (100), ao contrário, o HMF se liga tanto pelo carbono quanto pelo oxigênio da carbonila, prendendo a ligação com demasiada força e canalizando elétrons para hidrogenação simples ou formação de dímeros em vez do acoplamento C–N.
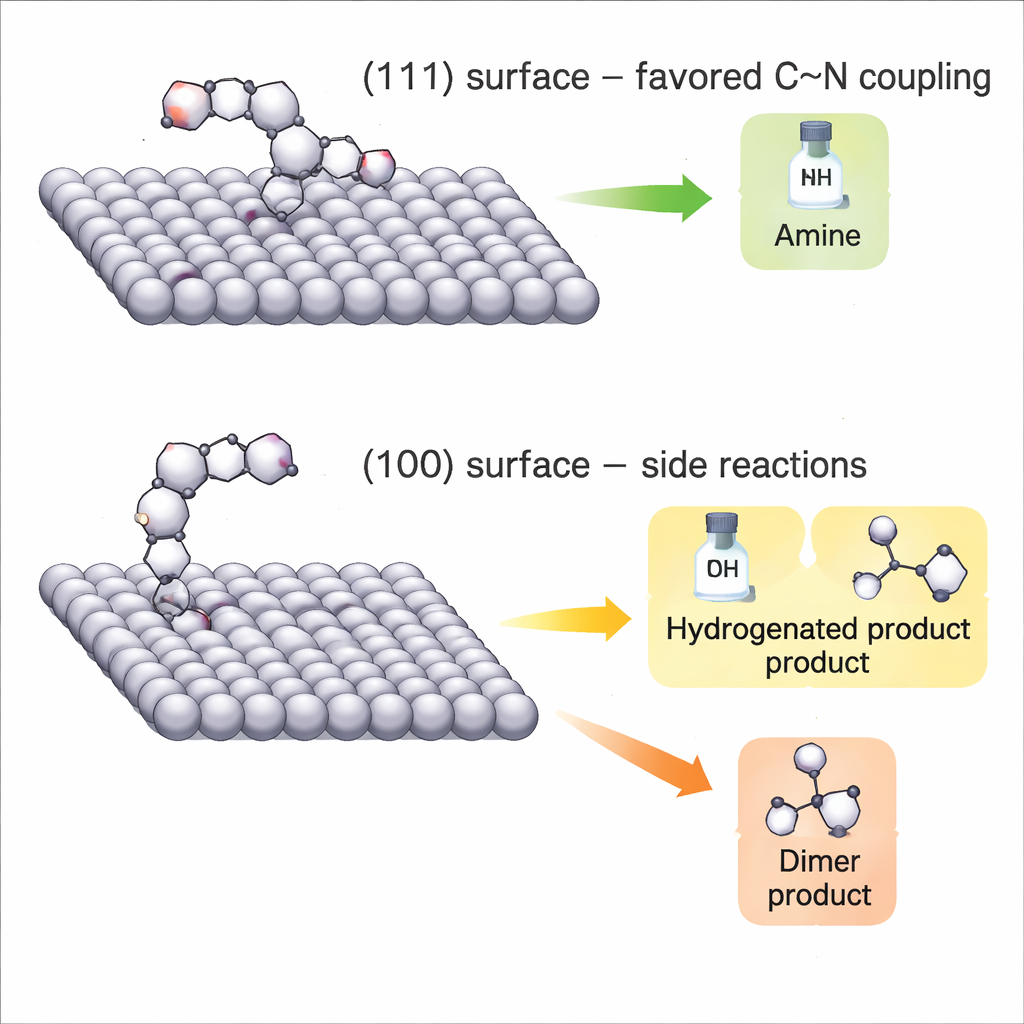
Equilibrando o hidrogênio e evitando desvios
Medições eletroquímicas lançam mais luz sobre a coreografia da reação. A análise cinética mostra que a formação da ligação C–N nas nanopartículas (111) procede mais facilmente do que a reação concorrente de evolução de hidrogênio a partir da água. Experimentos isotópicos usando água pesada revelam que transferências acopladas de próton e elétron são centrais para converter a imina na amina final. Testes de impedância indicam transferência de carga mais rápida nas superfícies (111), e RMN em tempo resolvido confirma que a imina nunca se acumula em solução porque é ou rapidamente reduzida na superfície ou hidrolisada sob as condições localmente alcalinas próximas ao cátodo. Ao ajustar a superfície para que a hidrogenação da imina seja rápida — mas não tão rápida a ponto de reduzir outras ligações primeiro — os autores mantêm a reação no caminho desejado. Eles também mostram que a mesma preferência por face melhora a formação de aminas a partir de outras moléculas à base de furfural e mesmo quando a amônia substitui a metilamina, sugerindo uma regra de projeto de ampla utilidade.
Regras de projeto para eletroquímica mais verde
Para não especialistas, a conclusão principal é que a “textura” microscópica de uma superfície metálica pode direcionar de modo decisivo quais produtos se formam em reações movidas a eletricidade. Ao fabricar nanopartículas de prata que expõem majoritariamente faces (111), os pesquisadores guiam um bloco de construção derivado de plantas para uma amina específica usada em farmacêuticos com alta eficiência e mínimo desperdício. Este trabalho demonstra como controlar a maneira como moléculas se assentam e se movimentam em um catalisador — em vez de apenas qual metal é usado — pode desbloquear rotas mais verdes para químicos importantes e potencialmente ajudar a traduzir biomassa e eletricidade renovável em produtos cotidianos de forma mais sustentável.
Citação: Lai, D., Yu, J., Ma, ZA. et al. Electrochemical C–N coupling via adsorption modulation: selective synthesis of amines from biomass-derived 5-hydroxymethylfurfural. Nat Commun 17, 1892 (2026). https://doi.org/10.1038/s41467-026-68734-4
Palavras-chave: aminação eletroquímica, valorização da biomassa, nanopartículas de prata, faces da superfície do catalisador, química verde