Clear Sky Science · pt
Determinação baseada em click da acumulação de moléculas em Escherichia coli
Por que pequenas drogas têm dificuldade para atingir bactérias perigosas
A medicina moderna depende de antibióticos, mas algumas das bactérias mais perigosas hoje estão protegidas por paredes externas resistentes que impedem a entrada de muitos fármacos. Bactérias Gram‑negativas, como Escherichia coli, possuem uma barreira de membrana externa particularmente eficaz, o que torna difícil projetar medicamentos que realmente penetrem e alcancem seus alvos. Este artigo apresenta um novo ensaio de laboratório, chamado CHAMP, que permite aos cientistas medir rapidamente quão bem milhares de pequenas moléculas conseguem contornar essas defesas e se acumular dentro de células vivas de E. coli.
Uma nova maneira de observar drogas entrando em células bacterianas
A descoberta tradicional de antibióticos baseava‑se em compostos naturais e testes simples de crescimento para ver se as bactérias viviam ou morriam. Esses testes não revelam quanto do fármaco realmente entrou na célula, nem onde ele foi depois de penetrar. Os autores propuseram construir um método direto e amplamente utilizável para rastrear a entrada de drogas no citosol bacteriano — o fluido interior onde muitos alvos antibióticos residem. O objetivo foi ir além de leituras grosseiras como a concentração inibitória mínima, que misturam efeitos de captação do fármaco, ligação ao alvo e biologia subsequente, e em vez disso obter uma medida limpa da acumulação intracelular.
Transformando bactérias em pequenos registradores químicos
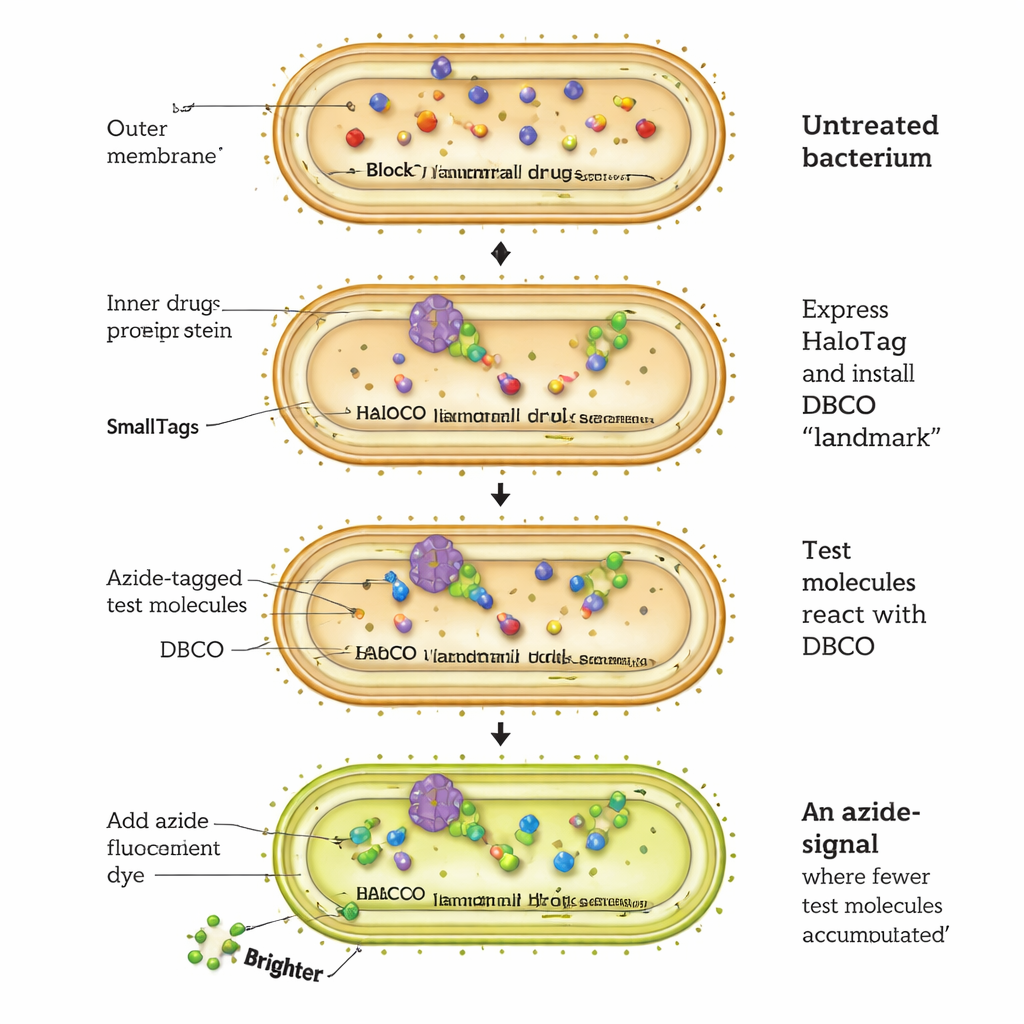
O ensaio CHAMP funciona reprogramando uma proteína bacteriana chamada HaloTag em uma espécie de plataforma de aterrissagem molecular. Células de E. coli são geneticamente modificadas para produzir HaloTag no citosol. Primeiro, os pesquisadores ligam uma alça química especial — um alquino tensionado chamado DBCO — ao HaloTag usando um curto conector cloroalcano. Em seguida, expõem as bactérias a moléculas‑teste que carregam cada uma uma pequena etiqueta azida. Somente as moléculas‑teste que atravessam a membrana externa, passam pela membrana interna e alcançam o citosol podem reagir com a alça DBCO numa reação altamente seletiva de “click”, marcando permanentemente o HaloTag. Finalmente, as células são tratadas com um corante fluorescente azida‑marcado que só se liga aos DBCO ainda não ocupados. Quanto mais intensa a fluorescência, menos moléculas‑teste chegaram ao citosol; células mais escuras indicam maior acumulação.
Investigando como química e biologia moldam a entrada de fármacos
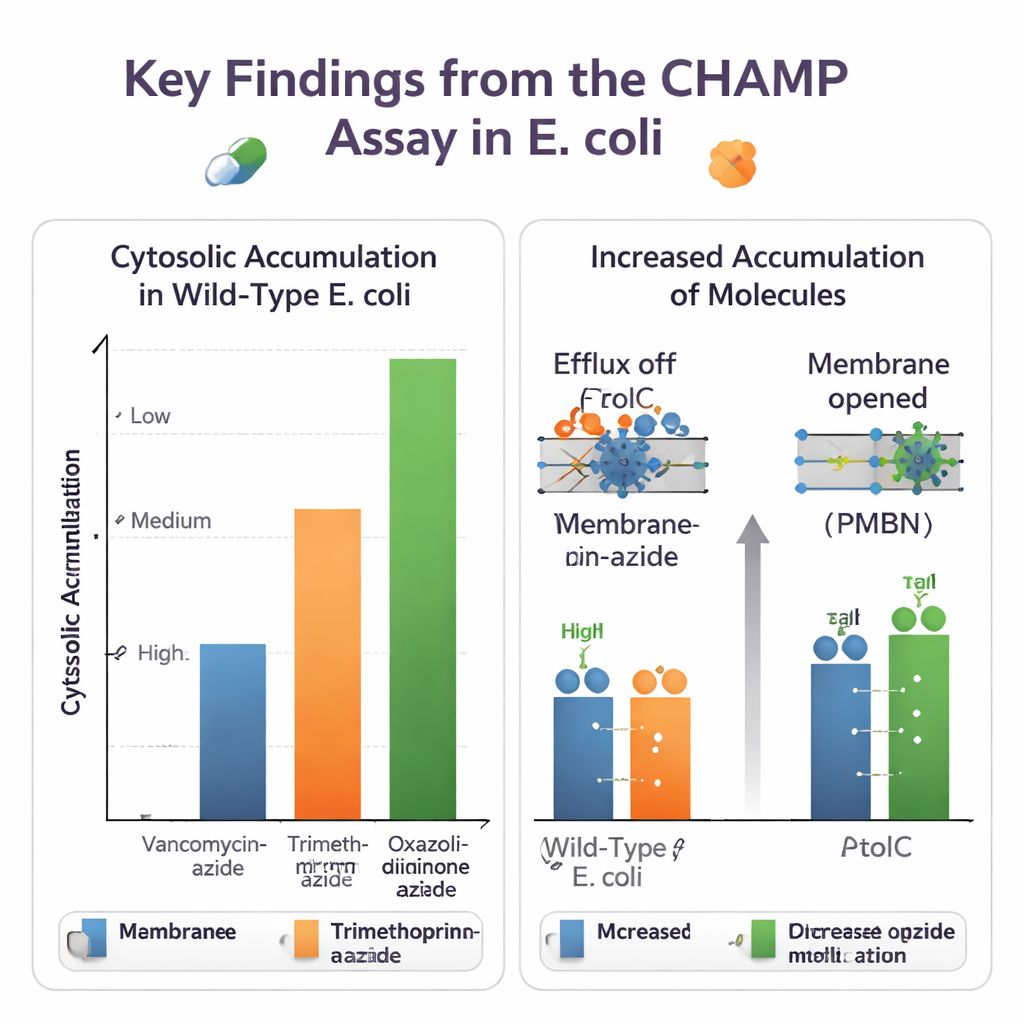
Usando o CHAMP, a equipe primeiro ajustou a expressão do HaloTag, a quantidade de âncora DBCO e a escolha dos corantes fluorescentes para obter uma janela de sinal grande e confiável. Em seguida, empregaram conjuntos de pequenas moléculas estreitamente relacionadas para ver como ajustes químicos afetam a entrada. Converter ácidos carboxílicos em amidas e adicionar ou remover grupos amino básicos poderia alterar notavelmente os níveis citosólicos. Em muitos casos, aminas primárias aumentaram a acumulação, ecoando regras independentes de “eNTRy” desenvolvidas por outros grupos. O ensaio também funcionou com versões azida‑marcadas de antibióticos reais, revelando grandes diferenças: fármacos volumosos como vancomicina mal alcançaram o citosol, enquanto antibióticos menores, como derivados de trimetoprim e alguns oxazolidinonas, entraram muito mais facilmente.
Desmascarando defesas bacterianas que bombeiam fármacos de volta para fora
Como o método é executado em bactérias vivas e geneticamente programáveis, ele pode desvendar os papéis de diferentes defesas celulares. Os autores compararam E. coli normal com cepas que carecem de TolC, um componente chave de uma bomba de efluxo multidroga importante, ou com células tratadas com um inibidor de TolC de pequena molécula. Para novobiocina e vários outros antibióticos azida‑marcados, o CHAMP mostrou acumulação citosólica claramente maior quando TolC foi desabilitado, confirmando esses compostos como substratos de efluxo. Também testaram maneiras de afrouxar a barreira da membrana externa, quimicamente com o peptídeo PMBN ou geneticamente ao superexpressar um poro amplamente aberto. Muitas moléculas que anteriormente acumulavam mal exibiram grandes ganhos quando a membrana foi permeabilizada, ressaltando como entrada e efluxo atuam conjuntamente para determinar os níveis internos de fármaco.
Escalando para milhares de moléculas para identificar padrões e regras
Para demonstrar real alto rendimento, os pesquisadores rastrearam um conjunto comercial de 404 compostos azida‑marcados e uma biblioteca personalizada de 1.152 moléculas contendo azida. Eles mediram a acumulação em vários contextos bacterianos, incluindo células não tratadas, células tratadas com PMBN, células hiperporinizadas e células hiperporinizadas sem TolC. Ao comparar a mesma molécula nessas condições, puderam ver quais mudanças eram devidas à biologia celular em vez de idiossincrasias da velocidade da reação click. Combinando dados CHAMP com análise computacional, relacionaram certas características físico‑químicas — como área de superfície polar, capacidade de formar ligações de hidrogênio e scaffolds de anel específicos — a maior reconhecimento por efluxo baseado em TolC. Esse tipo de perfil em larga escala começa a delinear regras de projeto para moléculas que ou evitam bombas ou exploram porinas de forma mais eficaz.
O que isso significa para futuros antibióticos
Em termos simples, este trabalho transforma E. coli em um sensor de alto rendimento que informa exatamente quanto de um composto‑teste chega à parte da célula onde muitos alvos de fármacos residem. O CHAMP não substitui testes de atividade letal das bactérias, mas preenche uma lacuna crucial ao separar “entrar” de “causar dano”. Com a capacidade de medir mais de mil moléculas em diferentes cepas mutantes ou quimicamente alteradas em questão de dias, os pesquisadores podem agora aprender sistematicamente quais características químicas promovem entrada, reduzem o efluxo ou se beneficiam de parceiros que perturbam a membrana. Esse conhecimento deve acelerar o projeto de novos antibióticos e fármacos auxiliares capazes de romper as formidáveis defesas de patógenos Gram‑negativos antes que a resistência comprometa ainda mais o arsenal antibiótico.
Citação: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Palavras-chave: resistência a antibióticos, Escherichia coli, permeabilidade de fármacos, bombas de efluxo, química click