Clear Sky Science · pt
Microscopia de iluminação estruturada cega em alta velocidade via desenrolamento não supervisionado de algoritmo
Filmes mais nítidos da vida dentro das células
A biologia moderna depende muitas vezes de observar células vivas em ação, mas muitas estruturas-chave são simplesmente pequenas e rápidas demais para serem capturadas com clareza por microscópios comuns. Este artigo apresenta uma nova maneira de transformar imagens borradas, capturadas rapidamente, em filmes nítidos e com superdetalhe em tempo real, sem necessidade de hardware perfeitamente afinado. O método, chamado microscopia de iluminação estruturada cega desenrolada (UBSIM), promete tornar a imageamento celular avançado e de alta velocidade mais acessível a laboratórios de biologia do dia a dia.
Por que microscópios comuns ficam aquém
Microscópios ópticos tradicionais são limitados pela difração, uma propriedade básica da luz que desbota detalhes finos menores que algumas centenas de nanômetros. A microscopia de iluminação estruturada (SIM) enfrenta isso projetando padrões de luz sobre a amostra e usando a interferência resultante para extrair detalhes extras, aproximadamente dobrando a resolução. Contudo, a SIM clássica exige padrões de iluminação precisamente conhecidos e calibração cuidadosa, o que pode ser caro e frágil. Uma variante mais nova, a blind-SIM, relaxa essas exigências de hardware ao permitir padrões aleatórios e resolver tanto a amostra quanto a iluminação a partir dos dados. A desvantagem é que esse processo de solução é lento e iterativo, levando segundos a minutos por quadro — tempo demais para filmes em tempo real de células vivas.
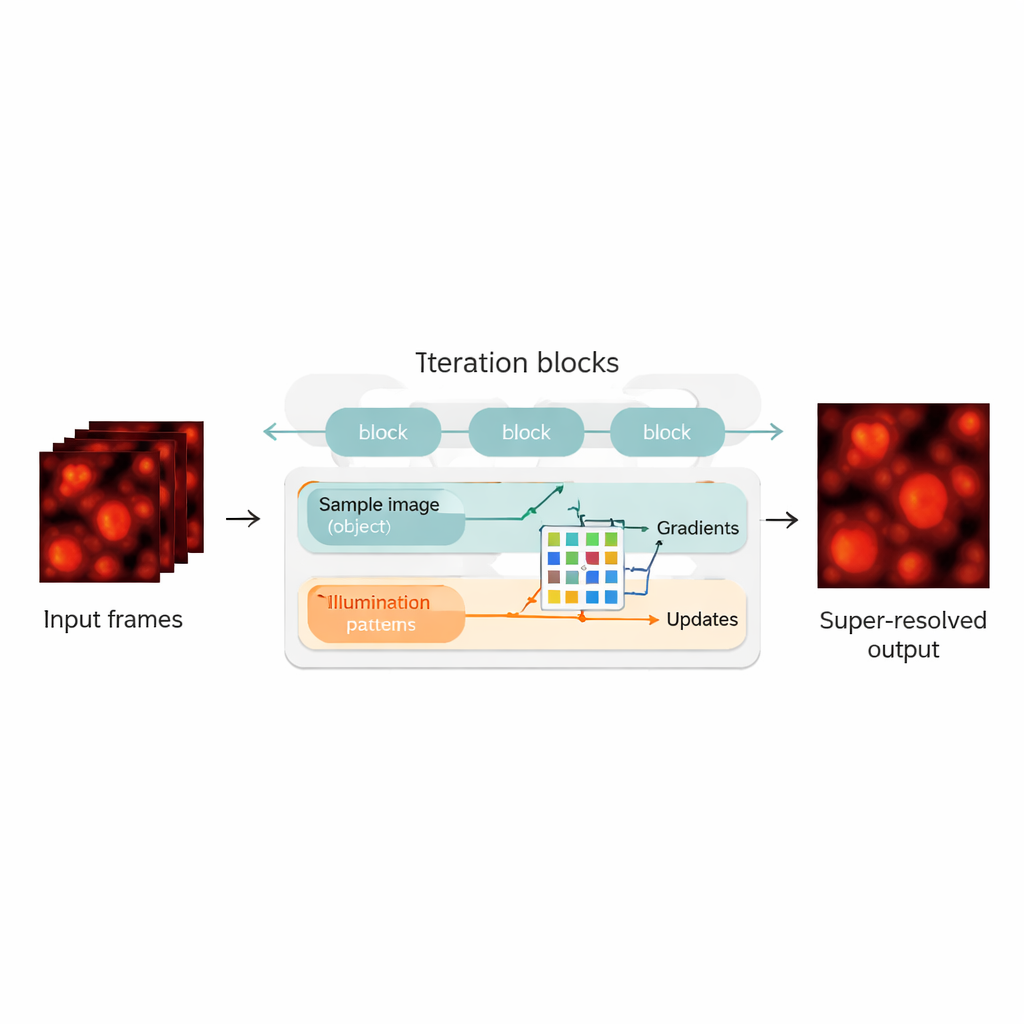
Combinando física com redes neurais
Os autores preenchem essa lacuna ao redesenhar a reconstrução blind-SIM como um híbrido entre um modelo baseado em física e uma rede neural. Eles “desenrolam” o algoritmo iterativo original — cada iteração torna-se uma camada em uma rede neural, formando uma cadeia de blocos de atualização. Dentro de cada bloco, o método calcula o quanto a estimativa atual da amostra e da iluminação explica as imagens medidas, calcula gradientes (direções de melhoria) e então alimenta esses sinais em uma rede neural convolucional compacta. Essa rede aprende a fazer passos de correção mais inteligentes, funcionando como um acelerador automaticamente afinado para o algoritmo original. Fundamentalmente, o UBSIM é treinado de forma não supervisionada: em vez de precisar de imagens perfeitas como verdade terrestre, ele só requer o modelo físico de como a luz atravessa o microscópio. Isso reduz o risco de a rede “alucinar” estruturas plausíveis, mas incorretas.
Rápido, preciso e menos sujeito a suposições
Para testar o UBSIM, a equipe primeiro usou imagens de microscopia simuladas onde as estruturas reais subjacentes são conhecidas. Eles mostraram que o UBSIM recupera cerca do dobro da resolução de imagens widefield ordinárias, comparável à blind-SIM padrão, mas roda de duas a três ordens de magnitude mais rápido — uma imagem de 256×256 pode ser reconstruída em cerca de 10 milissegundos em vez de segundos. Pontuações de qualidade de imagem, incluindo erro, similaridade e medidas de relação sinal-ruído, melhoraram de forma marcante em relação às imagens convencionais. O UBSIM também provou ser mais confiável do que redes populares de super-resolução por aprendizado profundo quando confrontado com dados desconhecidos. Enquanto redes padrão treinadas em um tipo de estrutura tendem a imprimir esse padrão em amostras novas e diferentes — introduzindo artefatos sutis, porém enganosos — o UBSIM manteve fidelidade consistente, pois está ancorado na física da imageamento subjacente em vez de depender apenas de exemplos visuais.
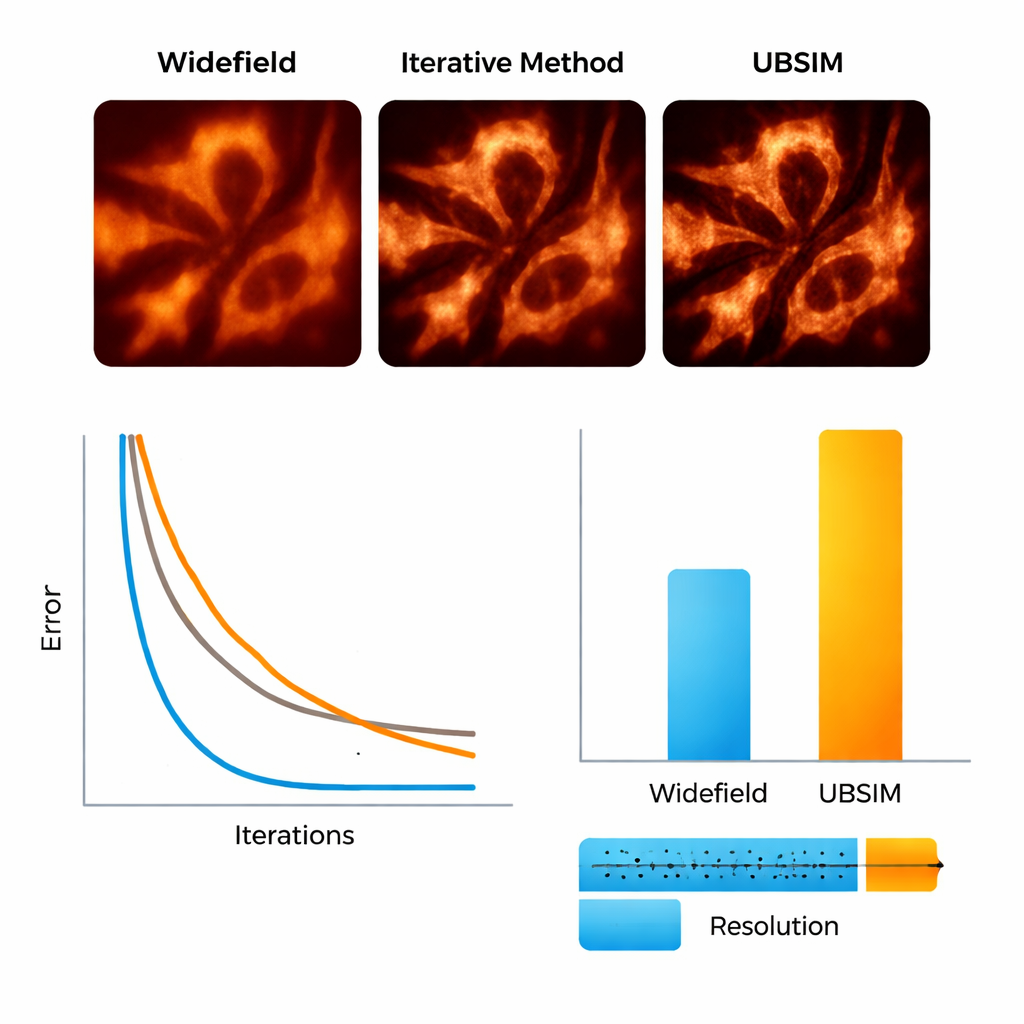
Vendo esqueletos e membranas celulares em movimento
Os pesquisadores então aplicaram o método em amostras biológicas reais. Usando um sistema flexível que projeta padrões de speckle aleatórios sobre células vivas, eles imagearam filamentos de actina — a “treliça” proteica dentro das células — e o retículo endoplasmático (RE), uma rede membranosa ramificada envolvida na produção de proteínas e em respostas ao estresse celular. Com o UBSIM, fibras de actina que apareciam como faixas difusas em imagens ordinárias tornaram-se fios nitidamente separados, com a resolução melhorando de aproximadamente 300 nanômetros para cerca de 150 nanômetros. O mais notável foi que o UBSIM possibilitou super-resolução em taxa de vídeo: capturando dados brutos a até 100 quadros por segundo e reconstruindo a até 50 quadros super-resolvidos por segundo, a equipe pôde observar túbulos do RE crescerem, colapsarem e se reorganizarem em tempo real. Essas dinâmicas, ocorrendo em frações de segundo a alguns segundos, normalmente são difíceis de visualizar com detalhe suficiente.
O que isso significa para o futuro da imageamento celular
Para não-especialistas, a principal conclusão é que o UBSIM torna muito mais prático observar estruturas celulares minúsculas em movimento, em tempo real, com clareza além dos limites normais dos microscópios ópticos — tudo isso sem exigir calibração perfeita do hardware ou conjuntos massivos de dados de treinamento. Ao combinar a confiabilidade de modelos baseados em física com a velocidade das redes neurais modernas, essa abordagem transforma pilhas de imagens ruidosas e padronizadas em filmes ultranitidos e confiáveis, rápido o suficiente para experimentos de rotina. À medida que o método for refinado e combinado com estratégias de iluminação melhores, ele poderá ajudar pesquisadores a investigar como organelas como o RE respondem ao estresse, como os esqueletos celulares se reorganizam durante movimentação ou divisão, e como doenças alteram a arquitetura celular em escala nanométrica.
Citação: Burns, Z., Zhao, J., Sahan, A.Z. et al. High-speed blind structured illumination microscopy via unsupervised algorithm unrolling. Nat Commun 17, 1967 (2026). https://doi.org/10.1038/s41467-026-68693-w
Palavras-chave: microscopia de super-resolução, iluminação estruturada, aprendizado profundo, imagem de células vivas, dinâmica do retículo endoplasmático