Clear Sky Science · pt
Percepções funcionais e estruturais sobre as interações entre β-Arrestina 1 e Gαs ou Gαi1
Por que isso importa para a saúde e a medicina
Muitos medicamentos de hoje, de anti-histamínicos a fármacos cardíacos e tratamentos psiquiátricos, atuam sobre uma grande família de proteínas de superfície celular chamadas receptores acoplados à proteína G, ou GPCRs. Esses receptores transmitem mensagens para dentro da célula usando dois ajudantes principais, as proteínas G e as chamadas beta-arrestinas. Este estudo investiga como uma beta-arrestina (beta-arrestina 1) conversa diretamente com dois tipos de subunidades G dentro da célula. Entender essa conversa oculta pode ajudar cientistas a projetar medicamentos mais precisos e com menos efeitos colaterais, ao ajustar como os sinais fluem dentro de nossas células.
Dois mensageiros principais dentro das nossas células
Quando um hormônio ou remédio se liga a um GPCR na superfície celular, ele desencadeia duas rotas amplas de comunicação. Uma rota usa proteínas G, que ligam e desligam como temporizadores moleculares ao trocar uma pequena molécula (GDP) por outra (GTP). A outra rota usa beta-arrestinas, que podem tanto interromper a sinalização via proteínas G quanto iniciar suas próprias vias de sinalização. Por muito tempo, os cientistas estudaram principalmente como os receptores se comunicam separadamente com proteínas G ou com beta-arrestinas. Trabalhos mais recentes sugeriram que proteínas G e beta-arrestinas também podem se ligar entre si ou até formar grandes “mega-complexos” com o receptor. Mas os detalhes de como essas proteínas se conectam e o que isso significa para a sinalização permaneceram incertos.
Medindo quem se liga a quem
No estudo, os pesquisadores focaram na beta-arrestina 1 e em duas subunidades alfa de proteínas G: Gαs, que normalmente estimula a atividade celular, e Gαi1, que geralmente a reduz. Usando uma técnica sensível de ligação, eles testaram quão fortemente a beta-arrestina 1 purificada e cada proteína G se unem em diferentes condições. Descobriram que o fator chave não é se a proteína G está “ligada” ou “desligada”, mas se a beta-arrestina 1 está em uma forma mais ativa e flexível. Uma versão de beta-arrestina 1 sem sua cauda — que se comporta como um conjunto solto e ativo de conformações — ligou-se fortemente tanto a Gαs quanto a Gαi1. Em contraste, a forma em repouso da beta-arrestina 1, ou uma forma travada por um peptídeo semelhante à cauda do receptor, ligou-se fracamente ou não se ligou. Isso sugere que as proteínas G reconhecem preferencialmente a beta-arrestina 1 quando ela amostra conformações do tipo ativo que podem existir após a ativação do receptor. 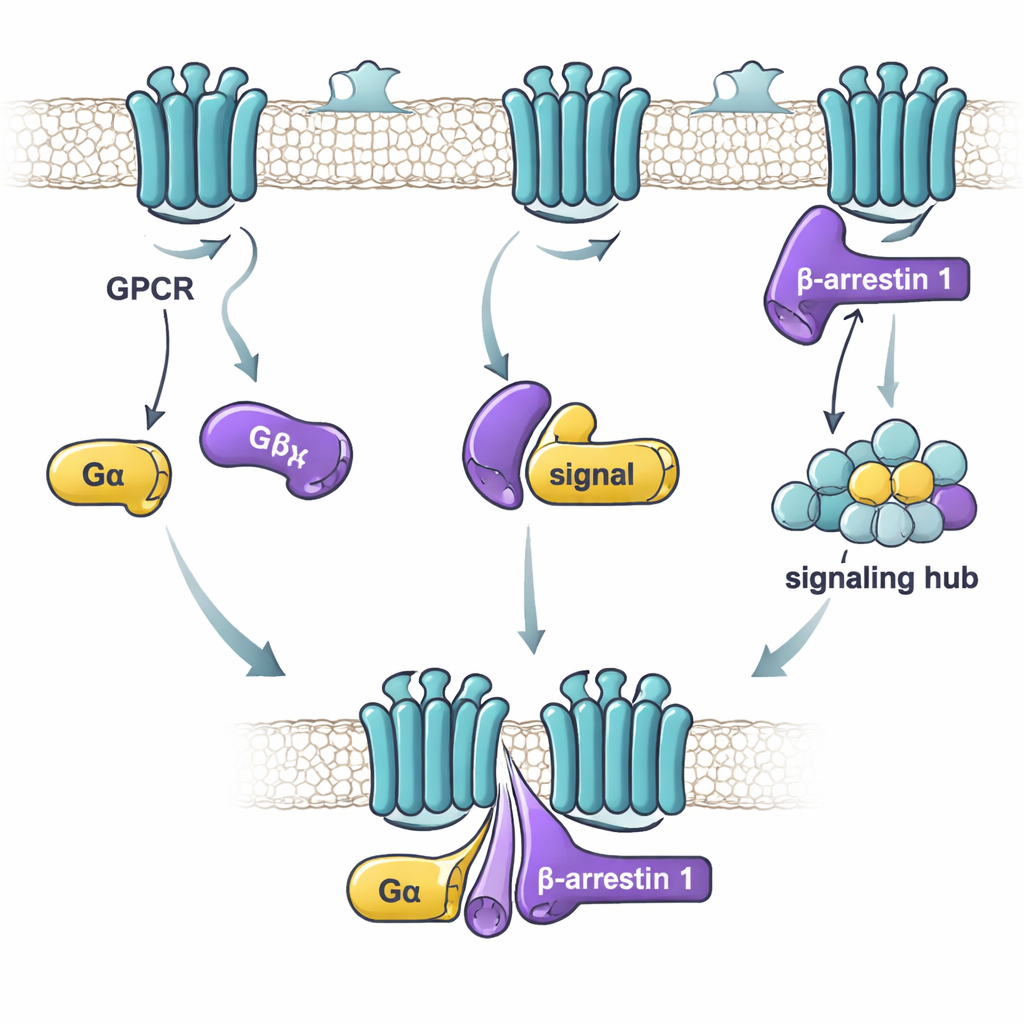
Observando mudanças sutis de forma
Para ver como a ligação afeta a conformação das proteínas, a equipe usou um método que rastreia quão rapidamente átomos de hidrogênio no esqueleto protéico trocam com hidrogênio pesado do solvente. Trocas mais lentas geralmente significam que uma região ficou mais protegida ou rígida; trocas mais rápidas indicam que ficou mais flexível ou exposta. Quando o fragmento de beta-arrestina 1 com conformação tipo-ativa se ligou a Gαs ou Gαi1, ambas as proteínas G mostraram mudanças claras de padrão em várias regiões, indicando que elas estavam se remodelando em torno do complexo. Em contraste, a própria beta-arrestina 1 mudou apenas levemente, principalmente em laços flexíveis. Trabalhando com domínios isolados das proteínas G, os pesquisadores também demonstraram que tanto a porção catalítica principal “tipo Ras” quanto a porção helicoidal alfa ao redor contribuem para a ligação. Para Gαs, a região helicoidal tem um papel particularmente forte; para Gαi1, ambas as regiões importam em proporções aproximadamente iguais.
Função sem acionar o interruptor principal
A próxima questão foi se esse contato direto altera como as proteínas G são ativadas. A equipe usou uma sonda fluorescente que imita GTP e que acende quando uma proteína G troca GDP por GTP, uma medida padrão de ativação. Surpreendentemente, adicionar beta-arrestina 1 não mudou a velocidade nem a extensão dessa troca de nucleotídeo para Gαs ou Gαi1. Em outras palavras, a beta-arrestina 1 não age como uma clássica enzima “liga” para as proteínas G. Em vez disso, sua influência aparece em sua própria estrutura. Usando uma beta-arrestina 1 engenheirada cuja movimentação da cauda podia ser rastreada por fluorescência, eles descobriram que Gαs ativo, mas não Gαi1, favorece a liberação da cauda C-terminal da beta-arrestina quando um peptídeo derivado do receptor está presente. Em células vivas, imagens adicionais e sensores de transferência de energia confirmaram que Gαs e beta-arrestina 1 se aproximam após a estimulação hormonal e que Gαs ajuda a empurrar a beta-arrestina 1 para uma conformação mais ativa. 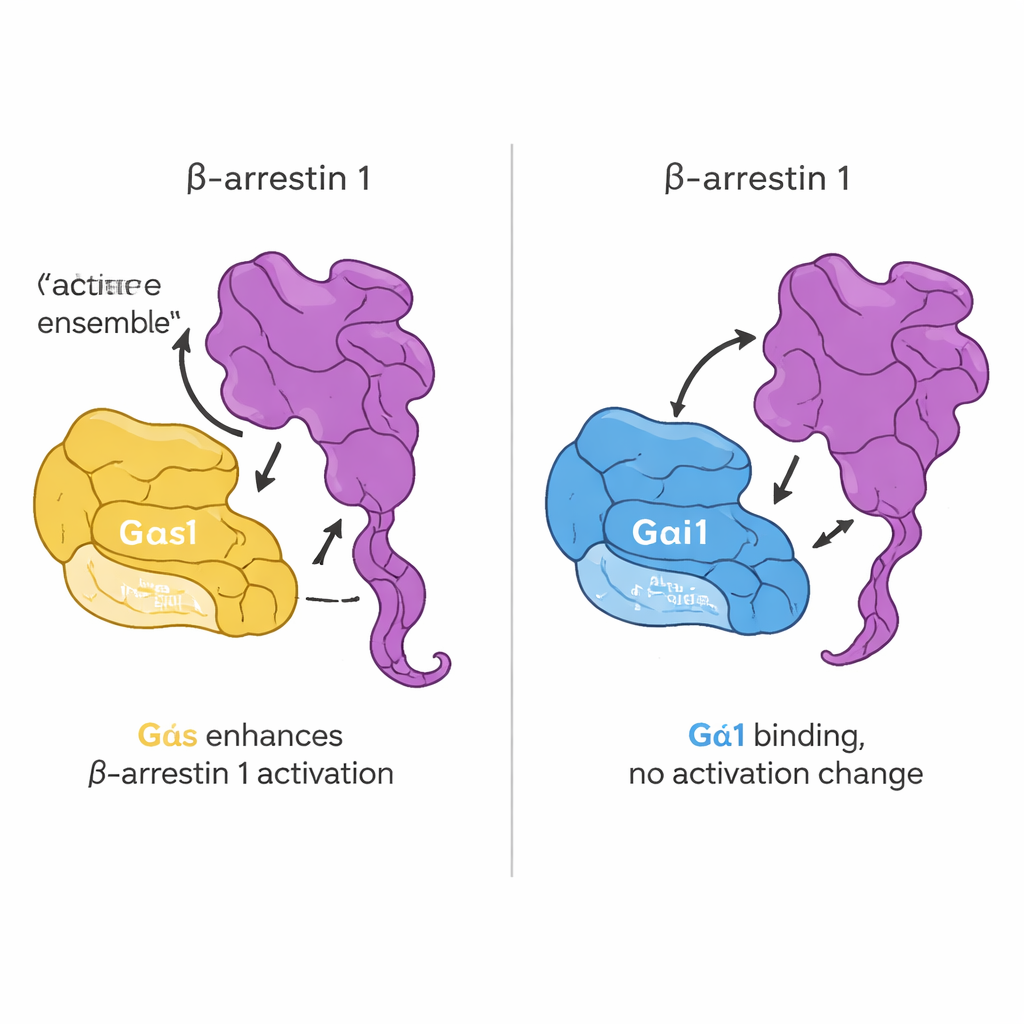
Uma nova camada de controle na sinalização celular
Reunindo esses resultados, o estudo propõe que Gαs e Gαi1 se ligam diretamente à beta-arrestina 1, mas de maneiras ligeiramente diferentes e com consequências distintas. Nenhuma das proteínas G tem seu comportamento principal de “liga/desliga” alterado por esse contato. Em vez disso, especialmente no caso de Gαs, a interação funciona mais como um botão de ajuste fino na beta-arrestina 1, empurrando-a ou estabilizando-a em uma forma mais ativa, com cauda liberada. Isso adiciona uma camada antes pouco apreciada à sinalização por GPCRs: não apenas os receptores podem coordenar proteínas G e beta-arrestinas, mas proteínas G e beta-arrestinas também podem se modular diretamente. A longo prazo, mapear essas interações sutis pode ajudar projetistas de medicamentos a direcionar a sinalização por rotas benéficas — reforçando vias úteis enquanto evitam aquelas que causam efeitos colaterais.
Citação: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Palavras-chave: Receptores acoplados à proteína G, beta-arrestina, sinalização por proteínas G, mecanismos de sinalização celular, biologia estrutural