Clear Sky Science · pt
Análise epigenômica identifica metilação do DNA como mediadora do risco cardiometabólico associado ao tratamento em sobreviventes de câncer infantil
Por que os efeitos pós‑câncer persistem no corpo
Graças a tratamentos melhores, a maioria das crianças com câncer hoje chega à vida adulta. Mas muitos desses sobreviventes enfrentam novos problemas de saúde décadas depois, incluindo obesidade, hipertensão e condições semelhantes ao diabetes. Este estudo investiga uma questão urgente: como tratamentos administrados na infância deixam sombras tão duradouras sobre o coração e o metabolismo? Ao examinar marcas químicas no DNA das células sanguíneas, os pesquisadores revelam pistas de que quimioterapia e radiação passadas podem “reprogramar” o organismo de maneiras que aumentam o risco cardiometabólico a longo prazo.
Rastreando riscos ocultos em sobreviventes adultos de câncer infantil
A equipe estudou quase 3.000 adultos que sobreviveram ao câncer infantil e são acompanhados na coorte de longo prazo St. Jude Lifetime Cohort. Esses sobreviventes haviam sido tratados na infância com várias quimioterapias e com radiação no cérebro ou na região do tronco (tórax, abdome, pelve) e retornaram anos depois para exames de saúde detalhados e testes de sangue. Os cientistas se concentraram em cinco problemas cardiometabólicos chave, conhecidos por aumentar o risco de doença cardíaca e morte prematura: obesidade, glicemia alterada, triglicerídeos elevados, colesterol alto e hipertensão. Comparando sobreviventes com e sem essas condições, eles buscaram milhões de pontos pelo genoma para diferenças na metilação do DNA — pequenos interruptores químicos que ajudam a controlar como os genes são ativados ou silenciados.
Marcas químicas no DNA como memória do tratamento
Ao longo do genoma, os pesquisadores encontraram quase 1.900 sítios de DNA onde os níveis de metilação se associavam a pelo menos uma das cinco condições cardiometabólicas. A maioria desses sítios estava ligada a um único problema, mas um pequeno grupo parecia funcionar como “hubs” conectados a vários. Cinco sítios-chave, localizados próximos a dois genes chamados CPT1A e LMNA, associaram‑se a todos os cinco riscos cardiometabólicos simultaneamente. Esses genes são conhecidos por influenciar como o organismo metaboliza gorduras e como as células mantêm sua estrutura, sugerindo que o tratamento pode perturbar vias metabólicas e cardiovasculares compartilhadas. Muitas das alterações de metilação coincidiram com sinais previamente observados na população geral, especialmente os relacionados à inflamação, mas outras pareceram exclusivas de sobreviventes de câncer — o que sugere que o tratamento deixa uma impressão biológica distintiva.
Ligando terapia, alterações no DNA e doença
O próximo passo foi testar se essas alterações de metilação ajudam realmente a explicar como o tratamento conduz à doença posterior, em vez de serem apenas marcadores associados. Os pesquisadores focaram em problemas cardiometabólicos novos ou que pioraram apenas após a coleta da amostra de sangue, preservando a sequência temporal do tratamento para a mudança no DNA e depois para a doença. Usando análises estatísticas de mediação, identificaram 24 sítios de metilação que, em conjunto, explicavam até cerca de um quarto da relação entre tratamentos específicos e problemas cardiometabólicos posteriores. A radiação no cérebro e no tronco mostrou padrões especialmente fortes: conjuntos de sítios de metilação juntos responderam por aproximadamente 10–20% do impacto dessas radioterapias sobre a glicemia alterada. Um sítio de destaque, próximo a um gene chamado ANTXR2, pareceu mediar cerca de 20% do efeito da radiação do tronco em problemas glicêmicos posteriores.
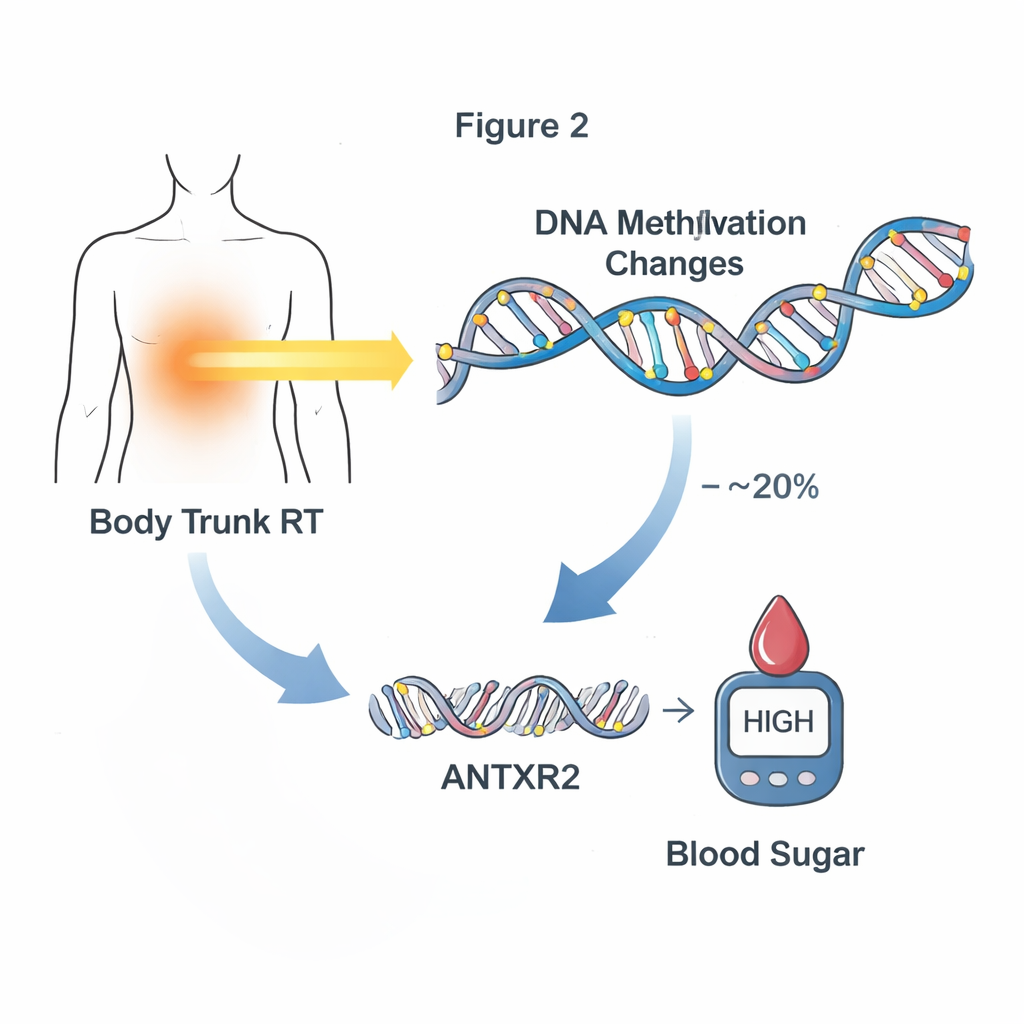
Das marcas no DNA à atividade gênica
Para entender como essas marcas de metilação podem alterar a biologia, a equipe examinou a atividade gênica em um subconjunto de sobreviventes com dados de DNA e RNA do sangue. Eles encontraram dezenas de sítios de metilação onde níveis maiores ou menores de metilação se associavam a alterações na expressão de genes próximos. Entre eles estava o sítio mediador chave próximo a ANTXR2, onde os níveis de metilação se correlacionaram fortemente com a quantidade de expressão desse gene, especialmente em sobreviventes que receberam radiação no tronco. ANTXR2 ajuda a regular vasos sanguíneos e a estrutura do tecido circundante — sistemas que influenciam como glicose e insulina circulam pelo corpo. Esse padrão sugere uma cadeia de eventos em que a radiação altera a metilação, o que modifica a atividade gênica, que por sua vez pode predispor o organismo a uma glicemia anormal.
O que isso significa para sobreviventes e cuidados futuros
Para não especialistas, a mensagem principal é que os tratamentos do câncer infantil não apenas lesionam tecidos no momento; eles também podem deixar “anotações” duradouras no DNA que moldam a saúde por décadas. Neste estudo, algumas dessas anotações — alterações na metilação do DNA — ajudam a explicar por que determinados sobreviventes têm maior probabilidade de desenvolver obesidade, dislipidemia ou problemas glicêmicos relacionados ao diabetes e às doenças cardíacas. Embora essas marcas químicas representem apenas parte da história, elas poderão, no futuro, servir como biomarcadores sanguíneos para identificar sobreviventes em maior risco e para testar se mudanças no estilo de vida ou novas terapias podem reescrever com segurança parte dessa história epigenética. O trabalho aproxima o cuidado de sobrevivência da medicina de precisão: usar pegadas moleculares do tratamento passado para orientar prevenção mais precoce e personalizada de doenças cardíacas e metabólicas.
Citação: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Palavras-chave: sobreviventes de câncer infantil, metilação do DNA, risco cardiometabólico, radioterapia, epigenética