Clear Sky Science · pt
Determinação cotranslacional de estruturas quaternárias em fábricas de chaperonas
Como as “linhas de montagem” celulares mantêm grandes máquinas em ordem
Dentro de cada uma de nossas células, milhares de peças proteicas precisam se encaixar em complexas máquinas moleculares, desde os motores que copiam o DNA até as fábricas que constroem outros RNAs. Este estudo faz uma pergunta aparentemente simples, com grandes implicações: como as células decidem, em tempo real, quais proteínas auxiliares acompanharão cada nova peça enquanto ela está sendo construída, e como mantêm esse processo organizado no fluido caótico da célula?
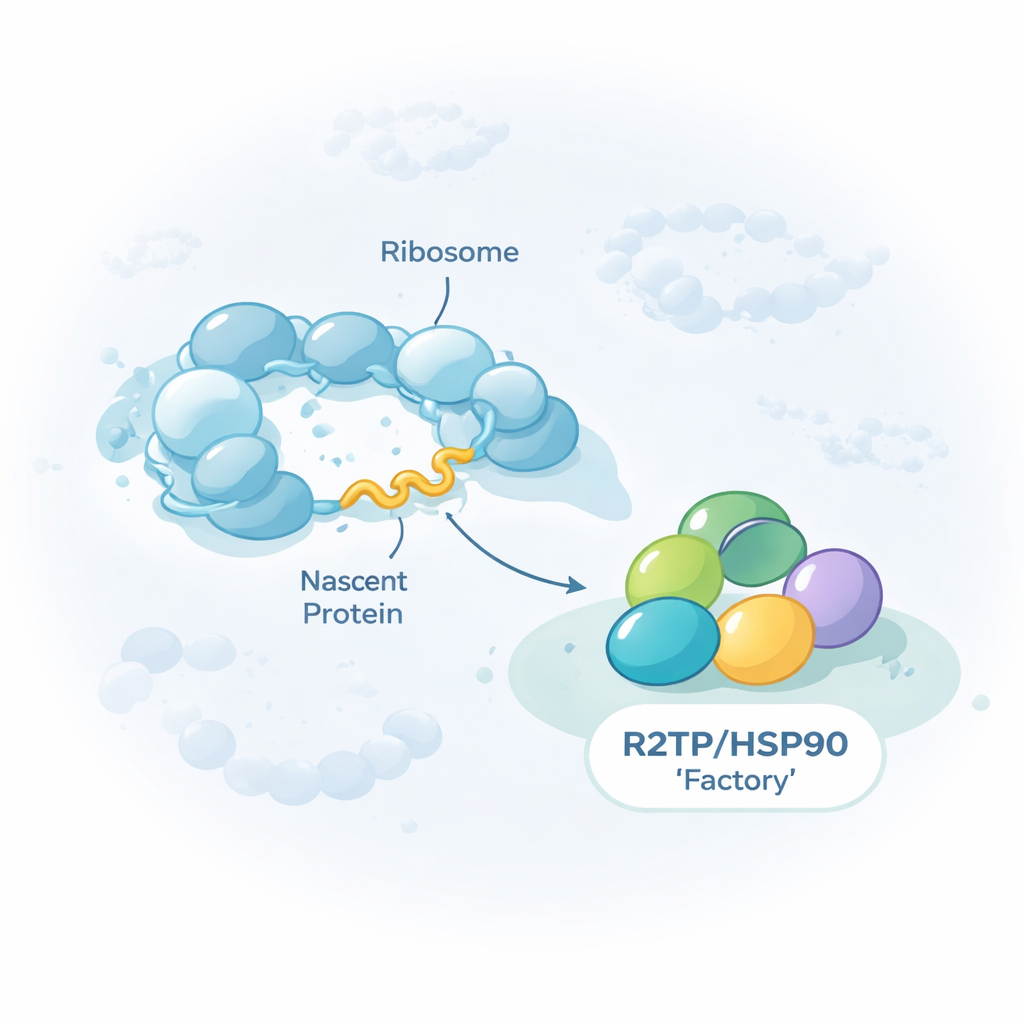
Um ajudante de uso geral para mega-máquinas celulares
O trabalho foca em um grupo de proteínas auxiliares, ou chaperonas, conhecidas como HSP90/R2TP. Em vez de dobrar proteínas individuais, essa chaperona se especializa em montar complexos gigantes de múltiplas partes, incluindo as três RNA polimerases nucleares que transcrevem DNA em RNA, certos grânulos ribonucleoproteicos e grandes máquinas de remodelamento que reorganizam a embalagem do DNA. Os autores mostram que a R2TP não encontra esses clientes apenas depois que estão prontos. Em vez disso, frequentemente se associa enquanto cada cliente ainda está sendo fabricado nos ribossomos, as máquinas de fazer proteína da célula. Ao purificar R2TP de células humanas e sequenciar os RNAs que vinham com ela, encontraram cerca de 150 RNAs mensageiros cujas proteínas codificadas são contatadas pela R2TP durante sua própria tradução.
Auxiliares que acompanham cadeias proteicas em crescimento
Para testar se essa ligação realmente ocorre durante a síntese proteica, a equipe usou drogas que congelam ou perturbam a tradução. Quando empregaram compostos que arrancam as cadeias proteicas em crescimento dos ribossomos, a maioria dos RNAs mensageiros desapareceu do alcance da R2TP. Mas quando usaram um fármaco que apenas pausa os ribossomos e mantém as cadeias nascente atreladas, a ligação da R2TP aumentou. RNAs repórteres geneticamente modificados confirmaram isso: se a tradução fosse interrompida artificialmente cedo, a chaperona deixava de se ligar à mensagem. Em conjunto, esses resultados apontam para uma regra clara de engajamento: a R2TP reconhece seus clientes principalmente através da cadeia proteica emergente que sai do ribossomo, e não por meio da sequência do RNA em si.
“Fábricas” construídas por chaperonas que agrupam mensagens específicas
Usando imagem de molécula única avançada, os autores fizeram então uma descoberta surpreendente. Em vez de ver muitas mensagens de clientes diferentes espalhadas aleatoriamente, observaram que algumas mensagens-chave — especialmente as que codificam subunidades principais da RNA polimerase II e um grande fator de splicing chamado PRPF8 — frequentemente se reuniam em focos brilhantes no citoplasma. Esses focos eram enriquecidos em R2TP e seu parceiro HSP90, bem como em componentes ribossomais e nas próprias proteínas em fabricação, mostrando que são sítios ativos de tradução. Quando a tradução ou a atividade ATPase exigente de energia da R2TP ou da HSP90 foi bloqueada, esses focos se dissolveram. Os autores chamam essas estruturas de “fábricas R2TP”: condensados especializados onde mensageiros selecionados e chaperonas se concentram para favorecer o contato oportuno e protetor entre as cadeias proteicas emergentes e seus ajudantes de montagem.
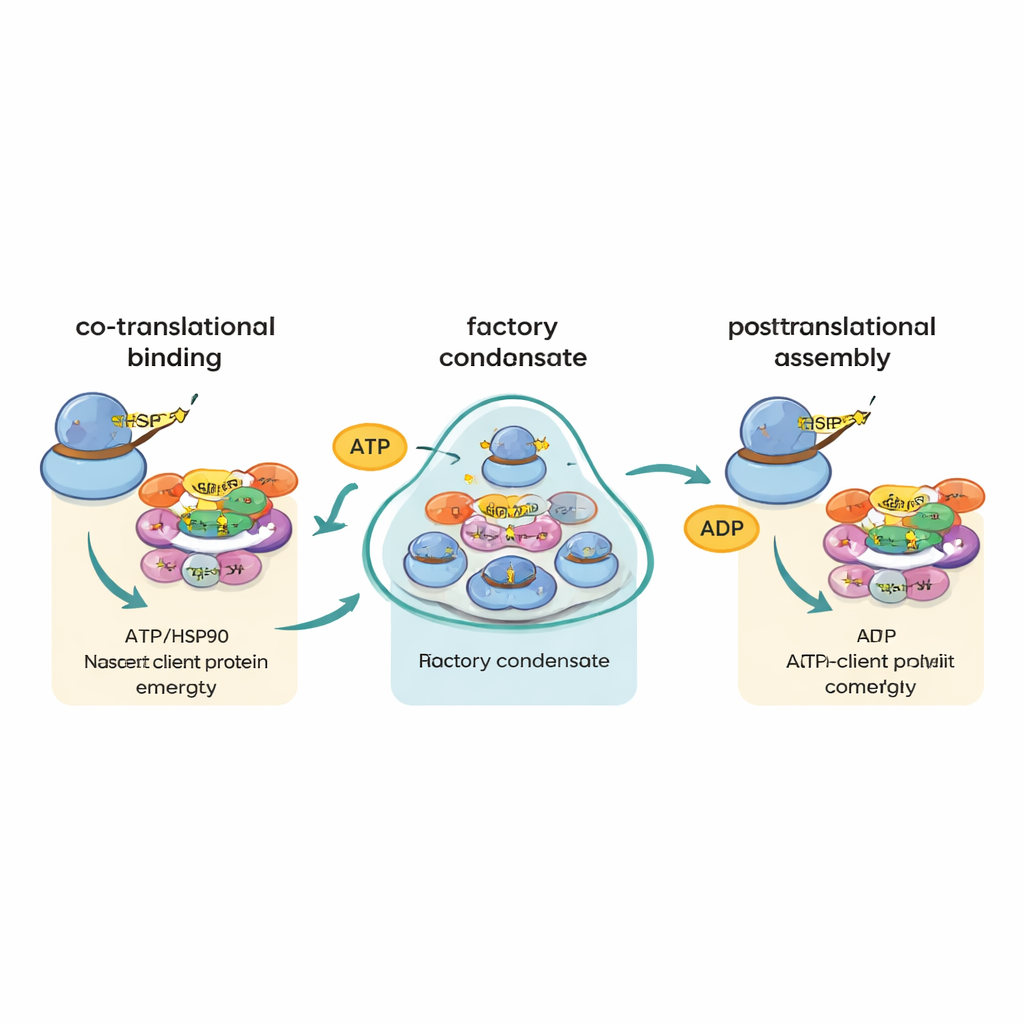
Roteando peças sem combinar seus projetos
Uma ideia anterior era que mensagens que codificam diferentes partes de um mesmo complexo poderiam se encontrar e ser traduzidas lado a lado, permitindo que seus produtos proteicos se montassem imediatamente. O novo trabalho em grande parte descarta esse modelo de “projeto colocalizado”. Mesmo para pares de proteínas conhecidos por se unirem na mesma máquina, seus RNAs mensageiros raramente apareciam juntos. Em vez disso, os dados sustentam uma estratégia diferente que os autores denominam “canalização cotranslacional por chaperonas”, ou “cha-cha”. Nesse esquema, à medida que cada proteína grande ou propensa a montagem começa a emergir do ribossomo, R2TP e HSP90 prendem-se e determinam seu destino, guiando-a por passos posteriores da montagem. As próprias fábricas não reúnem principalmente mensagens correspondentes; em vez disso, aumentam as chances de que proteínas novas e vulneráveis encontrem prontamente a chaperona certa.
Por que essa organização oculta importa para a saúde e a doença
Ao revelar que R2TP e HSP90 não apenas protegem peças proteicas frágeis, mas também moldam onde e como elas são traduzidas, este estudo expõe uma camada inesperada de organização intracelular. O mecanismo cha-cha ajuda a explicar como as células montam de forma confiável complexos moleculares enormes, mesmo que as mensagens para suas partes raramente compartilhem o mesmo endereço. Também sugere por que defeitos em chaperonas ou em seus ciclos energéticos podem desestabilizar máquinas vitais como RNA polimerase e fatores de splicing, com consequências que vão de distúrbios do desenvolvimento ao câncer. Em essência, o trabalho mostra que as células dependem de “fábricas” dinâmicas de chaperonas para direcionar peças recém-fabricadas às montagens corretas, mantendo suas máquinas internas eficientes e organizadas.
Citação: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Palavras-chave: chaperonas de proteína, montagem cotranslacional, máquinas moleculares, RNA polimerase, controle de qualidade celular