Clear Sky Science · pt
ProteoAutoNet: análise de proteínas co-eluidas em alto rendimento com robótica e aprendizado de máquina
Por que entender parcerias entre proteínas importa
Dentro de cada célula, proteínas raramente atuam sozinhas. Elas se unem em alianças dinâmicas para montar estruturas, copiar DNA, destruir partes danificadas e alimentar o crescimento. Muitos cânceres sequestram essas parcerias, mas mapear essas relações em detalhes tem sido um trabalho lento e minucioso. Este estudo apresenta o ProteoAutoNet, um sistema alimentado por robótica e aprendizado de máquina que acelera muito a forma como cientistas descobrem parcerias de proteínas nas células, e mostra como essa abordagem pode revelar pontos fracos ocultos em cânceres de tireoide.
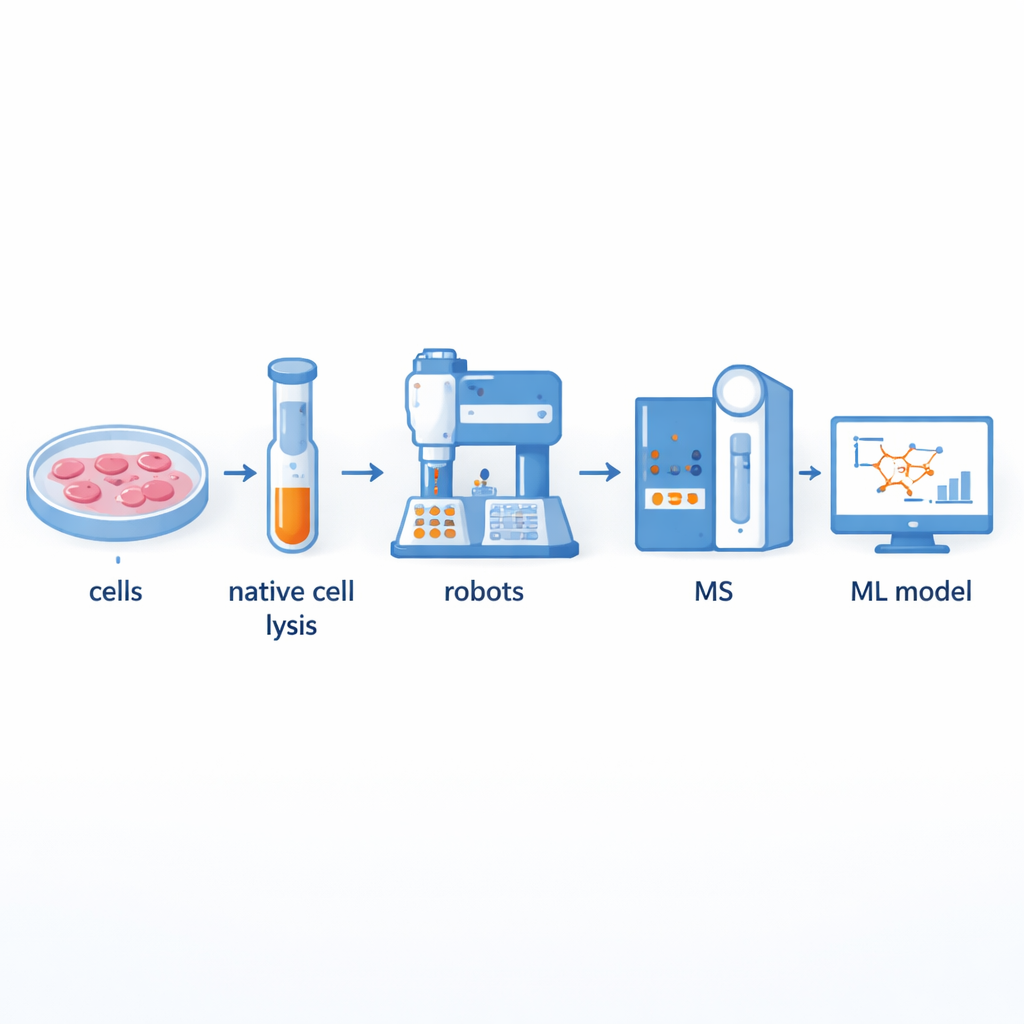
Construindo uma fábrica mais rápida de parcerias proteicas
Tradicionalmente, os cientistas usam um método chamado espectrometria de massas por co-fração para separar grandes complexos proteicos e então identificar seus componentes. Embora poderoso, esse método é trabalhoso e de baixa vazão: preparar centenas de frações à mão pode levar muitos dias. Os autores construíram uma plataforma assistida por robótica que automatiza a maior parte desse fluxo de trabalho. O conteúdo celular é primeiro cuidadosamente liberado para que complexos proteicos naturais permaneçam intactos, e então passado por colunas de separação por tamanho para dividi-lo em dezenas de frações. Robôs de manuseio de líquidos e braços robóticos passam a executar o restante, adicionando reagentes, digerindo proteínas em fragmentos menores, limpando as amostras e entregando-as a um espectrômetro de massas para medição. Essa configuração pode processar até 540 frações de múltiplas linhas celulares de tireoide em apenas dois a três dias, dobrando aproximadamente a vazão em comparação com sistemas semi-automatizados anteriores.
Robôs que não são apenas mais rápidos, mas mais confiáveis
A velocidade sozinha não basta se os resultados forem ruidosos ou inconsistentes. A equipe verificou cuidadosamente se o fluxo robótico equiparava ou superava a qualidade do processamento manual tradicional. Usando amostras de controle de qualidade, eles mostraram que o sistema automatizado identificou repetidamente quase 3.000 proteínas por linha celular de tireoide, com grande sobreposição entre réplicas e forte concordância nas quantidades de proteínas medidas. Quando compararam diretamente o processamento robótico e manual das mesmas amostras, ambas as abordagens detectaram números semelhantes de proteínas, mas o método robótico produziu variação ligeiramente menor nas contagens e medidas de abundância de proteínas mais estáveis. Isso significa que a nova plataforma não só economiza tempo e mão de obra, como também sustenta experimentos mais reprodutíveis — um requisito crucial para estudos de grande escala e aplicações clínicas.
Ensinando computadores a reconhecer conexões significativas
Mesmo com instrumentos rápidos, um desafio central permanece: decidir quais proteínas realmente interagem e quais apenas aparecem juntas por acaso. Para enfrentar isso, os autores combinaram bases de dados curadas de complexos proteicos com um modelo de aprendizado de máquina baseado no algoritmo XGBoost. Primeiro limparam e mesclaram três recursos principais de complexos proteicos, resultando em 96.635 interações proteína–proteína conhecidas. Em seguida, usaram perfis de como as proteínas apareciam nas frações como características de entrada e rotularam pares como prováveis parceiros ou não-parceiros com base nas bases de dados. Como parcerias reais e de alta confiança são relativamente raras, empregaram uma estratégia direcionada de aumento de dados: criaram muitas versões ligeiramente perturbadas de exemplos positivos conhecidos para ensinar ao modelo a reconhecer padrões robustos em vez de memorizar assinaturas específicas. Treinado em dezenas de milhões de exemplos desse tipo de três linhas celulares de tireoide, o modelo alcançou desempenho forte, classificando corretamente interações verdadeiras bem acima do acaso tanto em testes internos quanto em uma linha celular de validação independente.
Novas visões sobre a maquinaria das células cancerosas
Com esse fluxo de trabalho, os pesquisadores mapearam redes de interação em uma linha celular de tireoide normal e em duas cancerosas: uma linhagem de carcinoma papilífero da tireoide e uma de carcinoma folicular capaz de se espalhar para os pulmões. Nesses tecidos, identificaram mais de 25.000 interações proteicas prováveis e encontraram sinais fortes de máquinas celulares bem conhecidas, como ribossomos (que construem proteínas) e proteassomas (que as degradam), confirmando que o método recupera biologia estabelecida. Ao comparar as células cancerosas com a linha normal, descobriram redes que estavam amplificadas na doença. Nas células do carcinoma folicular metastático, componentes do proteassoma e um complexo chaperona chamado prefoldina estavam marcadamente mais conectados e abundantes. Várias subunidades da prefoldina já haviam sido associadas a outros cânceres, mas levantamentos proteômicos globais haviam perdido seu comportamento coordenado no câncer de tireoide, possivelmente porque essas proteínas são rigidamente reguladas por degradação. A abordagem de co-fração expôs suas mudanças coordenadas ao nível do complexo.
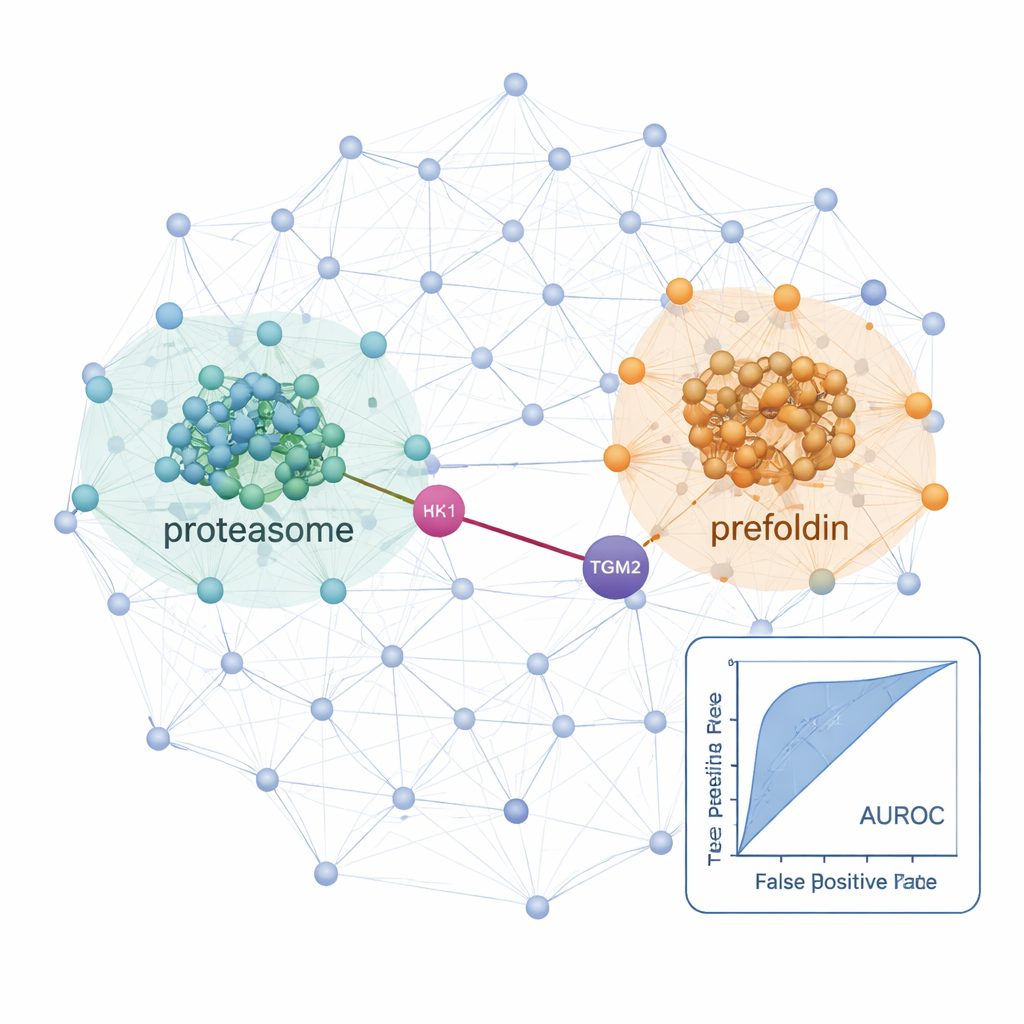
Conexões ocultas que podem orientar tratamentos futuros
O estudo também destacou interações específicas que podem influenciar como os cânceres de tireoide crescem e se disseminam. Um exemplo é uma parceria prevista entre HK1, uma enzima que inicia a principal via de queima de açúcar da célula, e TGM2, uma proteína conhecida por favorecer invasão e metástase em tumores de tireoide. Essa conexão HK1–TGM2, ausente das bases de dados de interação existentes, foi apoiada por modelagem estrutural e apareceu particularmente ativa na linha de carcinoma papilífero, sugerindo que reprogramação metabólica e comportamento invasivo podem estar ligados fisicamente. Em conjunto, o ProteoAutoNet demonstra como combinar robótica e aprendizado de máquina pode transformar o mapeamento das redes proteicas — antes lento e restrito a especialistas — em um processo mais escalável. Para leitores não especializados, a mensagem principal é que essa tecnologia pode revelar tanto mudanças amplas na maquinaria celular quanto parcerias proteicas inesperadas que, um dia, podem ajudar médicos a prever melhor quais cânceres de tireoide serão agressivos e sugerir novos alvos terapêuticos.
Citação: Lyu, M., Hu, P., Zhang, G. et al. ProteoAutoNet: high-throughput co-eluted protein analysis with robotics and machine learning. Nat Commun 17, 1949 (2026). https://doi.org/10.1038/s41467-026-68686-9
Palavras-chave: interações proteicas, espectrometria de massas, aprendizado de máquina na biologia, câncer de tireoide, proteassoma e prefoldina