Clear Sky Science · pt
Destruição diferencial de lipídios de membrana por antibióticos lipopeptídicos, colistina e turnercyclamicinas
Por que isso importa para antibióticos futuros
Infecções resistentes a medicamentos estão projetadas para matar dezenas de milhões de pessoas a cada ano até meados do século, e alguns dos culpados mais letais são bactérias Gram-negativas que já resistem a muitos antibióticos. A colistina é um dos poucos medicamentos remanescentes que ainda pode tratar essas infecções, mas é agressiva para os pacientes e as bactérias estão cada vez mais aprendendo a evitá-la. Este estudo dissecou como a colistina atua em comparação com uma nova família de antibióticos naturais chamada turnercyclamicinas, revelando que pequenos ajustes químicos podem produzir modos muito diferentes de matar bactérias — e, potencialmente, medicamentos mais seguros.
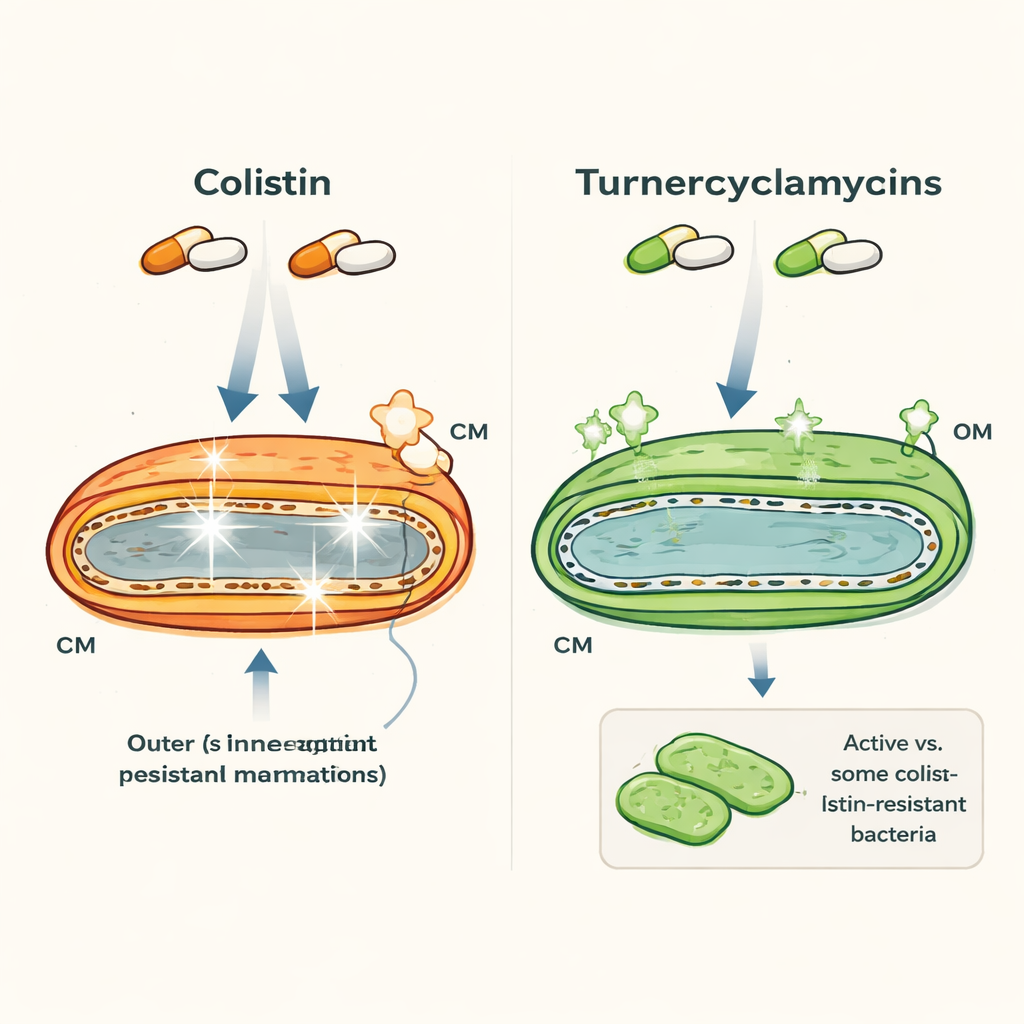
Dois medicamentos com aparência semelhante e comportamento muito diferente
Colistina e turnercyclamicinas são ambos lipopeptídeos — moléculas que combinam uma cauda gordurosa com um anel peptídico — e ambos têm como alvo bactérias Gram-negativas como Escherichia coli e Acinetobacter. À primeira vista parecem semelhantes, mas suas propriedades divergem nitidamente. A colistina é um fármaco de último recurso que age rapidamente, mas pode danificar rins e nervos humanos, e as bactérias transportam cada vez mais genes de resistência como mcr-1. As turnercyclamicinas, descobertas em bactérias associadas a teredos (shipworms), podem matar muitos dos mesmos patógenos, incluindo algumas cepas resistentes à colistina, mas mostram muito menos toxicidade em testes laboratoriais. Intrigantemente, duas versões que diferem apenas por uma pequena extensão da cauda gordurosa já exibem padrões de resistência distintos, sugerindo que recursos estruturais muito sutis são importantes.
Como a colistina faz buracos e as turnercyclamicinas agem mais lentamente
Os autores usaram corantes fluorescentes, experimentos de contagem de morte ao longo do tempo e microscopia eletrônica para observar como esses fármacos afetam as membranas bacterianas ao longo do tempo. A colistina torna rapidamente tanto a membrana externa quanto a membrana citoplasmática interna permeáveis, levando à morte celular rápida em poucas horas. As turnercyclamicinas, em contraste, matam mais lentamente — levando de 6 a 10 horas para eliminar completamente culturas — e perturbam principalmente a membrana externa. Corantes que acendem quando a membrana interna é violada mostraram sinais fortes para a colistina, mas apenas sinais modestos e retardados para as turnercyclamicinas, e imagens de alta resolução confirmaram pouco dano visível à membrana interna mesmo quando as células estavam morrendo. Isso indica que as turnercyclamicinas não matam pelo clássico mecanismo de “formação de poros” usado por muitos antibióticos que atingem membranas.
Blocos de construção lipídicos como botões de controle ocultos
Ambas as famílias de fármacos dependem, em última instância, de um componente bacteriano chamado lipopolissacarídeo (LPS), que é sintetizado na membrana interna e normalmente exportado para a superfície externa. Quando os pesquisadores desativaram etapas iniciais da biossíntese de LPS, tanto a colistina quanto as turnercyclamicinas perderam atividade; mas quando bloquearam a maquinaria de transporte que move o LPS para fora, os fármacos ainda funcionaram. Isso significa que a existência de blocos de construção do LPS é essencial, mas seu destino final não é. Uma diferença chave emergiu quando a ligação foi medida diretamente: a colistina adere ao LPS purificado com afinidade micromolar, enquanto as turnercyclamicinas não mostraram ligação mensurável. Em vez disso, as turnercyclamicinas foram fortemente afetadas por outros lipídios de membrana. Certos fosfolipídios, especialmente a fosfatidilglicerol, podiam atenuar ou modular sua atividade, e os fármacos eram prontamente capturados por vesículas da membrana externa — pequenas bolhas lipídicas liberadas pelas bactérias.
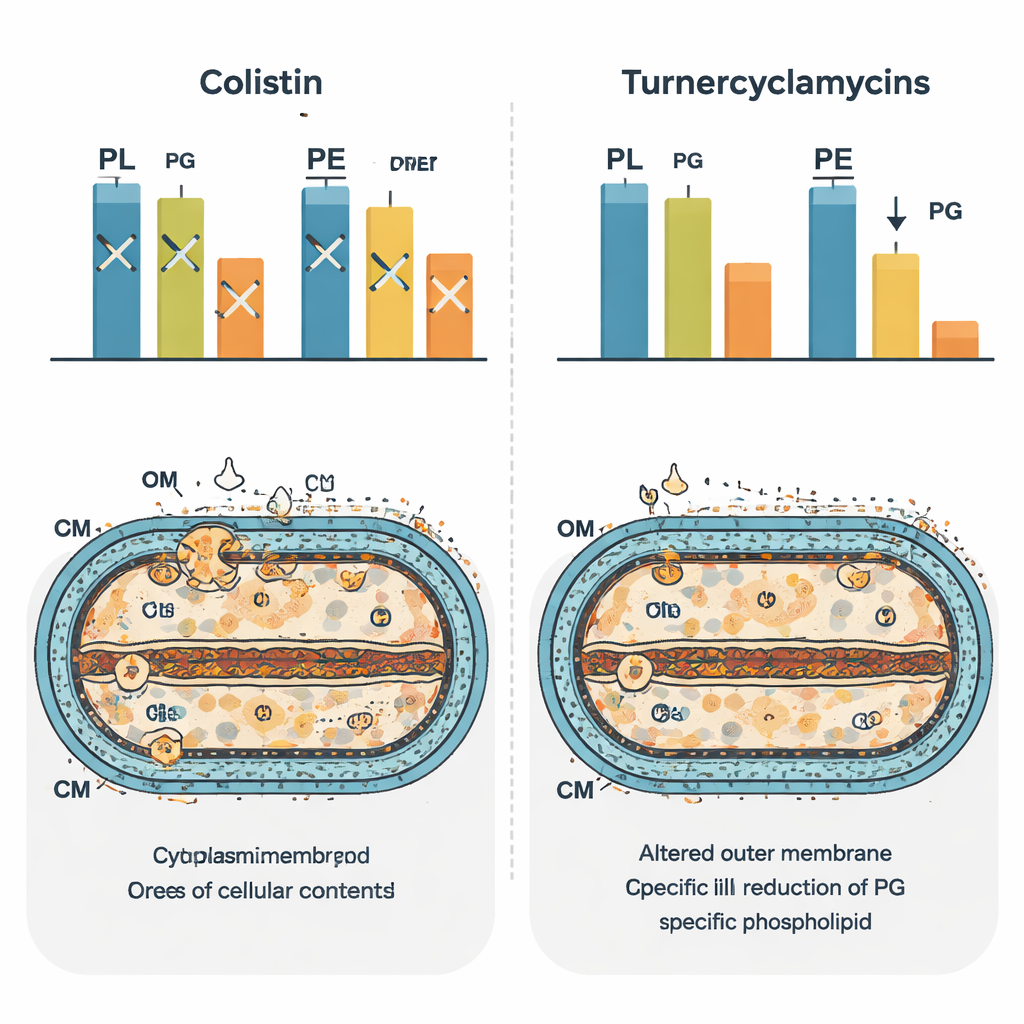
Reprogramando a paisagem lipídica bacteriana
Para ver o impacto mais amplo na célula, a equipe usou “fosfolipidômica” baseada em espectrometria de massa para catalogar centenas de espécies lipídicas após o tratamento. A colistina produziu um padrão distintivo de alterações, refletindo sua ampla perturbação da homeostase da membrana. As turnercyclamicinas geraram uma assinatura diferente que se assemelhava de perto a bactérias que careciam de uma proteína transportadora de lipídios chamada MlaA. Nessas células, certos lipídios diacil foram diminuídos e formas monoacil aumentaram, sugerindo que o ciclo normal e a remodelação de fosfolipídios entre membranas haviam sido desequilibrados. Notavelmente, os níveis de fosfatidilglicerol caíram em células tratadas com turnercyclamicinas, reforçando a ideia de que esse lipídio está diretamente ligado à potência desses compostos. Os autores propõem que as turnercyclamicinas podem agir como miméticas moleculares que emperram vias que ligam a síntese ou o transporte de ácidos graxos, LPS e fosfatidilglicerol.
O que isso significa para projetar fármacos melhores
Em termos simples, o estudo mostra que a colistina mata ao rasgar rapidamente ambas as camadas protetoras de uma bactéria Gram-negativa, ajudada por forte ligação ao LPS, enquanto as turnercyclamicinas agem mais como sabotadores da cadeia de suprimento lipídico da célula. Elas se infiltram na membrana externa, perturbam gradualmente como lipídios específicos são produzidos e reciclados, e acabam fazendo com que o envelope celular falhe — sem bombardear fortemente a membrana interna. Como esse mecanismo mais suave e mais direcionado está ligado a menor toxicidade e a um perfil de resistência diferente, entendê-lo oferece um mapa para a criação de antibióticos lipopeptídicos de próxima geração. Ao ajustar características como o comprimento e a saturação da cauda gordurosa, químicos podem ser capazes de construir fármacos que poupem tecidos humanos, mantenham atividade contra cepas resistentes à colistina e se mantenham um passo à frente na corrida armamentista contra bactérias resistentes a antibióticos.
Citação: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
Palavras-chave: resistência a antibióticos, bactérias Gram-negativas, colistina, antibióticos lipopeptídicos, lipídios de membrana