Clear Sky Science · pt
Base estrutural para as conformações dinâmicas do AP-4 e sua associação com ARF1
Como as células classificam e enviam suas cargas
Toda célula é um armazém movimentado, constantemente classificando e enviando milhares de “pacotes” de proteína para os destinos corretos. Quando esse sistema de entrega falha em células nervosas, o resultado pode ser transtornos graves do cérebro e do movimento. Este estudo desvenda como uma máquina-chave de envio, chamada AP-4, muda de forma e se associa a uma proteína reguladora, ARF1, para carregar a carga em pequenas bolhas de transporte e por que sua flexibilidade é tão importante para neurônios saudáveis.
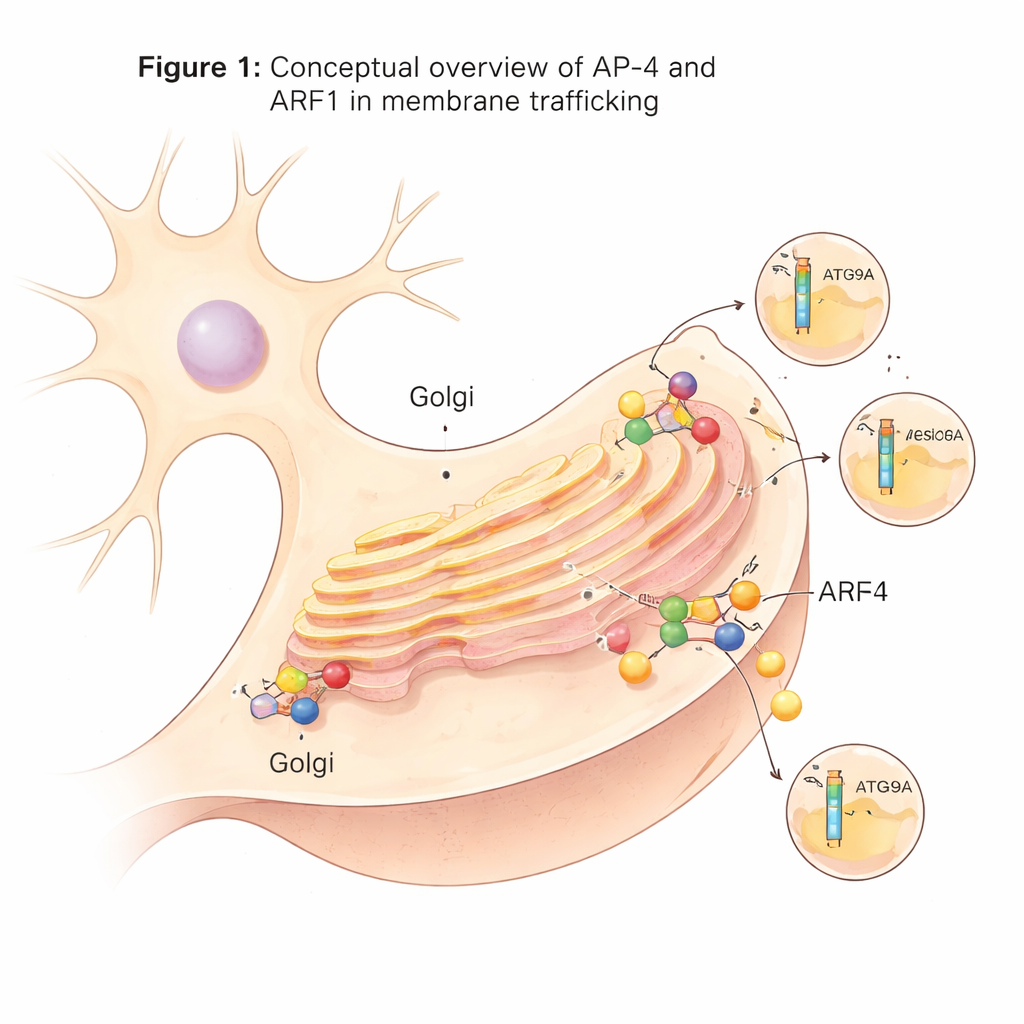
Uma máquina de envio especializada em neurônios
No interior das células, muitas vesículas de transporte brotam de uma estação central de triagem conhecida como rede trans-Golgi. Essas vesículas dependem de complexos de proteínas adaptadoras, ou complexos AP, que atuam como docas de carregamento: reconhecem proteínas cargo e ajudam a formar vesículas revestidas ao redor delas. O AP-4 é um desses adaptadores e é incomum porque, ao contrário de muitos outros, não usa a proteína de andaime comum clatrina. Embora o AP-4 seja produzido em muitos tecidos, ele desempenha um papel especialmente importante em neurônios. Quando o AP-4 está ausente ou defeituoso em humanos, cargas cruciais como a proteína relacionada à autofagia ATG9A e certos receptores de glutamato deixam de se deslocar corretamente, levando a uma condição neurodesenvolvimental grave conhecida como síndrome de deficiência de AP-4.
Um complexo que muda de forma em repouso
Os autores usaram criomicroscopia eletrônica (cryo-EM), um método de imagem poderoso que pode visualizar grandes montagens protéicas, para determinar a estrutura tridimensional do complexo “núcleo” do AP-4 em solução. O AP-4 é composto por quatro subunidades que, juntas, formam uma estrutura em forma de tigela. Descobriram que o AP-4 não permanece em uma única forma rígida. Em vez disso, ele alterna naturalmente entre uma forma “fechada”, na qual uma subunidade (o domínio C-terminal da subunidade média) está dobrada para o centro da tigela, e uma forma “aberta”, na qual essa peça se projeta para fora e se torna altamente flexível. Experimentos adicionais de fluorescência de molécula única mostraram que essa subunidade na verdade amostra pelo menos três posições — fechada, parcialmente aberta e totalmente aberta — revelando que o AP-4 é intrinsecamente dinâmico mesmo antes de se ligar às membranas.
Papel do ARF1: recrutador, não interruptor mestre
Muitos complexos adaptadores relacionados são ativados por mudança conformacional ao se ligarem a pequenas proteínas reguladoras chamadas ARFs. Para entender como isso funciona no AP-4, os pesquisadores resolveram estruturas do AP-4 ligado ao ARF1, uma pequena proteína de ligação a GTP que se ancora às membranas. Eles descobriram que o ARF1 se liga principalmente a uma das grandes subunidades do AP-4 próximo ao seu N-terminal, de maneira semelhante a outros complexos AP. Surpreendentemente, a ligação do ARF1 não desencadeia uma rearranjo estrutural dramático no AP-4. As conformações fechada e aberta continuam a coexistir, e a arquitetura geral do complexo permanece em grande parte inalterada. Testes bioquímicos confirmaram que pontos de contato específicos entre ARF1 e AP-4 são essenciais para o recrutamento à membrana, mas o ARF1 sozinho não fixa o AP-4 em um único estado ativo.
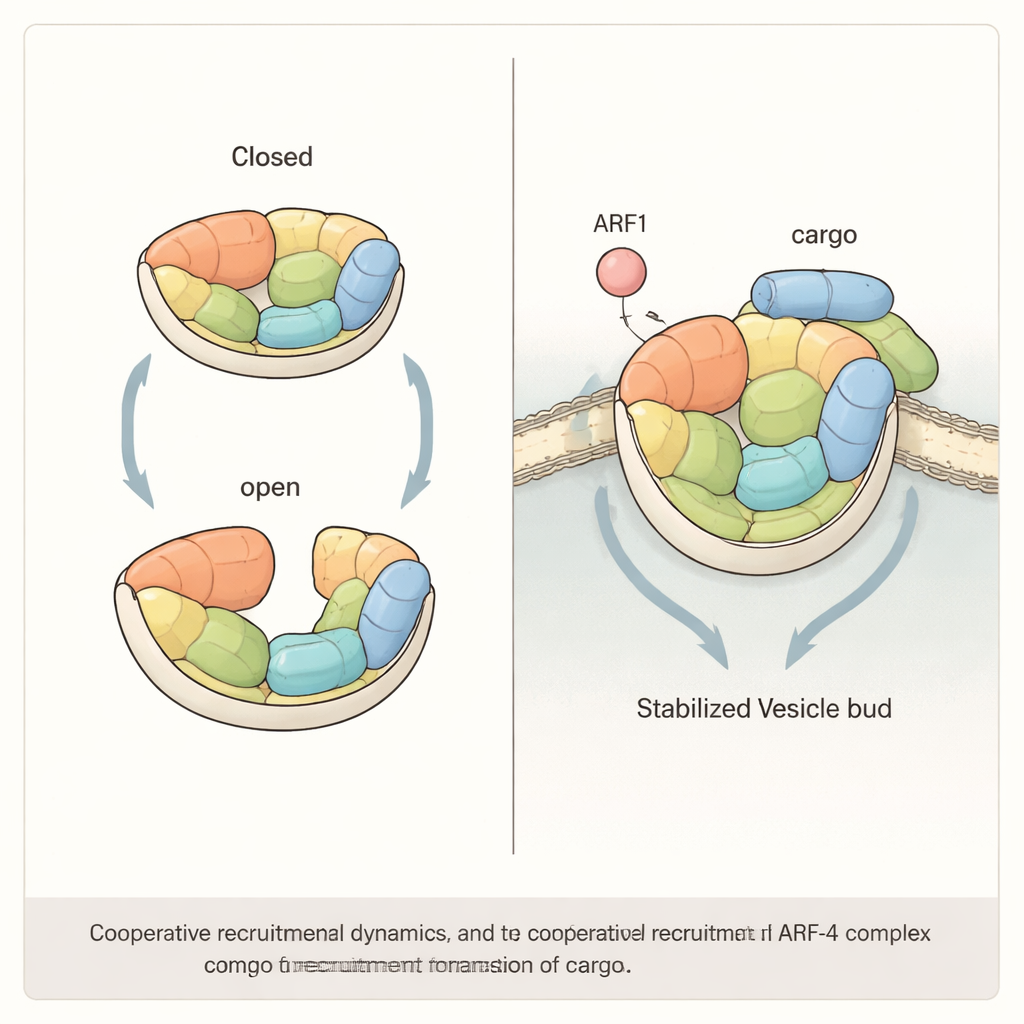
Trabalho em equipe entre regulador e carga
O estudo mostra também que o recrutamento eficiente do AP-4 às membranas provavelmente requer cooperação entre o ARF1 e as próprias proteínas cargo. Ao reconstituir o sistema em esferas artificiais e lipossomas, os autores descobriram que tanto o ARF1 quanto uma cauda curta da carga ATG9A podem atrair o AP-4, mas quando ambos estão presentes simultaneamente, recrutam significativamente mais AP-4 do que o esperado pela soma de seus efeitos individuais. Quando os pesquisadores introduziram mutações que tornaram a estrutura do AP-4 mais rígida — reduzindo sua capacidade de transitar entre os estados aberto e fechado — esse efeito sinérgico foi perdido. Em células humanas sem uma subunidade chave do AP-4, restaurar apenas versões mutantes “rígidas” do complexo não conseguiu resgatar o tráfego normal da ATG9A a partir do Golgi, destacando que a flexibilidade do AP-4 não é apenas uma curiosidade, mas um requisito funcional.
Por que a flexibilidade importa para a saúde cerebral
No conjunto, o trabalho descreve o AP-4 como um adaptador que muda de forma e amostra múltiplas conformações em solução e nas membranas. Em vez de atuar como um interruptor liga-desliga, o ARF1 funciona como um recrutador baseado na membrana que trabalha em conjunto com proteínas cargo para estabilizar o AP-4 em configurações produtivas para a formação de vesículas. Desestabilizar esse equilíbrio — seja enfraquecendo a ligação do ARF1 ou da carga, seja congelando o AP-4 em uma única forma — prejudica a exportação de cargas do Golgi e pode contribuir para doenças do neurodesenvolvimento. Ao revelar a base estrutural do comportamento dinâmico do AP-4, este estudo oferece um quadro para entender os distúrbios relacionados ao AP-4 e sugere possíveis estratégias futuras para restaurar o tráfego adequado em neurônios afetados.
Citação: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Palavras-chave: tráfego de membrana, complexo adaptador AP-4, ARF1, formação de vesículas, distúrbio do neurodesenvolvimento