Clear Sky Science · pt
Células NK ZNF683+ controlam a sensibilidade à quimioterapia em HPSCC avançado ao remodelar o microambiente imune
Por que algumas quimioterapias funcionam melhor em certos cânceres de garganta
Pessoas com câncer hipofaríngeo avançado — um tumor escondido no fundo da garganta — frequentemente enfrentam quimioterapia agressiva com resultados incertos. Alguns tumores encolhem consideravelmente, enquanto outros mal se alteram. Este estudo coloca uma pergunta simples, porém crucial: o que há de diferente dentro dos tumores que respondem bem? Ao analisar células imunes individualmente, os pesquisadores identificam um tipo particular de célula “guardiã” que pode desequilibrar a balança entre sucesso e fracasso do tratamento quimioterápico padrão.
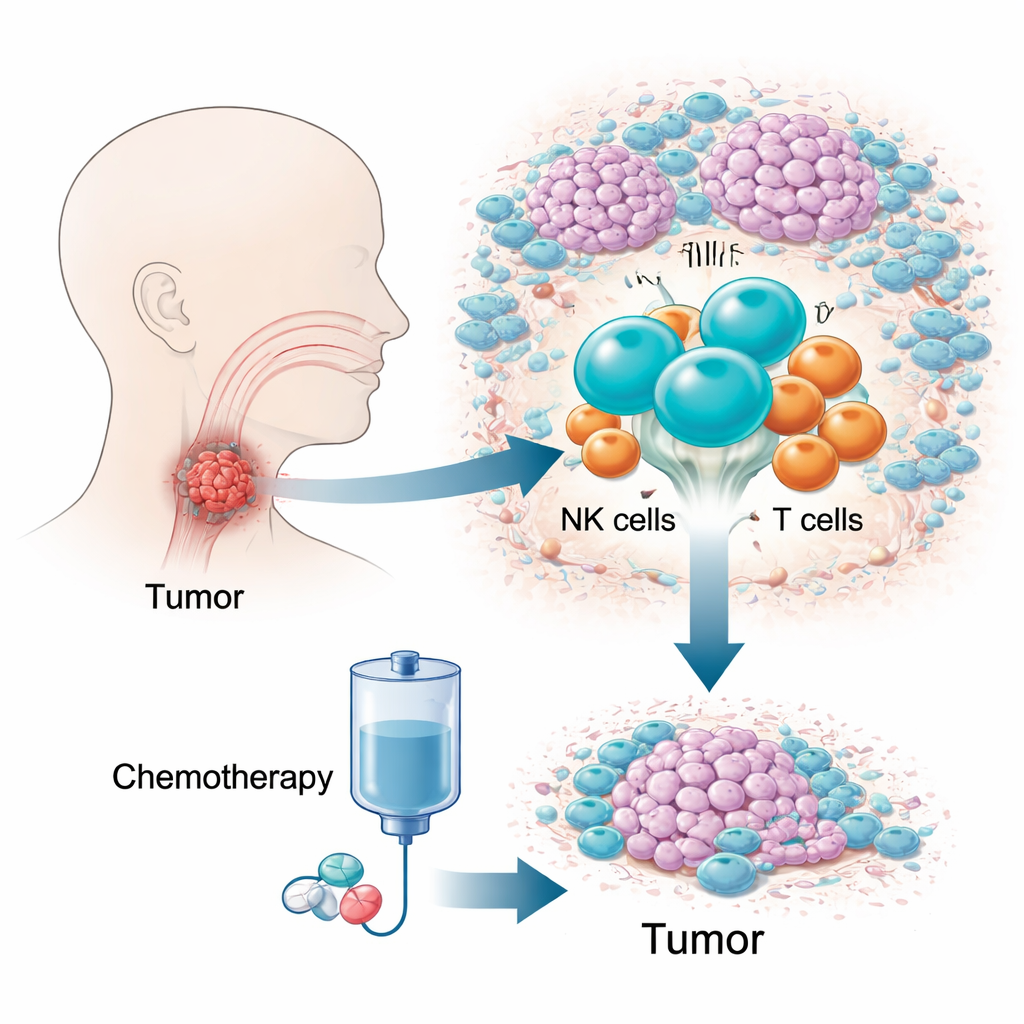
O desafio de um câncer oculto e de difícil tratamento
O carcinoma epidermóide da hipofaringe é um dos tumores de cabeça e pescoço mais letais, em parte porque cresce numa área cramped (apertada) e de difícil exame e causa poucos sintomas nas fases iniciais. Muitos pacientes são diagnosticados tardiamente, quando as opções são limitadas e a sobrevida em cinco anos é baixa. Uma combinação medicamentosa conhecida como quimioterapia TPF é amplamente usada porque pode controlar a doença preservando a laringe. Ainda assim, 10–20% dos pacientes apresentam pouca ou nenhuma resposta, perdendo tempo precioso. Testes genéticos tradicionais, que fazem média dos sinais em milhões de células, têm dificuldades para explicar essa diferença, o que levou os autores a focar no ecossistema vivo de células imunes do tumor.
Lendo a paisagem imune do tumor célula por célula
Os pesquisadores acompanharam 12 pacientes ao longo do tempo, coletando amostras tumorais antes e depois de dois ciclos de quimioterapia TPF e perfilando mais de 150.000 células imunes em resolução de célula única. Também examinaram outros 41 pacientes para confirmar achados-chave usando imagem e citometria de fluxo. Ao mapear a atividade gênica e o tipo celular de cada célula, construíram um atlas detalhado do microambiente tumoral: células T, células B, macrófagos, células dendríticas, mastócitos, neutrófilos e células natural killer (NK). Entre todos esses atores, um padrão se destacou. Antes do tratamento, tumores que depois encolheram tinham muito mais células NK do que aqueles que resistiram à terapia, e quanto maior a fração de NK, maior foi a redução tumoral final.
Um subconjunto especial de NK prepara as células T para o sucesso
Aprofundando-se, a equipe dividiu as células NK em três grupos com base em suas características moleculares. Apenas um desses grupos, marcado pelo fator de transcrição ZNF683 e localizado em grande parte no tecido circundante aos aglomerados tumorais, mostrou forte correlação com boa resposta à quimioterapia. Pacientes cujos tumores apresentavam mais dessas células NK ZNF683+ na linha de base tinham muito mais probabilidade de se beneficiar do TPF. Em experimentos com camundongos, a remoção das células NK praticamente eliminou o benefício da quimioterapia, confirmando que a atividade das NK não é apenas um marcador, mas um requisito para o tratamento eficaz. Curiosamente, essas NK não agiam simplesmente como matadoras diretas do câncer; em vez disso, seus programas gênicos estavam enriquecidos em funções de orientação e ativação das células T.
Como as NK liberam células T potentes que matam o tumor
Para entender quais células T eram mais importantes, os cientistas seguiram clones individuais do receptor de células T antes e depois do tratamento. Eles descobriram que, nos respondedores, um grupo específico de células T CD8 “memória efectora”, enriquecido para uma molécula chamada GZMK, expandiu-se dramaticamente após a quimioterapia. Essas células T produziam altos níveis das citocinas tóxicas TNF e interferon-gama sem apresentar exaustão profunda, tornando-se assassinas potentes e duráveis. Imagens espaciais revelaram que, após o tratamento, essas células CD8 GZMK+ se aglomeravam fortemente em tumores de respondedores, mas não em não-respondedores. Em testes de cocultura com células humanas, o contato direto com NK ZNF683+ impulsionou o crescimento desse subconjunto de CD8 GZMK+, efeito que desaparecia quando as células eram separadas por uma barreira.
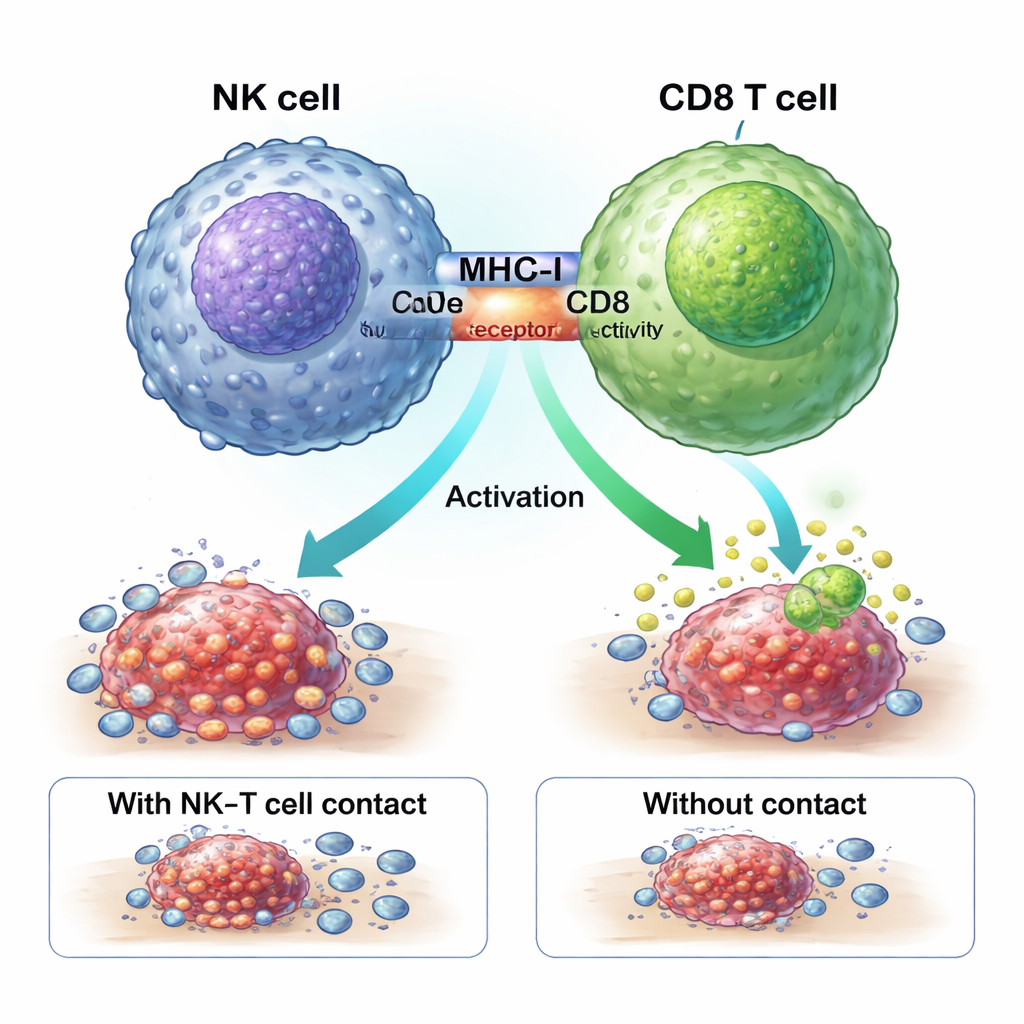
Um aperto de mão físico que ativa os combatentes do tumor
O estudo mostra que as NK ZNF683+ aumentam a resposta à quimioterapia por meio de um “aperto de mão” físico com células T CD8. Moléculas chamadas MHC-I na superfície das NK interagem com receptores CD8 nas células T numa zona de contato próximo, ou sinapse imune. Bloquear MHC-I impediu que as NK gerassem as potentes células CD8 GZMK+. Em camundongos geneticamente modificados para carecer de ZNF683 apenas nas NK, essas células expressaram menos MHC-I e foram muito menos eficazes em ativar células CD8, reforçando a ideia de que ZNF683 programa as NK para se tornarem treinadoras eficazes das células T atacantes, em vez de meras executoras.
O que isso significa para os pacientes
Para leitores leigos, a mensagem-chave é que nem todas as células imunes de um tumor são iguais. Este trabalho identifica um subconjunto específico de NK como um batedor avançado que prepara o campo de batalha antes do início da quimioterapia. Tumores ricos nessas células estão prontos para liberar ondas de fortes células T CD8 quando os medicamentos agem, levando a uma redução tumoral muito maior. Medir a abundância desse eixo NK–T antes do tratamento pode ajudar médicos a prever quem se beneficiará da quimioterapia TPF e quem pode precisar de terapias alternativas ou complementares. No futuro, tratamentos que aumentem ou imitem essas NK ZNF683+ poderiam transformar cânceres hipofaríngeos resistentes em tumores muito mais sensíveis à quimioterapia padrão.
Citação: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
Palavras-chave: câncer do hipofaríngeo, resistência à quimioterapia, células natural killer, microambiente imune tumoral, células T CD8