Clear Sky Science · pt
Fotossíntese de glicina via acoplamento C−N de plástico residual e nitrato sobre catalisador diatômico Pd−B
Transformando Lixo em Blocos de Construção da Vida
Garrafas plásticas, embalagens de alimentos e roupas de poliéster estão por toda parte — e o mesmo vale para os resíduos que deixam. Ao mesmo tempo, muitas indústrias liberam efluentes carregados de nitrato que podem poluir rios e mares. Este estudo mostra como ambos os problemas podem ser abordados simultaneamente: usando a luz do sol e um catalisador especialmente projetado para transformar plástico descartado e nitrato em glicina, um aminoácido simples amplamente usado na alimentação, medicina e agricultura.
Por que a Glicina e os Resíduos Importam
A glicina é um dos blocos básicos das proteínas e é produzida na escala de centenas de milhares de toneladas por ano. Métodos industriais convencionais, especialmente o processo clássico de Strecker, dependem de compostos tóxicos à base de cianeto e de condições de reação severas, o que levanta preocupações de segurança e ambientais. Enquanto isso, a produção global de PET — usado em garrafas, têxteis e embalagens — supera 100 milhões de toneladas anualmente, e mais de 80% acaba em aterros ou no meio ambiente. Quando o PET é degradado quimicamente, um dos produtos é o etilenoglicol, um líquido de baixo valor que é caro de purificar. Os autores fazem uma pergunta simples: em vez de tratar etilenoglicol e nitrato como resíduos, seria possível transformá‑los em matérias‑primas para produzir glicina valiosa usando apenas a luz solar?
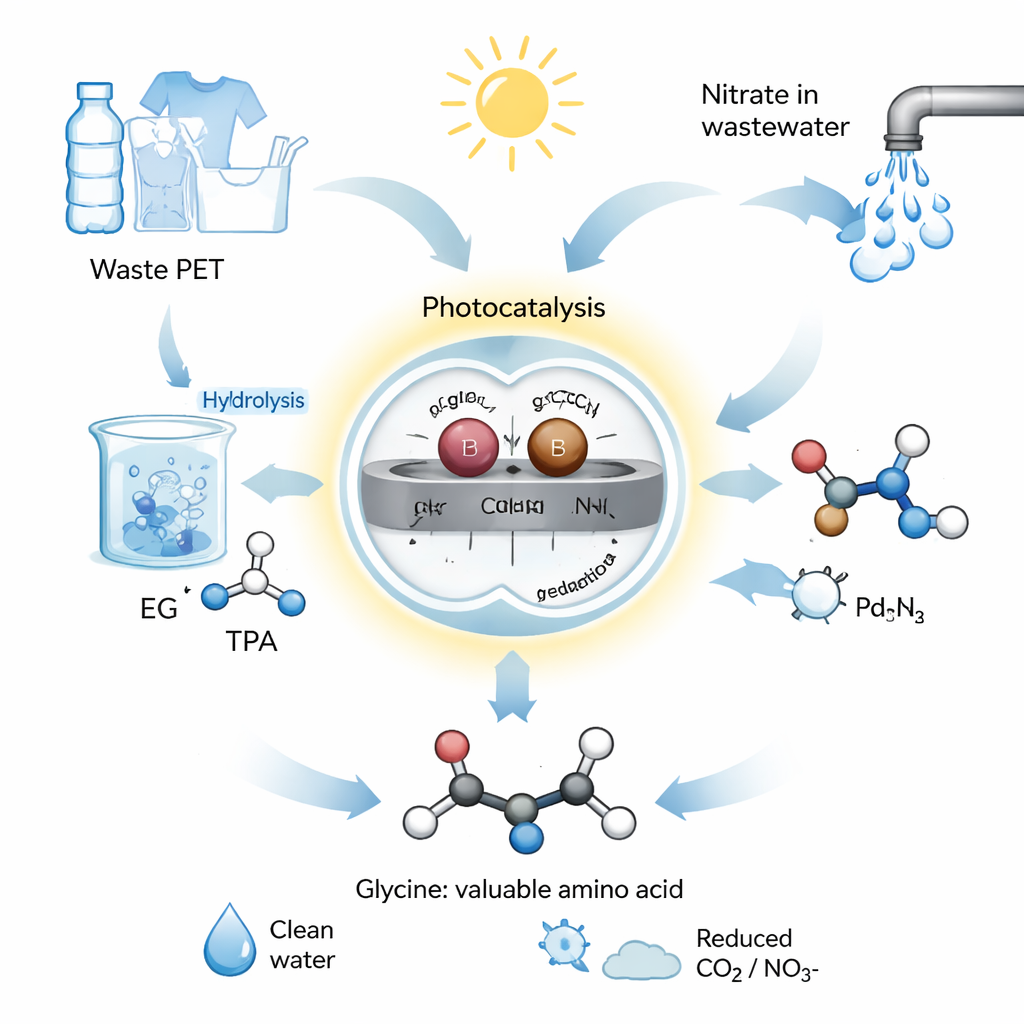
Um Atalho Químico Movido pelo Sol
A equipe projetou um sistema fotocatalítico, ou seja, que utiliza a luz para impulsionar reações químicas. Eles construíram um catalisador a partir de nitreto de carbono grafítico, um semicondutor, e ancoraram pares de átomos individuais de paládio (Pd) e boro (B) em sua superfície. Esses átomos pareados atuam como um time microscópico de duas pessoas, cada uma cuidando de metade da química. No processo deles, o resíduo de PET é primeiro hidrolisado — dividido em água alcalina — liberando etilenoglicol. Esse etilenoglicol e o nitrato proveniente de efluentes são então colocados em água com o catalisador Pd–B e expostos à luz solar simulada ou natural. Sob essas condições brandas, o sistema converte a mistura em glicina com alto rendimento e seletividade superior a 92%, o que significa que muito poucos subprodutos indesejados são formados.
Como a Dupla Atômica Funciona
O sucesso do catalisador depende de como ele gerencia intermediários reacionais de vida curta. Sítios de boro na superfície são “ricos em lacunas” (holes), ou seja, aceitam prontamente carga positiva quando o material absorve luz. Nesses sítios de B, o etilenoglicol é oxidado de forma suave — desprovido de hidrogênio — para formar glicolaldeído, uma molécula instável que normalmente tende a sobreoxidar para ácidos ou até dióxido de carbono. Já os sítios de paládio são “ricos em elétrons”. Eles usam os elétrons gerados pela luz para reduzir o nitrato passo a passo até amônio ou amônia. A etapa-chave é um acoplamento carbono–nitrogênio entre o glicolaldeído e essas espécies nitrogenadas para formar etanolamina, que então é oxidada adicionalmente, novamente principalmente nos sítios de B, para dar glicina. Ao estabilizar o glicolaldeído apenas tempo suficiente para reagir, e ao manter elétrons e lacunas espacialmente separados, o par Pd–B direciona a química para longe de reações laterais desperdiciadoras e em direção ao aminoácido desejado.
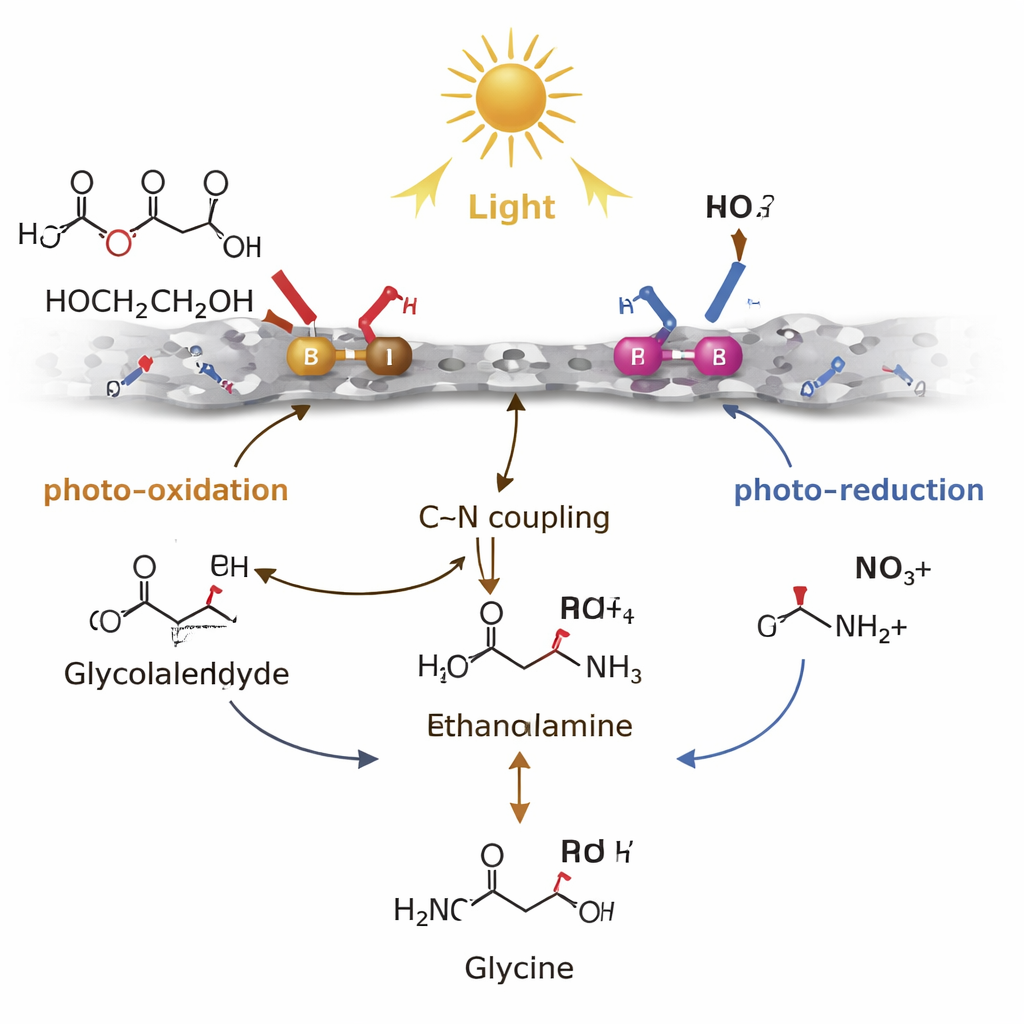
Do Mecanismo de Laboratório ao Resíduo do Mundo Real
Os pesquisadores confirmaram cada parte dessa via com um conjunto de técnicas, acompanhando radicais, intermediários e produtos nitrogenados em tempo real. Eles compararam diferentes materiais catalíticos e metais e descobriram que suportes de g‑C3N4 com pares isolados Pd–B tiveram o melhor desempenho, alcançando taxas de produção de glicina de 2,9 milimoles por grama de catalisador por hora. O catalisador manteve‑se ativo ao longo de ciclos repetidos, e sua estrutura permaneceu estável. Importante, a equipe foi além de produtos químicos de laboratório puros. Demonstraram produção de glicina em escala de gramas a partir de PET pós‑consumo real — pó, garrafas, roupas, sacolas e mais — combinado com soluções de nitrato e até efluentes complexos. Também mostraram que álcoois relacionados provenientes de biomassa, como glicerol, podem servir como fontes alternativas de carbono, ampliando a relevância da abordagem.
Uma Rota Vantajosa para Resíduos e Clima
Para aproximar o conceito da prática, os autores testaram seu processo sob luz solar natural concentrada por uma lente de Fresnel simples. O sistema produziu glicina de forma consistente com alta seletividade, e modelos sugerem que sua ampliação poderia evitar emissões substanciais de dióxido de carbono e prevenir o lançamento de nitrato no ambiente. Em termos simples, este trabalho descreve uma maneira de converter pilhas de plástico usado e água poluída em um aminoácido útil, usando apenas luz e um catalisador finamente ajustado. Embora desafios de engenharia permaneçam antes do emprego industrial, o estudo destaca como o projeto de catalisadores a nível atômico pode transformar duas grandes correntes de resíduo em um único produto químico valioso.
Citação: Ya, Z., Li, M., Fu, D. et al. Glycine photosynthesis via C−N coupling of waste plastic and nitrate over diatomic Pd−B catalyst. Nat Commun 17, 1887 (2026). https://doi.org/10.1038/s41467-026-68666-z
Palavras-chave: glicina, reciclagem de plástico, fotocatálise, efluente com nitrato, catalisadores de átomo único