Clear Sky Science · pt
Regulação da montagem do adaptador AP1 pela chaperona ambidestra MEA1
Por que esse ajudante oculto da célula importa
Dentro de cada célula humana, milhares de pequenas encomendas transportam proteínas para onde são necessárias ou para o “centro de reciclagem” celular para degradação. Esse tráfego mantém nossas células saudáveis e regula nossas defesas imunológicas. O artigo resumido aqui revela uma proteína antes misteriosa, chamada MEA1, que se mostra essencial para montar uma das máquinas de triagem que carregam essas encomendas. Entender como a MEA1 funciona ajuda a explicar como as células controlam cargas importantes, incluindo moléculas que ligam e desligam respostas antivirais imunes.
Controle de tráfego no centro de envio da célula
Muita da atividade de transporte da célula passa por uma estrutura chamada Golgi, um empilhamento de sacos achatados que funciona como um correio central. Do Golgi, a carga pode ser enviada para uso na superfície celular ou redirecionada para compartimentos internos para degradação. Um complexo proteico conhecido como AP1 fica no coração dessa rota. O AP1 reconhece marcas nas proteínas de carga, ajuda a curvar a membrana e recruta uma camada externa de clatrina para formar pequenos vesículos de transporte. Sem o AP1 corretamente montado, cargas cruciais se acumulam nos lugares errados e vias de sinalização normais, incluindo as ligadas à imunidade, podem se desregular. 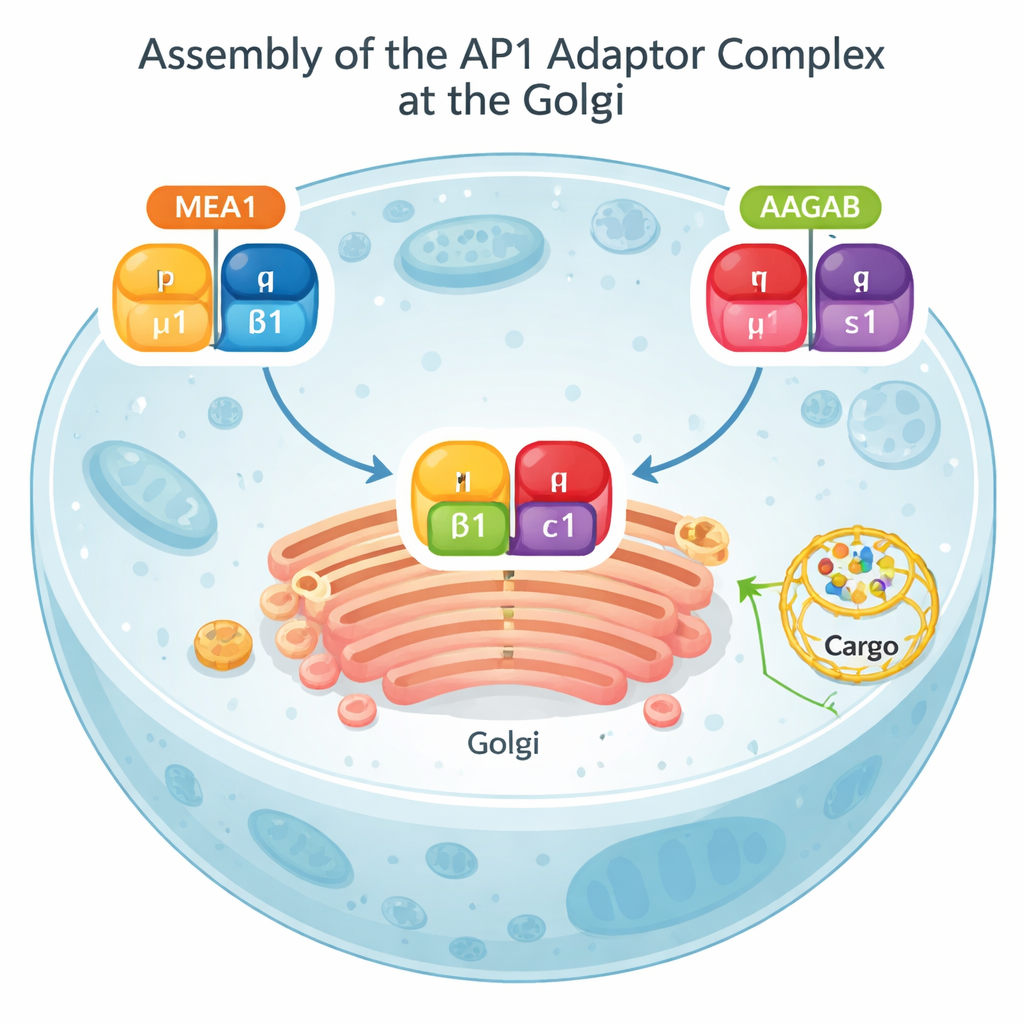
Encontrando um trabalhador de montagem ausente
Os autores buscaram identificar proteínas que se associam fisicamente ao AP1 e que poderiam ajudá-lo a se montar. Eles cruzaram um grande banco de dados de interações proteicas, eliminaram candidatos improváveis de agir com o AP1 e então usaram uma ferramenta de inteligência artificial, o AlphaFold, para prever como as proteínas restantes poderiam contatar as partes individuais do AP1. Essa busca destacou a MEA1, uma proteína pequena e previamente não caracterizada presente em muitos tecidos. Experimentos complementares em células humanas confirmaram que a MEA1 se liga a duas subunidades específicas do AP1, conhecidas como μ1 e β1, tanto quando testadas isoladamente quanto em suas formas naturais não modificadas.
MEA1 mantém o AP1 intacto e o tráfego de cargas em movimento
Para investigar o que a MEA1 realmente faz, os pesquisadores deletaram o gene MEA1 em linhas celulares humanas. Quando a MEA1 estava ausente, as quatro peças do AP1 foram drasticamente reduzidas, e os pontos característicos do AP1 próximos ao Golgi quase desapareceram. Essa perda teve consequências funcionais claras. Uma carga do AP1, o receptor de folato FOLR1, acumulou-se na superfície celular em vez de ser enviada para o interior, um marco de triagem do AP1 defeituosa. Outra carga, a proteína de sinalização imune STING, deixou de ser eficientemente empacotada em vesículas destinadas aos lisossomos, os centros de reciclagem da célula. Como resultado, a STING ativada e sua quinase parceira TBK1 permaneceram em níveis elevados, indicando que o “interruptor de desligamento” dessa via antiviral não estava funcionando corretamente. A reintrodução da MEA1 restaurou os níveis de AP1 e corrigiu esses defeitos de tráfego.
Uma chaperona de duas mãos e um processo de montagem por colisão
Testes bioquímicos e modelos do AlphaFold revelaram que a MEA1 se comporta como uma chaperona de “duas mãos”: sua porção frontal agarra a subunidade μ1, enquanto sua porção traseira agarra a β1. Isoladas, μ1 e β1 são instáveis e tendem a agregar ou ser degradadas; quando ligadas à MEA1, tornam-se solúveis e prontas para montar-se. Outra chaperona conhecida, AAGAB, desempenha um papel paralelo para as duas subunidades restantes do AP1, γ e σ1. Quando os complexos MEA1–μ1–β1 e AAGAB–γ–σ1 se encontram, suas subunidades se combinam em um adaptador AP1 completo de quatro partes. Nesse ponto, ambas as chaperonas se soltam e retornam ao fluido celular, enquanto o AP1 recém-formado se dirige às membranas para realizar seu trabalho de triagem. Esse mecanismo de “colisão dupla de chaperonas” mostra que a montagem do AP1 é cuidadosamente orquestrada, e não deixada ao acaso.
Liçons mais amplas sobre controle de qualidade celular
Além do AP1, o estudo sugere uma estratégia mais geral que as células podem usar para montar muitas máquinas proteicas grandes. A MEA1 também pode ajudar de forma fraca outro complexo adaptador chamado AP2, e junto com AAGAB e uma terceira chaperona chamada CCDC32, ilustra uma via mais ampla que os autores chamam de “Montagem de Proteínas Adaptadoras Assistida por Chaperonas”. Nesse esquema, chaperonas especializadas estabilizam subunidades frágeis, aproximam os pares corretos e bloqueiam temporariamente sítios de ligação de carga até que o complexo esteja totalmente formado e seguro para ser empregado. 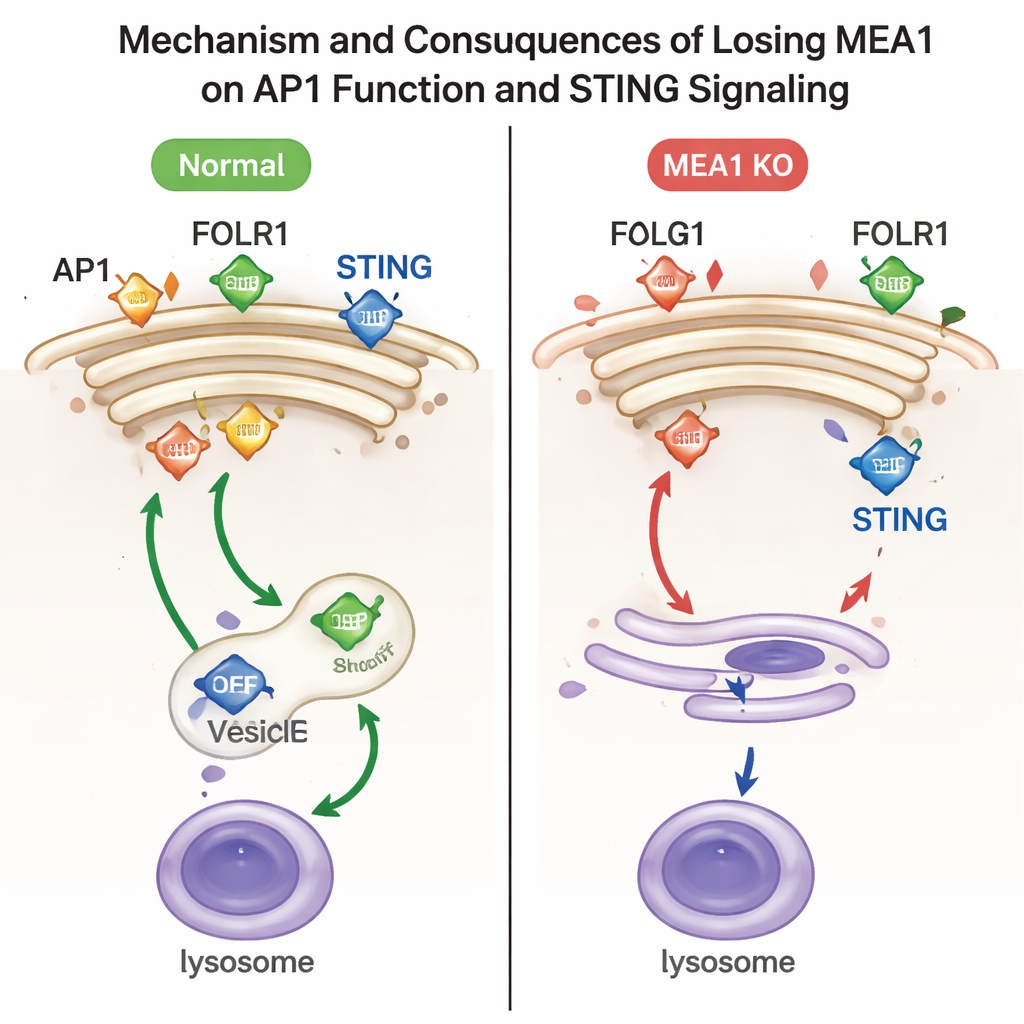
O que isso significa para saúde e doença
Para não especialistas, a principal conclusão é que a MEA1 é um trabalhador crucial dos bastidores que ajuda a montar o AP1, uma máquina central de triagem em nossas células. Quando a MEA1 está ausente, o AP1 se desmonta, engarrafamentos se formam e reguladores importantes como a STING não são desligados corretamente. Essa nova compreensão pode eventualmente ajudar a explicar certos distúrbios imunológicos ou outras doenças ligadas ao tráfego proteico defeituoso, além de revelar um princípio geral sobre como as células constroem com segurança máquinas moleculares complexas a partir de partes instáveis.
Citação: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
Palavras-chave: trânsito de proteínas, proteína adaptadora AP1, chaperonas moleculares, sinalização STING, biologia celular