Clear Sky Science · pt
Reconhecimento molecular da tiroglobulina pela sortilina
Como as células da tireoide decidem quando liberar hormônio
Os hormônios tireoidianos ajudam a ajustar o “termostato” metabólico do corpo, influenciando desde a frequência cardíaca até a temperatura corporal. Esses hormônios são construídos e armazenados dentro de uma proteína gigante chamada tiroglobulina. Este estudo revela como outra proteína, a sortilina, ajuda as células tireoidianas a escolher qual forma da tiroglobulina recuperar para dentro da célula para que o hormônio possa ser liberado na corrente sanguínea — uma decisão que, em última instância, afeta a quantidade de hormônio tireoidiano disponível para o organismo.
Uma proteína de armazenamento à espera de processamento
A tiroglobulina é uma proteína maciça, em forma de Y, produzida e secretada pelas células da tireoide para uma matriz gelatinosa chamada coloide. Lá, ela atua tanto como matéria-prima quanto como depósito para o hormônio tireoidiano: blocos construtores específicos (aminoácidos) dentro da tiroglobulina são quimicamente modificados com iodo para se tornarem hormônios tireoidianos, ainda incorporados na proteína maior. Para liberar esses hormônios, a tiroglobulina precisa ser reabsorvida pela célula, fragmentada dentro de compartimentos de reciclagem chamados lisossomos, e os pedaços hormonais transportados para o sangue.
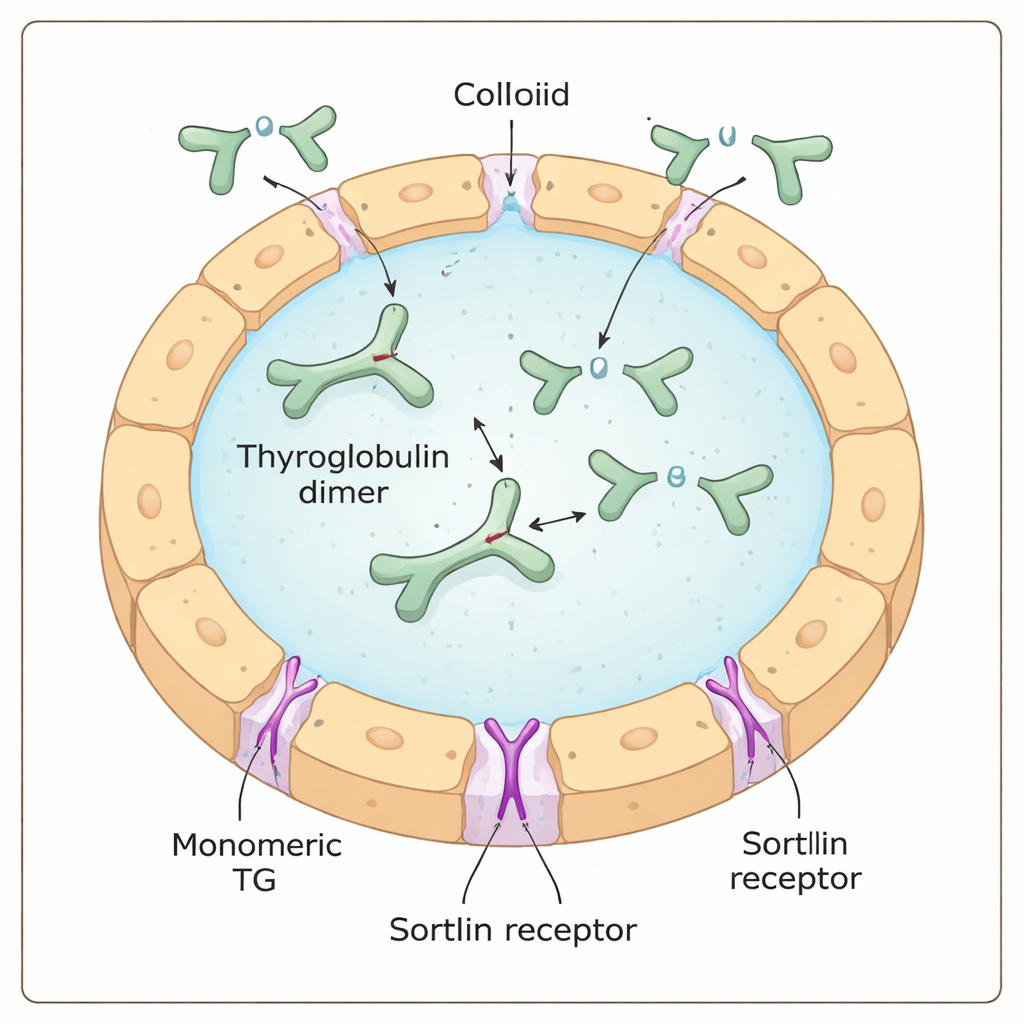
Um porteiro celular com uma preferência oculta
O receptor sortilina tem sido proposto como um dos “porteiros” que se ligam à tiroglobulina na superfície celular e a conduzem para o interior. Trabalhos anteriores sugeriam que a sortilina preferia tiroglobulina altamente iodada, insinuando que o receptor poderia, de alguma forma, detectar diretamente o teor de iodo. Usando uma combinação de testes bioquímicos, medidas de massa por molécula única e experimentos de captação em células, os autores descobriram, em vez disso, que a sortilina favorece fortemente a forma monomérica (unidade única) da tiroglobulina em relação à sua forma pareada mais comum, a dímera. Quanto mais monômero havia numa amostra, mais eficientemente ela formava complexos com a sortilina e era internalizada pelas células tireoidianas, independentemente da quantidade de iodo que carregava.
Ampliando o ponto de contato
Para entender essa preferência em nível atômico, a equipe recorreu à criomicroscopia eletrônica de alta resolução e à espectrometria de massa com cross-linking. Esses métodos mostraram que a sortilina reconhece uma cauda curta e flexível no terminal C (uma extremidade) da tiroglobulina monomérica. Essa cauda se insere numa cavidade central da sortilina, em forma de hélice de dez lâminas, encaixando-se em dois pequenos “pontos quentes” internos. Notavelmente, na forma dimérica da tiroglobulina, parte da região ao redor dessa cauda fica enterrada, de modo que a sortilina não consegue acessá-la, explicando por que o dímero é um parceiro pobre. Os dados sugerem que o aparo ou o relaxamento extracelular da tiroglobulina — por degradação protéica natural — ajuda a converter dímeros em monômeros que a sortilina pode agarrar.
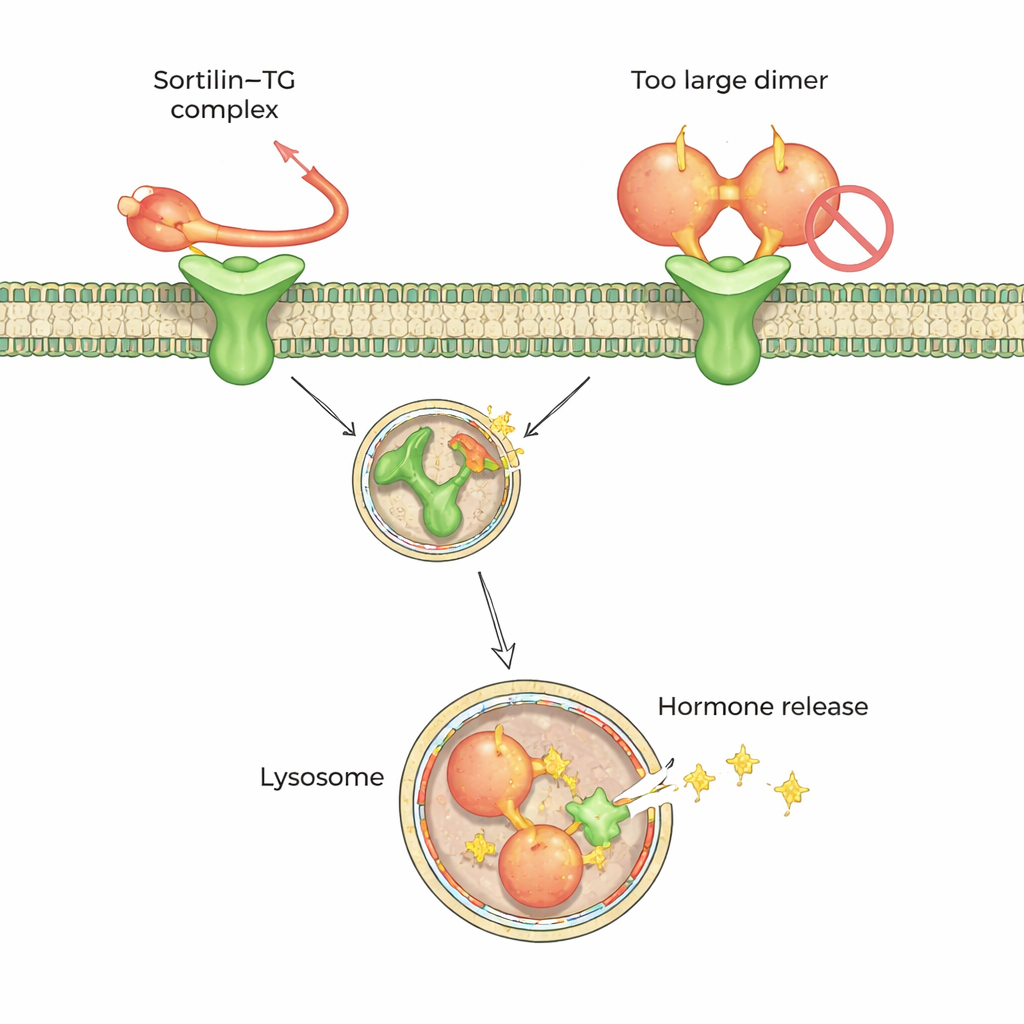
Um código de acoplagem compartilhado por muitas proteínas cargueiras
A sortilina não é apenas uma proteína tireoidiana; ela ajuda a trafegar muitas moléculas diferentes pelo corpo, incluindo fatores ligados a doenças cardíacas e distúrbios cerebrais. Ao combinar seu trabalho estrutural com ferramentas avançadas de predição de estrutura, como AlphaFold e AlphaPulldown, os pesquisadores compararam como dezenas de parceiros conhecidos da sortilina poderiam se ligar à sua cavidade em forma de hélice. Encontraram um padrão recorrente: muitos cargueiros apresentam um segmento peptídico não estruturado de cerca de vinte aminoácidos que se encaixa no mesmo bolso que a cauda da tiroglobulina, às vezes orientado na mesma direção de um peptídeo cerebral conhecido chamado neurotensina, e às vezes na direção oposta. Apesar da orientação invertida, esses peptídeos compartilham características semelhantes — um grupo ácido ou carregado negativamente em uma extremidade, um resíduo aromático volumoso na outra, e um trecho flexível, frequentemente rico em prolina, no meio.
Por que o iodo importa menos que a forma
Como o contato-chave entre sortilina e tiroglobulina é essa cauda flexível, os autores testaram se iodinar um resíduo de tirosina formador de hormônio na cauda alteraria a ligação. Não alterou: um peptídeo sintético carregando um hormônio tireoidiano completamente formado comportou-se quase de forma idêntica à versão não modificada. Modelagem mostrou que o anel iodinado projeta-se para o solvente sem criar novos contatos apertados. Junto com os experimentos de captação, isso apoia uma visão revisada: a sortilina não “conta” átomos de iodo na tiroglobulina. Em vez disso, ela percebe se a proteína relaxou ou foi parcialmente degradada o suficiente para expor sua forma monomérica e a cauda de maneira acessível.
O que isso significa para a saúde da tireoide
Para um não especialista, a mensagem central é que a liberação de hormônio tireoidiano é controlada menos por um sensor interno de iodo e mais por uma verificação mecânica da forma e flexibilidade da proteína. A sortilina atua como um scanner na superfície celular, procurando moléculas de tiroglobulina que foram afrouxadas ou aparadas em monômeros, e então as puxa para dentro para a liberação final do hormônio e a reciclagem do iodo. Este trabalho esclarece um passo-chave na biologia do hormônio tireoidiano e sugere que drogas projetadas para bloquear a sortilina — atualmente exploradas para outras doenças — poderiam, inadvertidamente, alterar o manejo do hormônio tireoidiano ao perturbar esse passo de reconhecimento.
Citação: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Palavras-chave: hormônio tireoidiano, tiroglobulina, sortilina, transporte de proteínas, endocitose