Clear Sky Science · pt
A hélice de ligação (bridge helix) da Cas12a é um regulador alostérico da formação do R-loop e da ativação do RuvC
Por que isso importa para a edição gênica
Muitas ferramentas poderosas de edição gênica, incluindo aquelas por trás de terapias emergentes e testes diagnósticos rápidos, dependem de proteínas CRISPR que cortam DNA em locais escolhidos. Mas se essas tesouras moleculares cortarem o lugar errado, podem causar efeitos adversos. Este estudo dissecou uma pequena peça móvel dentro do editor Cas12a, chamada hélice de ligação, e mostra como suas mudanças de forma atuam como um interruptor de segurança interno que vincula o reconhecimento correto do alvo ao corte do DNA. Entender esse interruptor oferece um roteiro para projetar ferramentas CRISPR mais precisas e mais seguras para aplicações médicas e biotecnológicas.
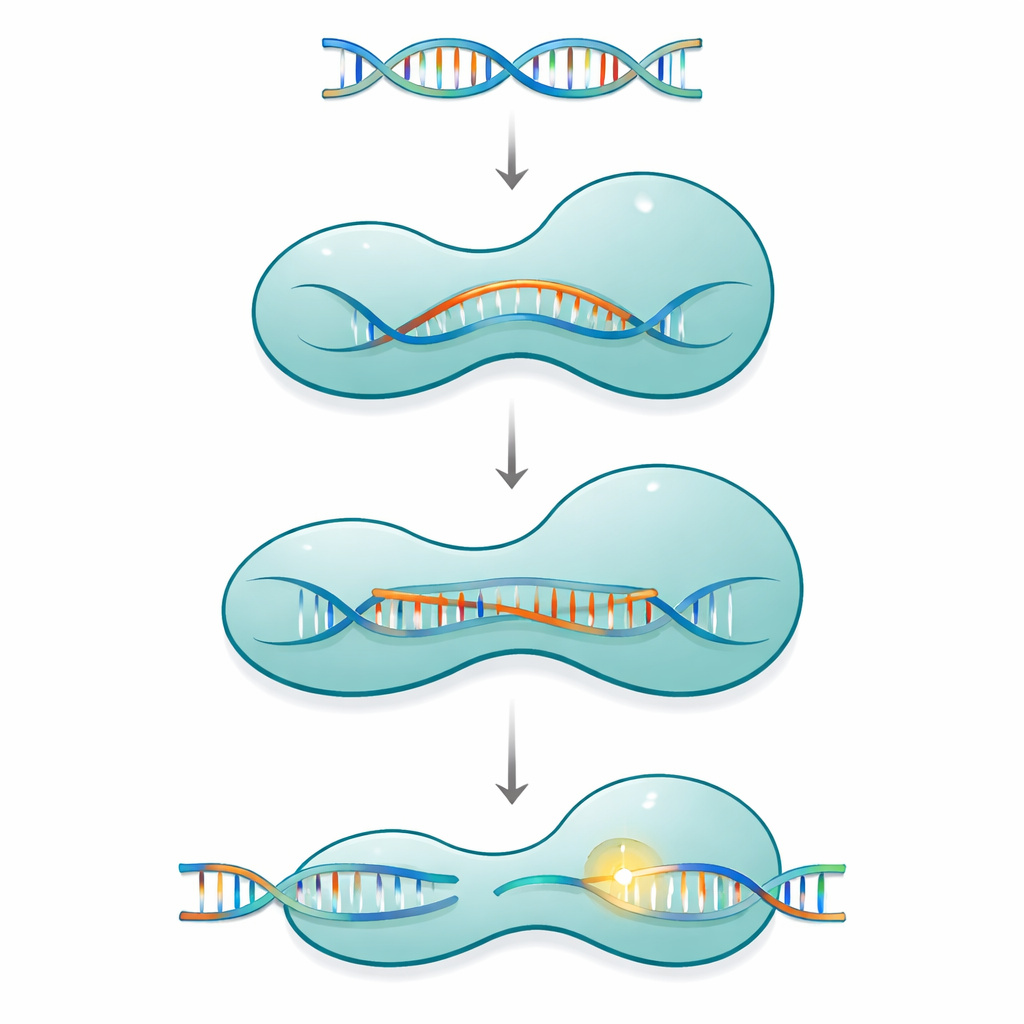
Uma braçadeira molecular com partes móveis
Cas12a pertence a uma família de sistemas CRISPR formados por uma única proteína que usam um pequeno RNA guia para localizar e cortar DNA correspondente em vírus ou no genoma da célula. A proteína tem a forma de uma braçadeira de dois braços: um lado de reconhecimento que verifica a sequência, e um lado de corte que abriga a maquinaria química. Essas duas metades são conectadas por um segmento delgado e carregado positivamente chamado hélice de ligação. À medida que a Cas12a se liga ao RNA guia e depois ao DNA alvo, a proteína não age como uma ferramenta rígida. Em vez disso, ela passa por uma série de grandes e pequenas mudanças conformacionais que gradualmente se fecham ao redor de uma estrutura híbrida RNA–DNA em crescimento conhecida como R-loop, ativando totalmente o sítio de corte apenas quando um trecho suficientemente longo de pareamento correto de bases foi formado.
Investigando o interruptor de segurança embutido
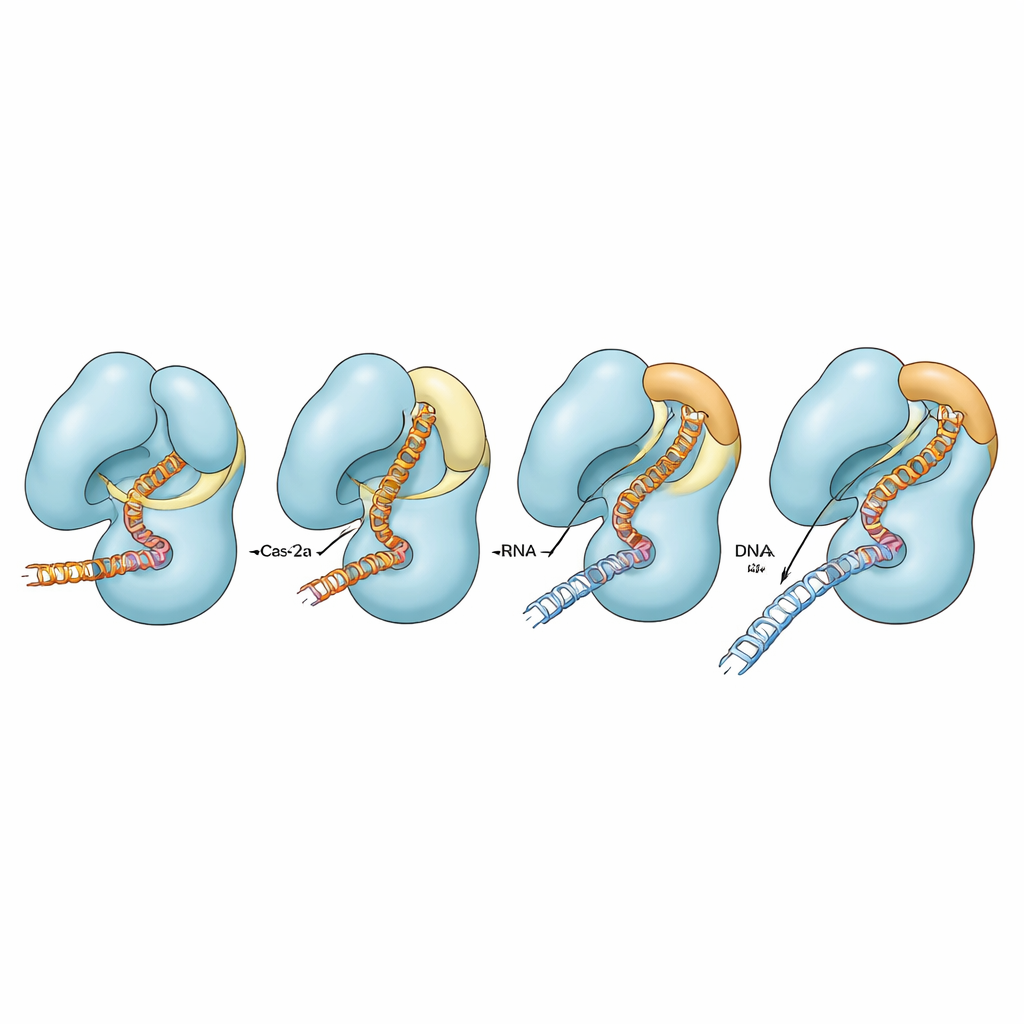
Os pesquisadores enfocaram uma Cas12a da bactéria Francisella novicida e uma versão previamente engenheirada na qual dois aminoácidos na hélice de ligação foram substituídos por prolina, uma mudança conhecida por tornar hélices mais rígidas ou interrompê-las. Essa variante, chamada FnoCas12aKD2P, corta o DNA de forma mais seletiva, porém mais lenta do que a proteína natural. Usando criomicroscopia eletrônica (cryo-EM), capturaram cinco instantâneos estruturais distintos dessa variante ligada ao seu RNA guia e a um trecho de DNA alvo. Esses instantâneos mostram a proteína em diferentes estágios ao longo de sua via de ativação, desde o reconhecimento inicial do DNA até estados posteriores em que parte do híbrido RNA–DNA está formada, mas a prontidão completa para o corte ainda não foi alcançada.
Como as mudanças de forma dirigem cortes precisos
Comparar a variante com estruturas previamente determinadas da Cas12a normal revelou um padrão claro. Na proteína natural, um segmento da hélice de ligação se converte de um laço frouxo em uma hélice mais longa e reta e curva-se em direção ao híbrido RNA–DNA em crescimento, entrando em contato próximo com ele. Ao mesmo tempo, uma hélice vizinha no domínio de corte afrouxa, e uma pequena região chamada de “tampa” (lid), que normalmente bloqueia o sítio ativo, vira de um laço em uma hélice e se abre. Juntos, esses movimentos coordenados abrem uma cavidade que permite que uma única fita de DNA entre e seja cortada. Na variante contendo prolina, a hélice de ligação não consegue executar completamente essa transição de laço para hélice nem curvar-se adequadamente. Como resultado, o híbrido RNA–DNA permanece distorcido e mais afastado, a tampa permanece em um estado fechado, semelhante a um laço, e o complexo raramente alcança uma conformação pré-catalítica completa. Esse gargalo mecânico desacelera o corte no alvo e dificulta a passagem de DNA com incompatibilidades pelos pontos de verificação internos.
Ajustando a fidelidade mexendo nos contatos
Para testar como diferentes contatos ao redor da tampa e da hélice de ligação contribuem para a atividade, os autores alteraram resíduos carregados específicos que ligam essas regiões. Na Cas12a normal, romper esses contatos teve apenas efeitos modestos no corte de DNA perfeitamente pareado, embora algumas condições tenham afetado a eficiência com que a segunda fita de DNA era clivada quando havia incompatibilidades. No contexto da hélice de ligação comprometida, contudo, as mesmas substituições reduziram severamente ou quase aboliram o corte de ambas as fitas, especialmente quando o guia e o DNA não eram perfeitamente correspondentes. Simulações computacionais sustentaram esses achados, mostrando que somente quando a hélice de ligação pode adotar completamente sua forma helicoidal é que a ponte, a hélice adjacente, a tampa e os ácidos nucleicos se movem de maneira fortemente coordenada. Quando a hélice está comprometida, esses movimentos tornam-se parcial ou totalmente desacoplados, e a enzima tem dificuldade em completar seu ciclo catalítico.
Um guia de projeto para ferramentas CRISPR de próxima geração
No geral, o trabalho revela a hélice de ligação como uma alavanca de controle interna que vincula o comprimento e a qualidade do híbrido RNA–DNA à abertura do bolso de corte na Cas12a. Ao forçar a proteína a completar uma sequência específica de mudanças conformacionais antes de clivar o DNA, esse mecanismo naturalmente reforça a discriminação de incompatibilidades. As descobertas ajudam a explicar por que alterações direcionadas nessa pequena região podem gerar variantes de Cas12a com corte fora do alvo reduzido e atividade colateral de DNA diminuída — propriedades desejáveis para edição genômica e diagnósticos mais seguros. Mais amplamente, o estudo destaca como mudanças sutis em hélices curtas podem coordenar comunicação de longo alcance em grandes máquinas moleculares, oferecendo princípios gerais para a engenharia de enzimas de processamento de ácidos nucleicos de alta fidelidade.
Citação: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
Palavras-chave: CRISPR-Cas12a, fidelidade de edição gênica, hélice de ligação, formação de R-loop, regulação alostérica