Clear Sky Science · pt
RoboA reforça o destino de células-tronco planárias por meio de FoxA e Anosmin1a
Como vermes regeneram seus órgãos
Algumas planárias conseguem regenar quase qualquer parte do corpo que falta, do tubo alimentar ao cérebro. Essa habilidade notável depende de células-tronco adultas que podem se transformar em muitos tipos celulares diferentes sob demanda. Mas com tanta liberdade, como essas células evitam construir o tecido errado no lugar errado — por exemplo, gerar células do estômago na cabeça em vez de neurônios? Este estudo usa a planária para descobrir como um pequeno conjunto de sinais mantém células-tronco altamente flexíveis no caminho certo durante a regeneração.
O verme em regeneração e seu potencial oculto
A planária Schmidtea mediterranea é um modelo preferido para estudar regeneração porque uma grande população de células-tronco está distribuída por todo o seu corpo. Um órgão-chave é a faringe, um tubo muscular de alimentação que fica no meio do verme e se conecta ao exterior quando o animal se alimenta. Trabalhos anteriores mostraram que um gene chamado foxA é crucial para reconstruir essa faringe após lesão, e que apenas certas células-tronco próximas à faringe normalmente ativam foxA. O novo estudo faz uma pergunta aparentemente simples: o que impede células-tronco em outras regiões — especialmente na cabeça e no cérebro — de também escolherem uma identidade de faringe?
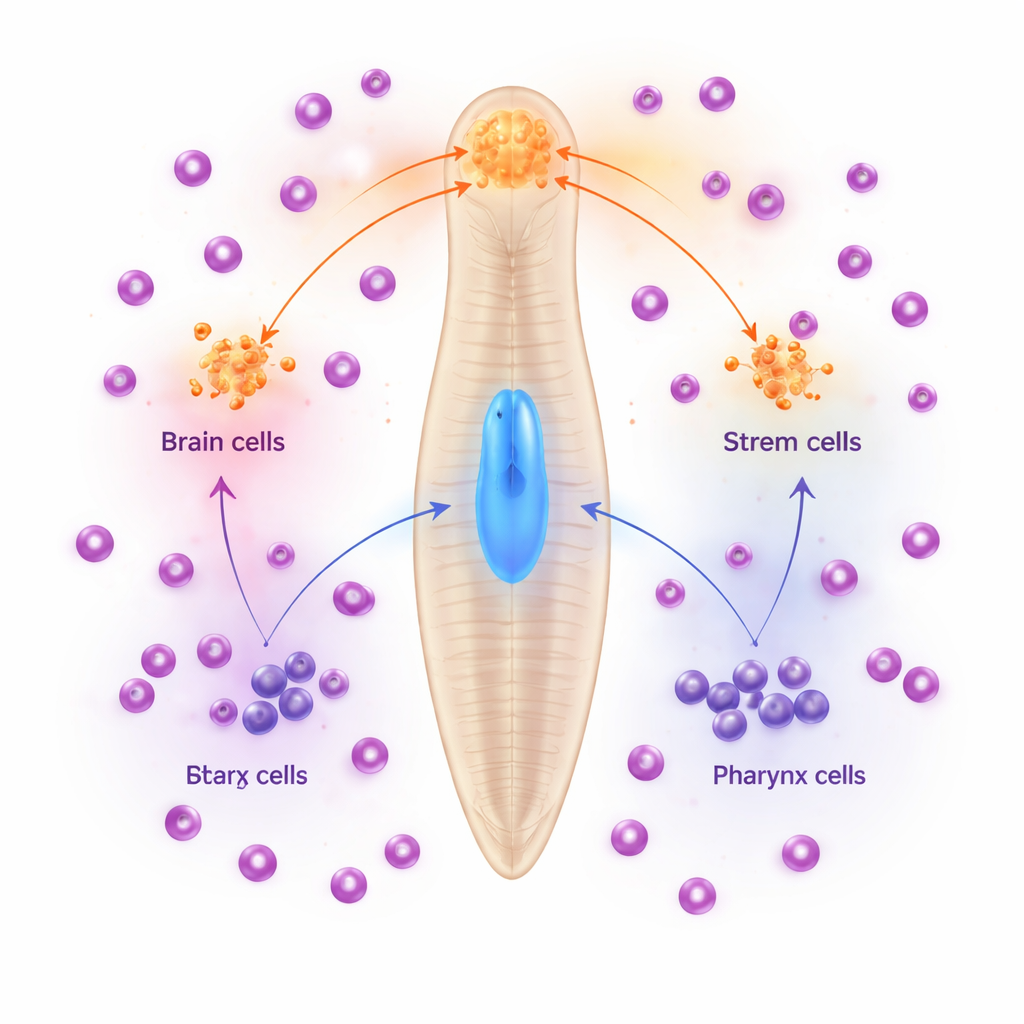
Quando a orientação falta
Os pesquisadores concentraram-se em uma proteína receptora chamada RoboA, encontrada em níveis baixos em muitos tipos celulares, inclusive nas células-tronco. Quando reduziram a atividade de RoboA usando interferência por RNA, os animais frequentemente desenvolveram faringes extras e deslocadas após serem cortados. Uma inspeção mais detalhada revelou algo mais sutil: mesmo em vermes não lesionados, reduzir RoboA fez com que neurônios e músculos com aparência de faringe aparecessem dentro da região cerebral. Esses “neurônios de faringe ectópicos” se comportaram como células de faringe normais em termos de expressão gênica, mas estavam no lugar errado. Importante: o plano corporal geral e a arquitetura cerebral permaneciam amplamente intactos, sugerindo que RoboA não estava redesenhando o animal inteiro, mas sim ajustando finamente o que as células-tronco próximas se tornavam.
Um interruptor de três participantes para o destino celular
Para entender como RoboA funciona, a equipe procurou parceiros fora da célula. Embora proteínas Robo sejam mais conhecidas por se ligar a um ligante chamado Slit, derrubar Slit não reproduziu as células de faringe deslocadas. Uma triagem ampla por RNAi de proteínas secretadas e de membrana apontou, em vez disso, para Anosmin1a (Anos1a), uma proteína secretada relacionada a um fator humano envolvido na síndrome de Kallmann. Reduzir Anos1a causou neurônios de faringe extras semelhantes, e knockdowns combinados de RoboA–Anos1a comportaram-se como se atuassem na mesma via. Ao mesmo tempo, perfis moleculares mostraram que o fator de transcrição FoxA está no centro da decisão: quando RoboA está presente, ele mantém FoxA desligado nas células-tronco da cabeça; quando a sinalização de RoboA é removida, FoxA é ativado e essas mesmas células-tronco podem escolher um destino de neurônio de faringe mesmo estando no cérebro.
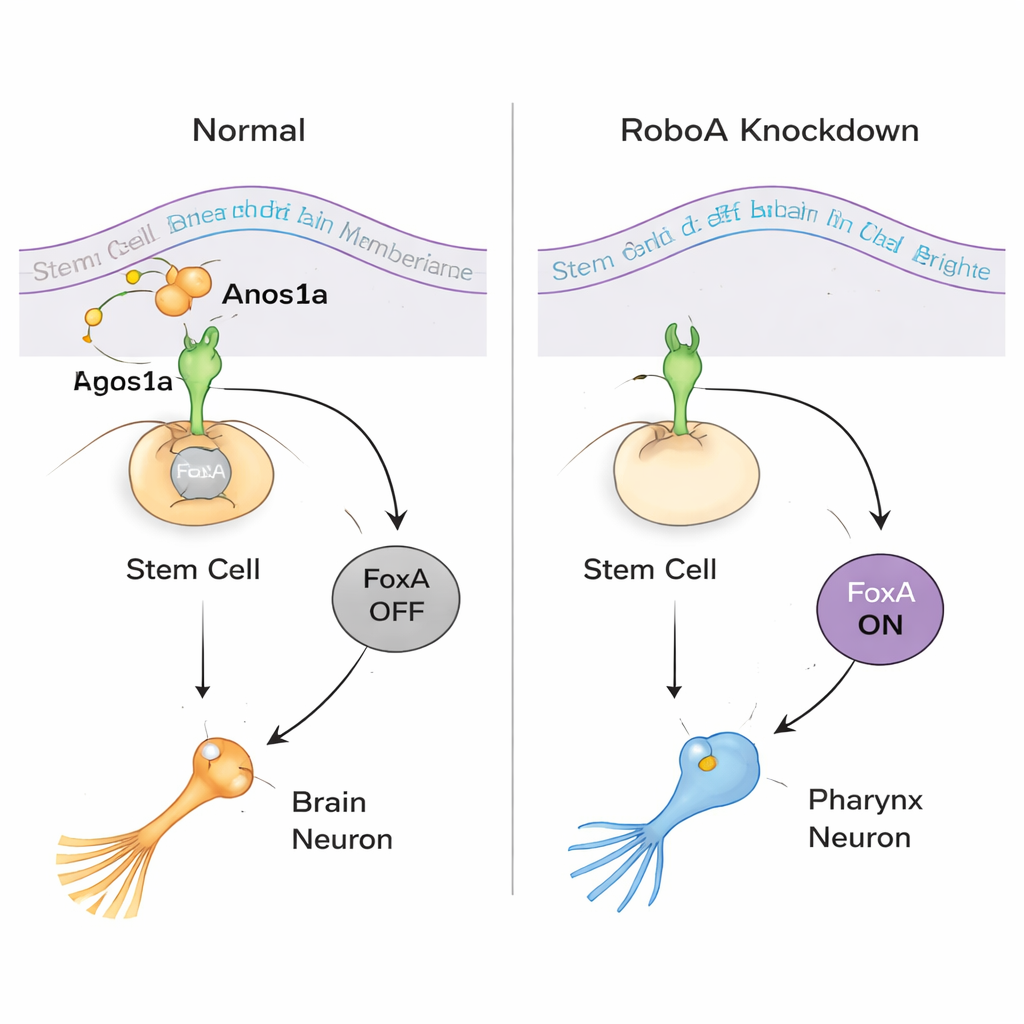
Revelando uma escolha bidirecional nas células-tronco
A equipe então perguntou se essa flexibilidade operava em ambas as direções. Em animais normais, as células-tronco ao redor da faringe dependem de FoxA para se tornarem neurônios e células epiteliais da faringe, enquanto os músculos da faringe seguem uma rota diferente. Quando FoxA foi suprimido por períodos mais longos, os vermes perderam suas faringes inteiramente e desenvolveram crescimentos anormais no meio do corpo. Sequenciamento de RNA de célula única e análise de marcadores revelaram que esses crescimentos continham muitos tipos celulares normalmente restritos à cabeça, incluindo células oculares e neurônios específicos do cérebro. Em outras palavras, quando FoxA está ausente onde a faringe deveria se formar, as células-tronco locais tendem a um destino parecido com o do cérebro. Essa descoberta mostra que as mesmas células-tronco podem ser direcionadas tanto para identidades “faringe” quanto “cérebro”, dependendo dos sinais que recebem.
Ajustando a regeneração, não redesenhando o mapa
Juntando todas as evidências, os autores propõem que a regeneração planária é guiada em duas camadas. Sinais amplos de “controle de posição”, como Wnt e outras moléculas de padronização, estabelecem o mapa grosseiro de cabeça, tronco e cauda. Sobre isso, genes locais “reforçadores de destino” como RoboA e Anos1a atuam como verificações de segurança, bloqueando opções inapropriadas. Na cabeça, a sinalização RoboA–Anos1a mantém FoxA desligado para que as células-tronco produzam neurônios cerebrais em vez de células de faringe; perto da faringe, FoxA é permitida se ligar e direcionar destinos específicos da faringe. Esse controle em camadas permite que as células-tronco planárias permaneçam extraordinariamente plásticas, ao mesmo tempo em que reconstruem órgãos no lugar certo, oferecendo um roteiro de como a regeneração robusta pode coexistir com uma ordem anatômica rigorosa.
Citação: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
Palavras-chave: regeneração de planárias, plasticidade de células-tronco, padronização de órgãos, sinalização RoboA, fator de transcrição FoxA