Clear Sky Science · pt
NeoPrecis: aprimorando a predição de resposta à imunoterapia por meio da integração de paisagens de neoantígenos qualificadas e cientes da clonalidade
Por que alguns cânceres respondem à imunoterapia e outros não
A imunoterapia transformou o cuidado do câncer, mas muitos pacientes ainda não se beneficiam e alguns enfrentam efeitos colaterais graves. Uma grande questão é por que alguns tumores são identificados e destruídos pelo sistema imunológico enquanto outros escapam. Este estudo apresenta o NeoPrecis, um método computacional que examina mais de perto as “bandeiras” que os tumores exibem ao sistema imunológico — chamadas neoantígenos — e usa essa informação para prever com mais precisão quais pacientes têm maior probabilidade de responder às imunoterapias modernas.
Novas bandeiras nas células cancerosas
As células cancerosas acumulam mutações no DNA que podem alterar as proteínas que produzem. Pequenos fragmentos dessas proteínas alteradas, conhecidos como neoantígenos, podem ser exibidos na superfície celular e reconhecidos como estranhos pelas células T, os assassinos do sistema imunológico. Por anos, médicos e pesquisadores dependeram de medidas grosseiras como a carga mutacional tumoral — o número total de mutações — para estimar a probabilidade de um câncer responder a inibidores de checkpoint imunológico. Mas isso é uma ferramenta imprecisa: nem toda mutação gera um alvo visível ou atraente para as células T, e os tumores podem ser colchas de retalhos de muitos subtipos celulares. O NeoPrecis foi projetado para ir além da simples contagem de mutações e, em vez disso, avaliar quantas delas são genuinamente alvos promissores em todo o tumor.
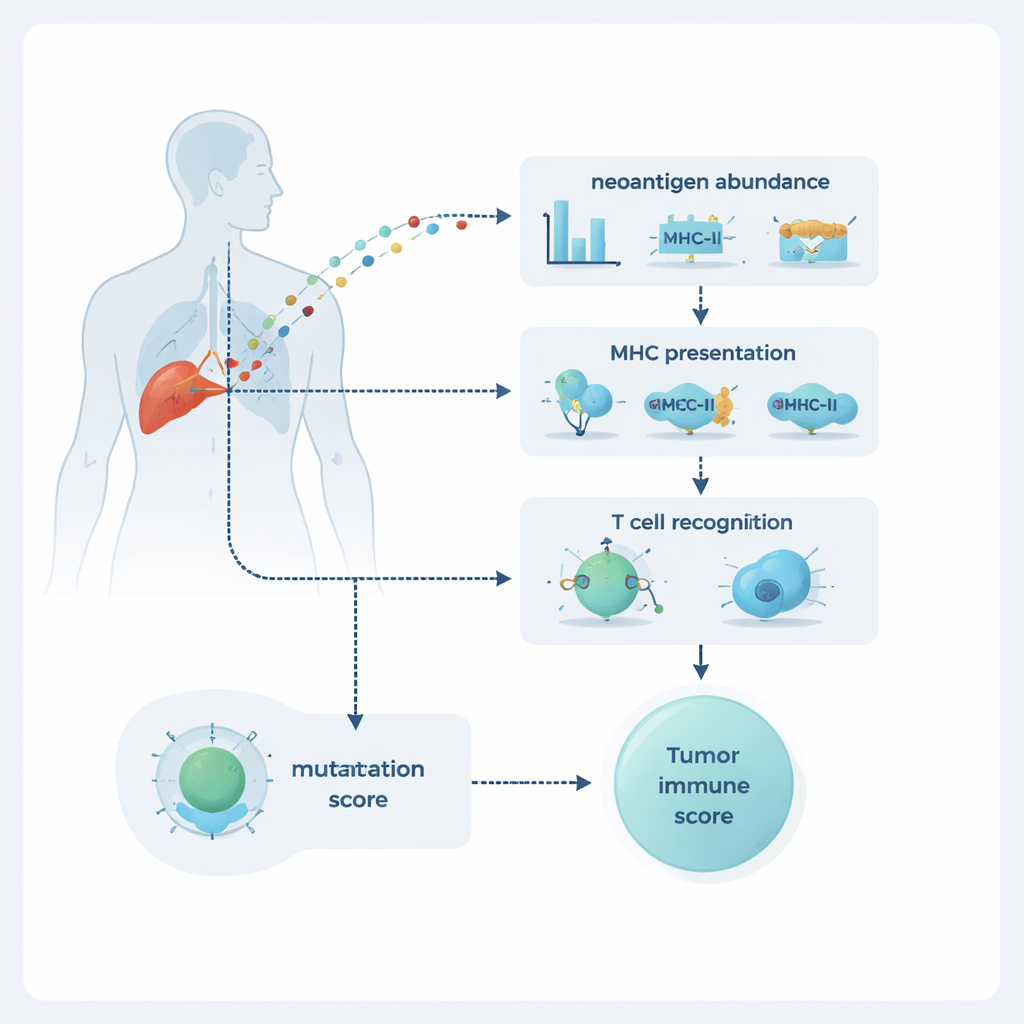
Analisando três ingredientes-chave ao mesmo tempo
O NeoPrecis avalia cada mutação em três dimensões: quão abundante ela é no tumor, se é provável que seja exibida na superfície celular e quão provável é que seja notada pelas células T. A abundância é estimada a partir do sequenciamento de DNA e RNA, que revelam quão comum é a mutação e quão fortemente ela é expressa. A exibição é modelada pelo acoplamento a moléculas chamadas MHC classe I e classe II, que funcionam como painéis exibindo fragmentos de proteínas às células T. A parte mais inovadora é o componente de reconhecimento pelas células T, o NeoPrecis-Immuno. Esse modelo aprende a partir de grandes bancos de dados de interações conhecidas entre células T e peptídeos para avaliar quão diferente um fragmento mutado é em relação ao seu equivalente normal de uma forma que importe para o reconhecimento pelas células T, levando também em conta as variantes específicas de MHC que cada pessoa carrega.
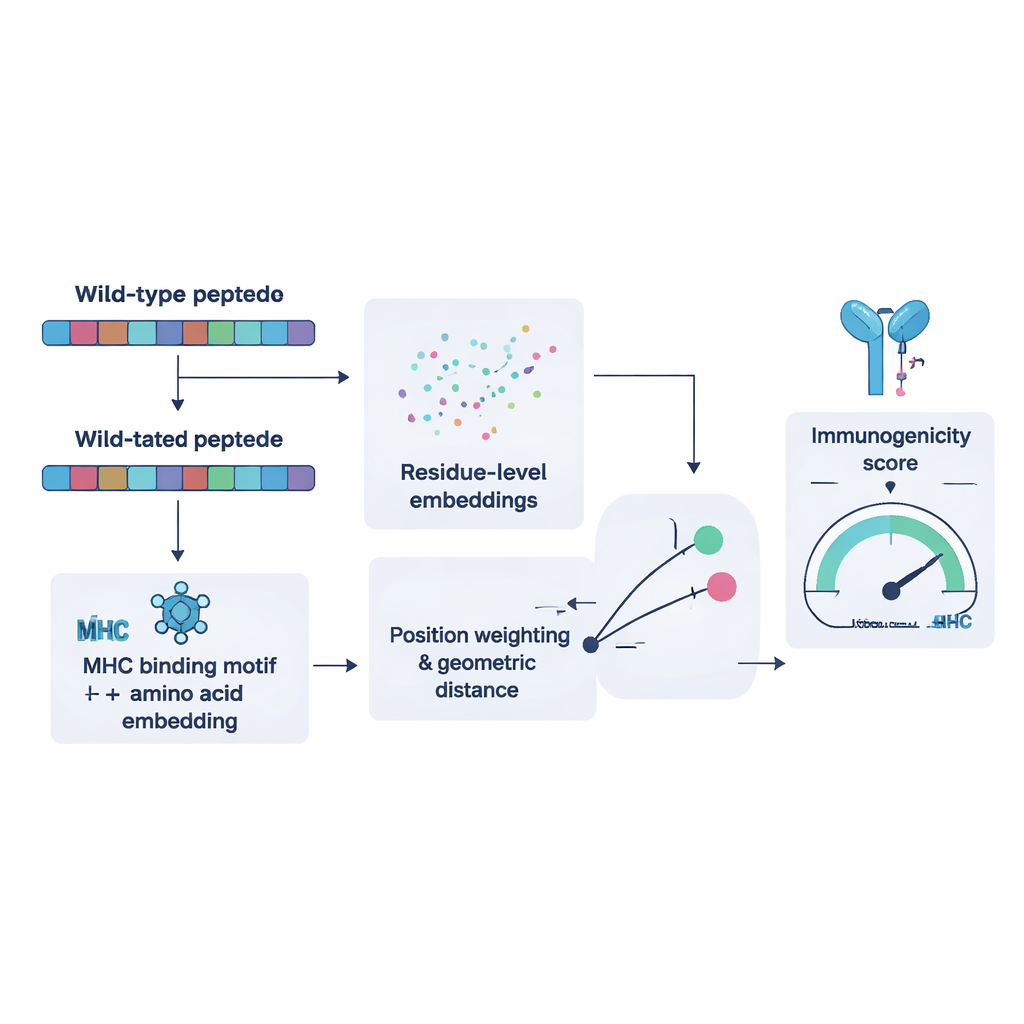
Ensinando um computador ao que as células T “veem”
Para treinar o NeoPrecis-Immuno, os pesquisadores primeiro reuniram milhares de exemplos em que a mesma célula T reconhece múltiplos peptídeos semelhantes e outros que não reconhece. Eles usaram esses exemplos para ensinar ao modelo que fragmentos mutantes muito semelhantes aos normais têm menos probabilidade de desencadear um ataque imunológico, porque alvos semelhantes ao self geralmente são filtrados durante o desenvolvimento das células T. O modelo representa cada peptídeo como um ponto em um espaço matemático moldado tanto pela sequência de aminoácidos quanto pelas preferências de ligação das moléculas de MHC da pessoa. Em seguida, mede quão distante o peptídeo mutante está do original. Distâncias maiores, informadas por motivos (motifs), correspondem a uma maior chance de ser imunogênico. Quando testado contra ferramentas existentes em conjuntos de dados independentes de câncer, o NeoPrecis-Immuno igualou ou superou essas ferramentas, especialmente ao trabalhar com MHC classe II, que apresenta antígenos às células T auxiliares que apoiam e sustentam respostas antitumorais.
Das mutações individuais ao tumor inteiro
Mutations individuais são apenas parte da história; a forma como elas se distribuem dentro do tumor também importa. Algumas mutações são “clonais”, encontradas em quase todas as células cancerosas, enquanto outras são “subclonais”, presentes apenas em bolsões específicos. O NeoPrecis constrói uma “paisagem de neoantígenos” somando suas pontuações de imunogenicidade ao longo das mutações e acrescentando informações sobre a quais subclones elas pertencem e quão comuns esses subclones são. Isso produz pontuações em nível tumoral que destacam cânceres ricos em neoantígenos fortes e amplamente compartilhados — especialmente aqueles que podem ser apresentados tanto em MHC classe I quanto em MHC classe II e potencialmente desencadear respostas coordenadas de células T auxiliares e citotóxicas. Em grupos de pacientes com melanoma e câncer de pulmão de não pequenas células tratados com inibidores de checkpoint, essas pontuações baseadas no NeoPrecis separaram com mais precisão respondedores de não-respondedores do que as contagens padrão de mutações, sendo particularmente úteis em tumores pulmonares complexos e heterogêneos.
O que isso significa para os pacientes
Para os pacientes, a promessa do NeoPrecis é um pareamento mais preciso das imunoterapias com aqueles que têm maior probabilidade de se beneficiar, e uma compreensão mais clara de por que alguns tumores resistem ao tratamento. Ao focar na qualidade e na distribuição dos neoantígenos — e não apenas na quantidade — o quadro ajuda a explicar por que tumores com cargas mutacionais semelhantes podem se comportar de maneira muito diferente. No futuro, mapas tão detalhados da paisagem imunovisível de um tumor poderiam orientar não só o uso de inibidores de checkpoint, mas também o desenho de vacinas contra o câncer personalizadas que priorizem os alvos mais potentes e amplamente compartilhados dentro do câncer de cada pessoa.
Citação: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
Palavras-chave: imunoterapia do câncer, neoantígenos, heterogeneidade tumoral, inibidores de checkpoint, oncologia computacional