Clear Sky Science · pt
NR6A1 é essencial para a especificação, formação e sobrevivência das células da crista neural
Como decisões celulares precoces moldam o rosto e o corpo
Antes de nascermos, um grupo especial de células chamado de células da crista neural migra pelo embrião para ajudar a construir o rosto, o coração, os nervos e outras estruturas. Quando essas células falham em seu desenvolvimento, bebês podem nascer com defeitos congênitos graves. Este estudo revela um interruptor molecular até então pouco valorizado — uma proteína chamada NR6A1 — que ajuda a determinar quando e onde as células da crista neural se formam em embriões de mamíferos, e o que acontece quando esse interruptor falha.
Os construtores errantes do embrião
As células da crista neural surgem muito cedo no desenvolvimento, ao longo da borda do tecido em formação que dará origem ao cérebro e à medula espinhal. Depois de se separarem desse tecido, elas migram por longas distâncias para criar muitas estruturas diferentes, desde ossos e cartilagens faciais até partes do sistema nervoso periférico e células pigmentares da pele. Como contribuem para tantos órgãos, mesmo pequenas interrupções em sua formação podem causar condições de amplo espectro conhecidas como neurocristopatias, incluindo síndromes craniofaciais como a de Treacher Collins. Entender como essas células aparecem pela primeira vez é, portanto, central para explicar tanto o desenvolvimento normal quanto os defeitos congênitos.
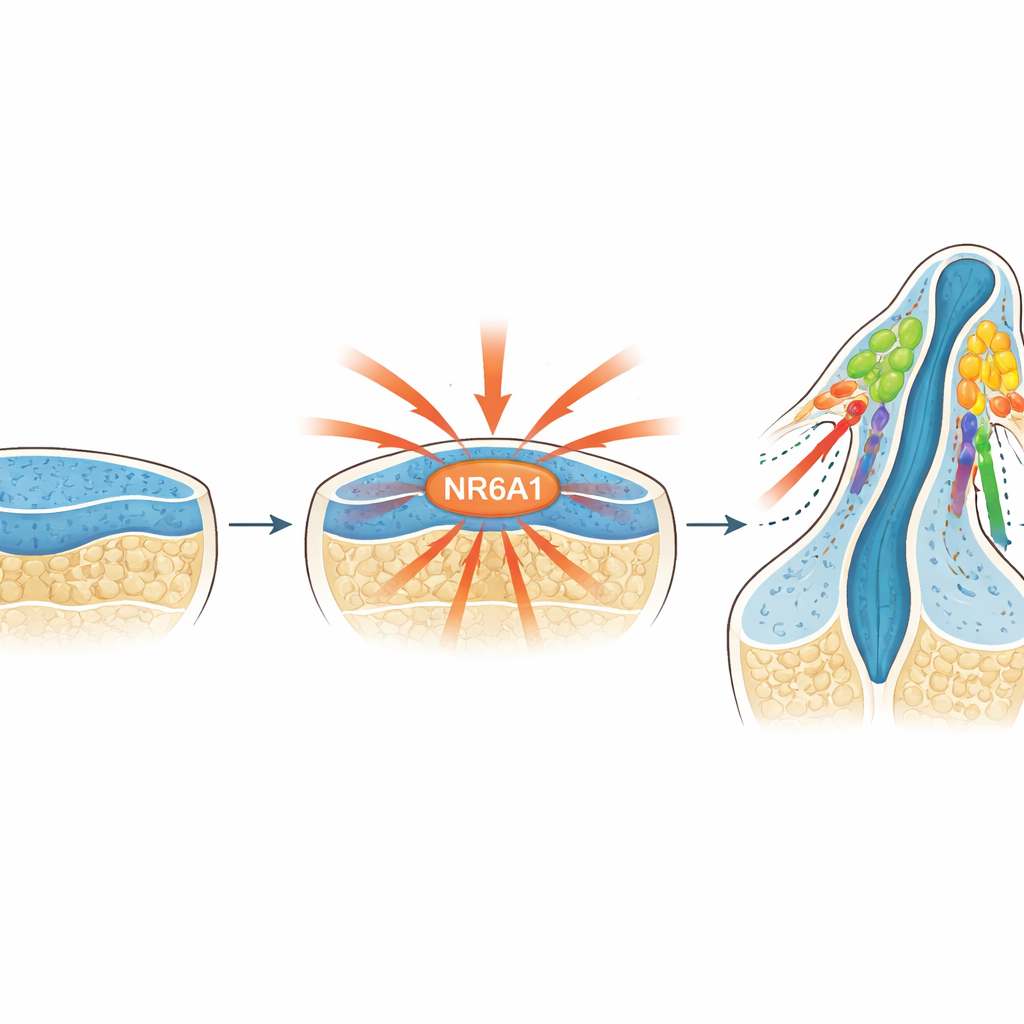
Um interruptor mestre recém-reconhecido
Os pesquisadores se concentraram em NR6A1, um membro da família dos receptores nucleares de proteínas que controlam a atividade gênica. Trabalhos anteriores sugeriam que NR6A1 poderia estar envolvido em defeitos de cabeça e face, mas seu papel nas células da crista neural era desconhecido. Ao rastrear NR6A1 em embriões de camundongo desde logo após a implantação, a equipe descobriu que sua presença correspondia de perto a onde e quando as células da crista neural normalmente nascem: aparece no tecido neural inicial, concentra-se ao longo do lado dorsal (posterior) do cérebro e da medula em desenvolvimento, e também é visto nas células exatamente quando elas deixam esse tecido para começar a migrar.
O que acontece quando o interruptor está ausente
Camundongos totalmente desprovidos de NR6A1 morrem cedo durante o desenvolvimento, então a equipe examinou embriões pouco antes desse ponto. Observaram uma escassez severa de células da crista neural, particularmente atrás do primeiro arco que formará partes da mandíbula e do pescoço, onde as células migratórias da crista neural estavam quase totalmente ausentes. Programas gênicos-chave que normalmente marcam a identidade da crista neural e permitem que as células se desprendam e se movam estavam fortemente reduzidos. Ao mesmo tempo, genes que mantêm as células em um estado semelhante a células-tronco, altamente proliferativo, permaneceram ligados, e muitas das células com perfil semelhante ao da crista neural que se formaram logo morreram. Esses achados indicam que, sem NR6A1, células-tronco neurais falham em fazer a transição adequada para células migratórias da crista neural e não conseguem sobreviver.
Desligando a pluripotência e ligando o movimento
Para entender como NR6A1 exerce esse controle, os autores combinaram várias técnicas moleculares poderosas, incluindo sequenciamento de RNA de célula única, mapeamento da acessibilidade da cromatina e ensaios direcionados de ligação DNA–proteína em células da crista neural derivadas de camundongo e de células-tronco humanas. Eles descobriram que NR6A1 se liga fisicamente a motivos específicos de DNA próximos a genes que regulam dois programas opostos: um que mantém a pluripotência (a capacidade de se tornar muitos tipos celulares) e outro que impulsiona a identidade da crista neural e o movimento celular. Quando NR6A1 está presente, a cromatina em torno de genes de “stemness” como Oct4 e Nanog torna-se menos acessível e esses genes são reprimidos, enquanto regiões próximas a genes da crista neural e da transição epitélio-mesênquima tornam-se mais abertas e ativas. A superexpressão de Oct4 durante a janela crítica de formação da crista neural imitou a perda de NR6A1, mostrando ainda que a pluripotência deve ser silenciada para que as células da crista neural emergam.
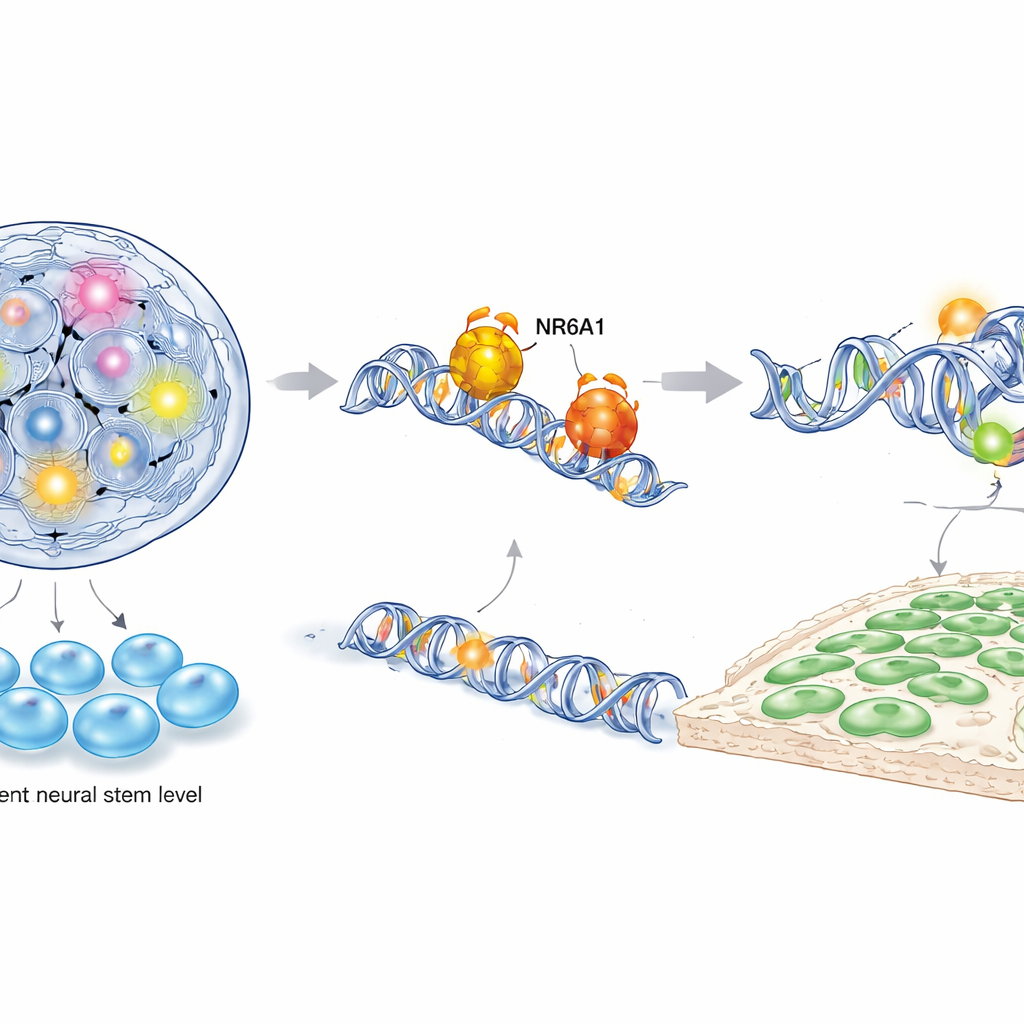
Reescrevendo a linha do tempo do desenvolvimento precoce
O estudo também revisa o calendário de quando as células da crista neural começam a ser especificadas em mamíferos. Usando um sistema genético induzível para remover NR6A1 em tempos diferentes, a equipe mostrou que deletá-lo até meados da gastrulação — um estágio anterior ao tradicionalmente pensado — foi suficiente para bloquear a ativação de genes da crista neural. Em contraste, excluir NR6A1 mais tarde, inclusive com uma linhagem amplamente usada que dirige especificamente a crista neural, não produziu defeitos óbvios. Isso significa que decisões cruciais sobre o destino da crista neural são tomadas antes que essas ferramentas padrão comecem a atuar, explicando por que alguns estudos anteriores em camundongos podem ter perdido requisitos iniciais.
Por que isso importa para defeitos congênitos e doenças
Em conjunto, o trabalho revela NR6A1 como um coordenador central que ajuda células-tronco neurais a “amadurecer” em células da crista neural ao desligar simultaneamente programas de pluripotência e ativar programas de migração e sobrevivência. Essa ação dupla parece começar durante a metade da gastrulação, mais cedo do que se reconhecia em mamíferos, e aproxima o desenvolvimento do camundongo ao de outros vertebrados. Ao esclarecer quando e como esse interruptor opera, o estudo fornece um quadro para reinterpretar experimentos genéticos anteriores, identificar melhores ferramentas para estudar a biologia da crista neural e, em última instância, entender e potencialmente prevenir neurocristopatias que surgem quando essa decisão precoce de desenvolvimento dá errado.
Citação: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
Palavras-chave: células da crista neural, NR6A1, desenvolvimento embrionário, mudança de pluripotência, neurocristopatia