Clear Sky Science · pt
Engenharia do sistema MmeFz2-ωRNA para edição genômica eficiente por meio de uma estrutura integrada computacional-experimental
Tesouras Gênicas Menores para Grandes Problemas Médicos
A edição gênica já transformou a forma como cientistas estudam doenças, mas convertê-la em medicina segura e prática continua sendo um grande desafio. Um obstáculo importante é que as “tesouras” de DNA mais potentes atualmente, como o CRISPR-Cas9, são fisicamente grandes e difíceis de embalar nos pequenos vetores de entrega usados em pacientes. Este estudo apresenta uma nova ferramenta compacta de edição gênica construída a partir de uma família pouco conhecida de enzimas chamada Fanzor2 e mostra como a inteligência artificial pode redesenhá-la rapidamente em uma forte candidata para futuras terapias genéticas.
Uma Nova Classe de Editores Gênicos Compactos
A maioria dos editores genômicos atuais, como Cas9 e Cas12a, são proteínas volumosas compostas por mais de mil blocos construtores. Esse tamanho as torna difíceis de caber em vírus adeno-associados (AAVs), o principal sistema de entrega para terapias gênicas. Em contraste, proteínas Fanzor2 são muito menores e ocorrem naturalmente em eucariotos, o ramo da vida que inclui animais e humanos. Os autores concentraram-se em um membro dessa família, MmeFz2, que usa uma molécula curta de RNA chamada ωRNA para localizar e cortar sequências específicas de DNA. No papel, MmeFz2 parecia ideal para terapia: compacta e programável. Na prática, entretanto, sua atividade em células humanas era pífia, editando menos de um por cento dos sítios-alvo. A equipe então se propôs a transformar essa enzima de baixo rendimento em uma ferramenta prática.
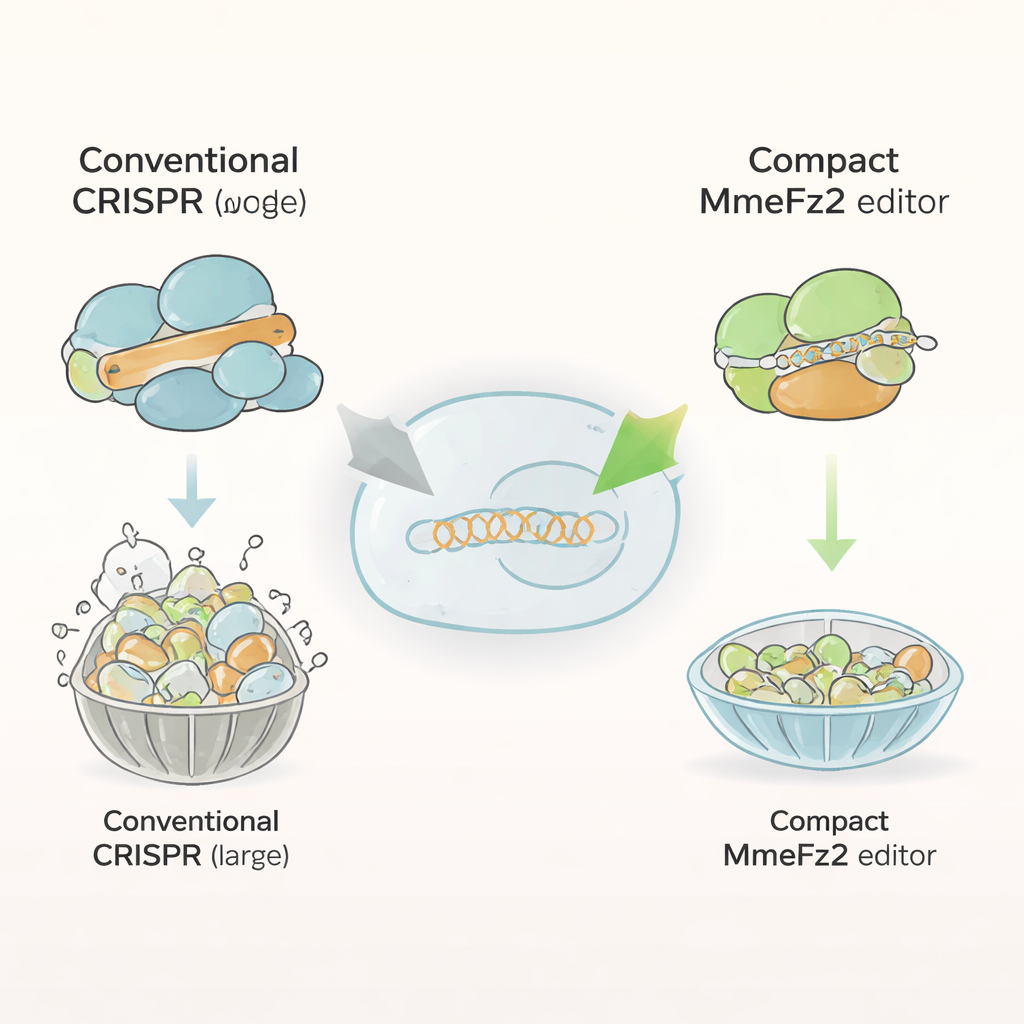
Usando IA para Redesenhar a Molécula Guia
O primeiro alvo foi a ωRNA, a guia que indica onde MmeFz2 deve cortar. Usando AlphaFold3, um programa de ponta que prevê estruturas 3D de complexos proteína–RNA–DNA, os pesquisadores construíram um modelo de MmeFz2 ligada à sua ωRNA e a um alvo de DNA. Essa estrutura virtual revelou que partes da ωRNA eram flexíveis, mal pareadas e pouco em contato com a proteína. Orientados por essa informação, a equipe substituiu sistematicamente ligações instáveis no RNA e removeu trechos de uridinas que podem interferir na transcrição. Em seguida testaram dezenas de variantes em células humanas. Ao combinar as melhores alterações e aparar uma região de haste desnecessária, eles criaram uma ωRNA encurtada que ficou 30% menor e, ainda assim, proporcionou um aumento próximo a 20 vezes na eficiência de edição em muitos sítios de DNA.
Ajustando a Proteína com Aprendizado de Máquina
Em seguida, a equipe refinou a própria proteína. Novamente usaram AlphaFold3 para mapear onde MmeFz2 tocava RNA e DNA e projetaram mais de cem mudanças de um único aminoácido visando fortalecer esses contatos ou melhorar a flexibilidade. Após rastrear essas variantes em células, alimentaram os dados de desempenho no EVOLVEpro, um sistema de aprendizado de máquina baseado em modelos de linguagem de proteínas treinados com milhões de sequências naturais. Essa ferramenta aprendeu quais características tendiam a aumentar a atividade e sugeriu novas combinações de mutações com previsão de desempenho ainda melhor. Por meio de algumas rodadas desse ciclo computacional–experimental, os cientistas chegaram a duas variantes enzimáticas otimizadas que, quando emparelhadas com a ωRNA melhorada, elevaram a atividade de edição em mais de 60 vezes em relação ao sistema inicial.
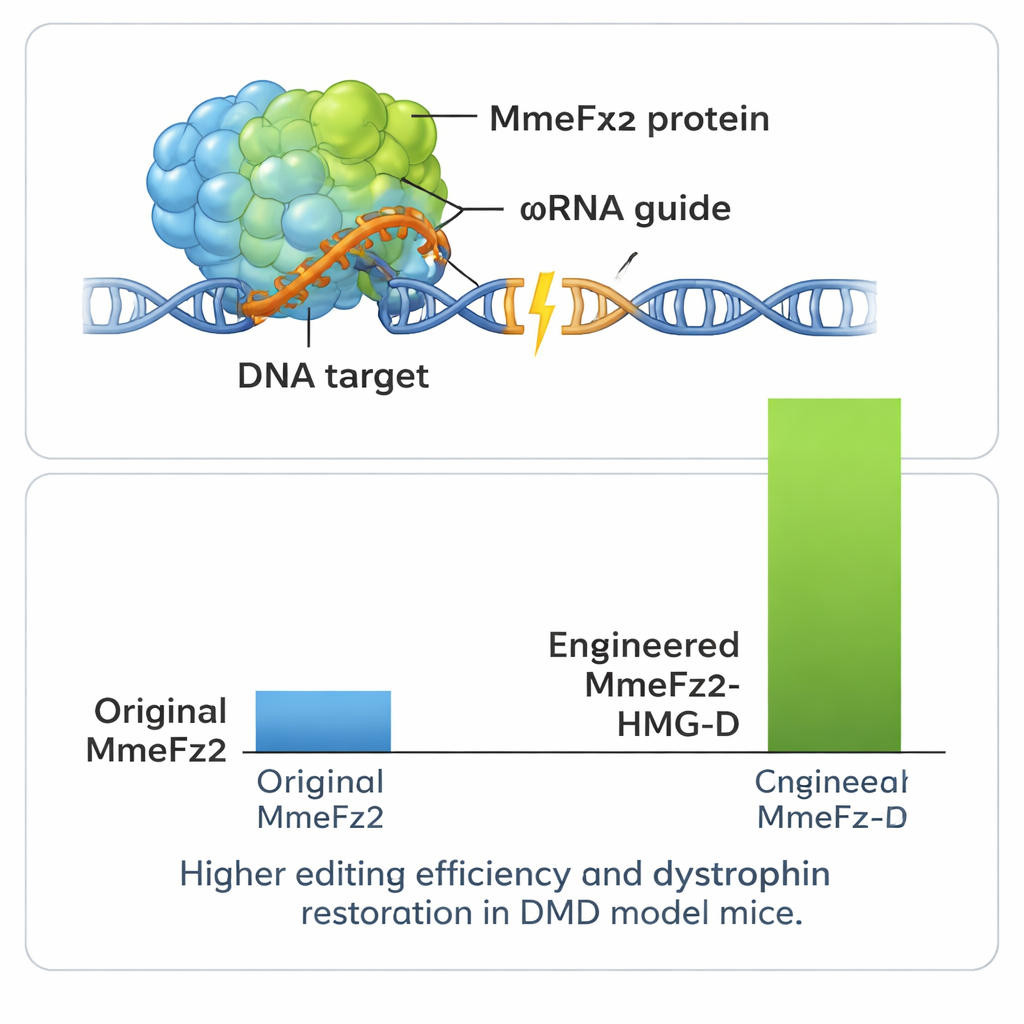
Aumentando a Potência e Testando em um Modelo de Doença
Para extrair ainda mais desempenho do sistema, os autores fundiram MmeFz2 a pequenos domínios de ligação ao DNA que ajudam proteínas a se fixar ao material genético. Um desses, chamado HMG-D, mostrou-se especialmente eficaz quando anexado à extremidade da enzima projetada, produzindo níveis de edição acima de 80% em alguns sítios. Importante: testes em locais de efeito fora do alvo previstos no genoma mostraram que esse poder adicional não veio com perda significativa de precisão. Como o editor gênico inteiro — incluindo proteína e RNA guia — é tão compacto, ele cabe confortavelmente em um único vetor AAV, algo que não é possível para a maioria dos sistemas CRISPR. A equipe aproveitou essa vantagem em um modelo de camundongo da distrofia muscular de Duchenne, uma doença letal que causa desgaste muscular devido a erros no gene da distrofina. Uma injeção única do editor entregue por AAV no músculo da perna levou a correções detectáveis no RNA do gene e restaurou a proteína distrofina em uma fração substancial das fibras musculares.
O Que Isso Significa para Futuras Terapias Gênicas
Para não especialistas, a mensagem-chave é que os autores transformaram uma enzima de corte gênico fraca e obscura em um editor compacto e de alto desempenho que pode ser entregue em um único pacote viral e pode reparar uma doença genética grave em um modelo animal realista. Igualmente importante é como eles chegaram lá: ao combinar de forma estreita predição estrutural baseada em IA e aprendizado de máquina com testes laboratoriais focados, melhoraram tanto a proteína quanto seu RNA guia de forma muito mais eficiente do que abordagens tradicionais de tentativa e erro. Essa estratégia integrada pode acelerar a criação de muitos editores genômicos de próxima geração, aproximando terapias gênicas mais precisas e seguras de pacientes com distrofia muscular e outras doenças hereditárias.
Citação: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Palavras-chave: edição gênica, alternativas ao CRISPR, distrofia muscular de Duchenne, terapia gênica viral, inteligência artificial na biologia