Clear Sky Science · pt
Nanorrobôs camuflados miram e regulam padrões de comunicação entre organelas subcelulares de macrófagos para promover a regeneração neural
Por que pequenos “ajudantes” camuflados importam para lesões da medula
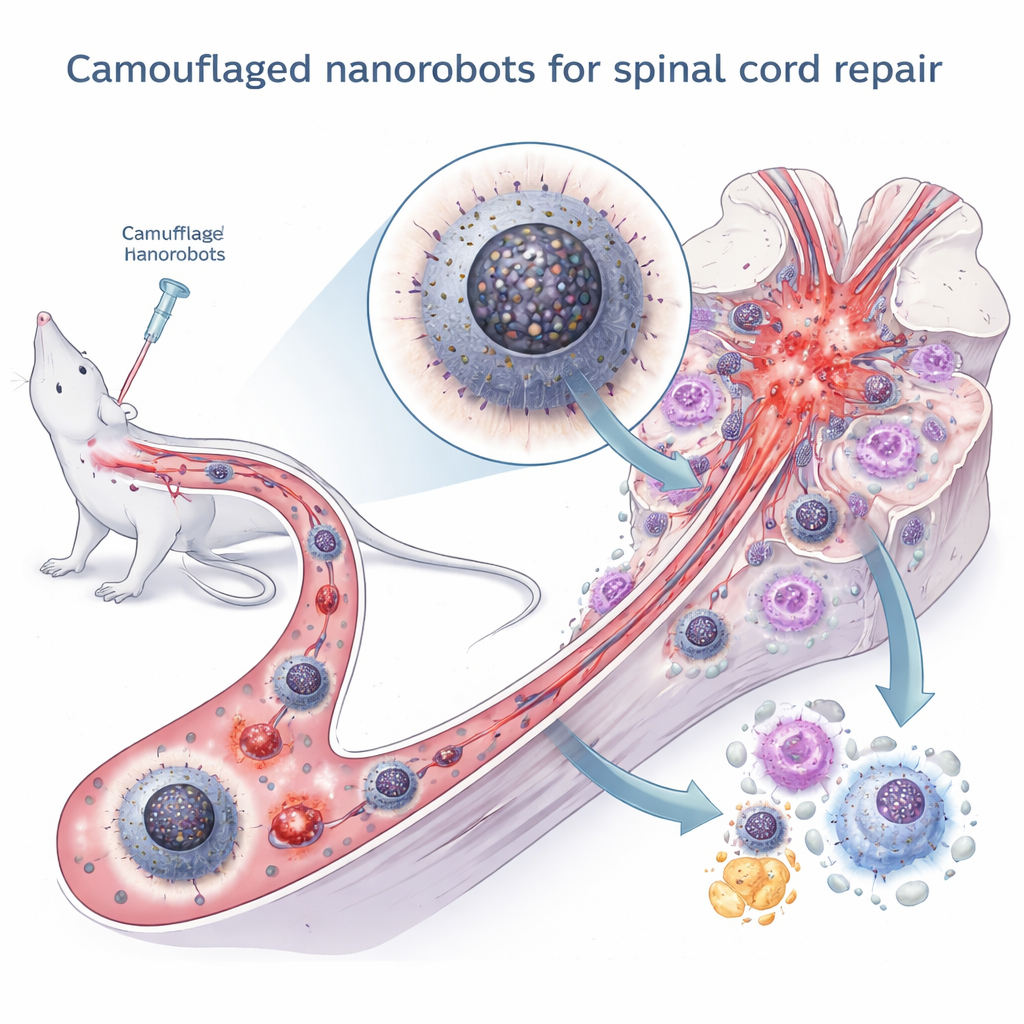
A lesão da medula espinhal frequentemente resulta em paralisia permanente porque o tecido nervoso danificado é extremamente difícil de reparar. Um dos motivos principais é que o local da lesão se torna uma zona hostil repleta de inflamação e estresse celular que bloqueia a cicatrização. Este estudo descreve um novo tipo de nanorrobô camuflado que circula pela corrente sanguínea, passa despercebido pelas defesas do corpo e reprograma células imunes no local da lesão para mudarem do modo de ataque para o modo de reparo, ajudando os nervos a reganhar crescimento em animais com dano na medula espinhal.
O problema: inflamação que não se desliga
Após uma lesão da medula espinhal, a primeira onda de dano vem do próprio trauma físico. Mas uma segunda onda, mais lenta, é conduzida por inflamação, moléculas tóxicas chamadas espécies reativas de oxigênio e morte celular generalizada. Células imunes conhecidas como macrófagos correm para limpar os detritos. No início, elas adotam um estado agressivo “M1” que mata patógenos e células danificadas, mas também libera sinais inflamatórios intensos. Para que a cura verdadeira comece, essas mesmas células devem depois migrar para um estado mais calmo, “M2”, que apoia o reparo tecidual, o crescimento de vasos sanguíneos e a regeneração nervosa. Infelizmente, o estresse intenso dentro do tecido lesionado pode aprisionar os macrófagos no estado M1 prejudicial, consolidando um ciclo de inflamação crônica que impede a recuperação funcional.
Conversa oculta entre partes da célula
Os autores concentraram-se em uma “conversa” interna sutil, porém crucial, dentro dos macrófagos: a comunicação entre dois compartimentos-chave, o retículo endoplasmático (que auxilia na dobragem de proteínas e armazena cálcio) e as mitocôndrias (as usinas energéticas da célula). Em condições normais, essas estruturas compartilham pequenas quantidades de íons de cálcio através de zonas de contato especializadas, ajudando a ajustar a produção de energia às necessidades da célula. Após a lesão, porém, o excesso de espécies reativas de oxigênio provoca má-dobragem proteica e estresse no retículo endoplasmático. Esse estresse, por sua vez, impulsiona a transferência excessiva de cálcio para as mitocôndrias, levando ao colapso energético, ao aumento de moléculas tóxicas e ao vazamento de DNA mitocondrial para o fluido intracelular. Esse DNA escapado ativa uma potente via de alarme chamada cGAS–STING–NFκB, que mantém os macrófagos no estado inflamatório M1.
Projetando um nanorrobô camuflado
Para quebrar esse ciclo vicioso, a equipe construiu um nanorrobô multicamadas chamado BP@D/N. No núcleo estão pontos quânticos de fósforo negro, partículas minúsculas com forte atividade antioxidante e anti-inflamatória, mas com baixa estabilidade no organismo. Esses pontos são encapsulados em uma concha oca de polidopamina, um material biocompatível que os protege de se degradarem cedo demais e acrescenta suas próprias propriedades antioxidantes. Finalmente, toda a partícula é revestida com uma membrana retirada de neutrófilos ativados, um tipo de glóbulo branco naturalmente atraído por sítios de inflamação. Essa “camuflagem” permite que o nanorrobô evite a depuração imune, siga sinais inflamatórios até a medula lesionada e se fixe aos macrófagos para uma captação eficiente.
Reconectando células imunes estressadas
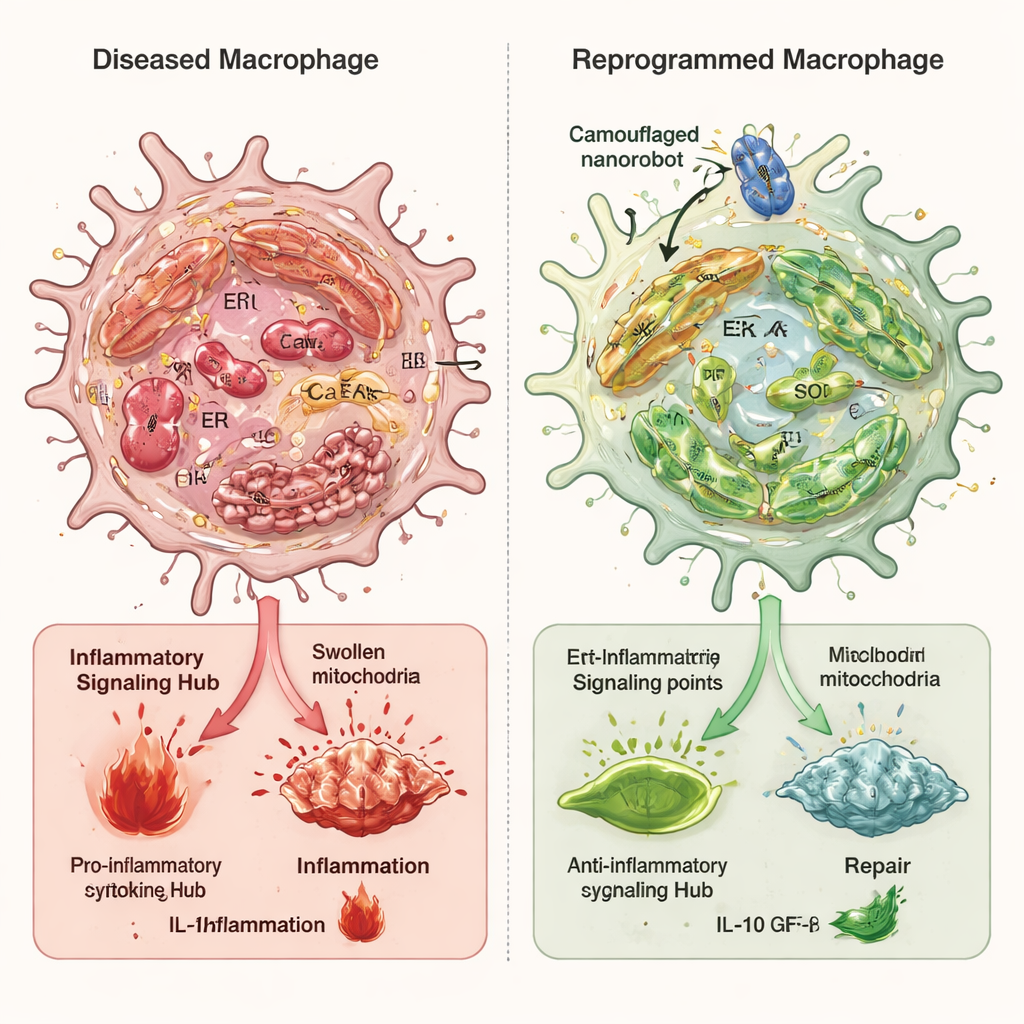
Em estudos celulares, macrófagos expostos a gatilhos inflamatórios mostraram altos níveis de estresse do retículo endoplasmático, mitocôndrias inchadas e danificadas, sobrecarga de cálcio e forte ativação da via de alarme cGAS–STING–NFκB. Quando tratados com os nanorrobôs camuflados, o estresse oxidativo geral caiu acentuadamente, as membranas internas entre retículo endoplasmático e mitocôndrias ficaram menos hiperconectadas e o cálcio mitocondrial retornou a níveis próximos do normal. Isso evitou o vazamento de DNA mitocondrial para o fluido celular e atenuou a cascata de sinalização inflamatória. Um componente chave nesse processo foi uma enzima chamada Ero1α, que ajuda a controlar o ambiente oxidativo e a liberação de cálcio do retículo endoplasmático. Os nanorrobôs reduziram a atividade de Ero1α, e quando os pesquisadores aumentaram artificialmente a Ero1α, isso cancelou em grande parte os benefícios do nanorrobô, confirmando seu papel central.
De acalmar a inflamação a reganhar nervos
Essas mudanças internas converteram os macrófagos do estado destrutivo M1 para o estado reparador M2. Em culturas celulares, as células enviesadas para M2 secretaram menos moléculas inflamatórias como TNF-α e IL-6 e mais fatores de crescimento que incentivam neurônios e células de suporte a crescer e estender axônios. Em modelos de rato com lesão medular, injeções repetidas dos nanorrobôs reduziram sinais imunes danosos na lesão, diminuíram a formação de cicatriz, reduziram a formação de cavidades e aumentaram fibras nervosas em regeneração. Animais que receberam os nanorrobôs camuflados recuperaram melhor o movimento dos membros posteriores, respostas musculares mais fortes e melhor estrutura vesical em comparação com tratamentos sem nanopartículas ou menos direcionados.
O que isso pode significar para pacientes futuros
Este trabalho mostra que ajustar com precisão o estresse interno e a comunicação entre compartimentos celulares pode transformar células imunes de prejudiciais em benéficas para nervos danificados. Ao embalar partículas antioxidantes potentes, porém frágeis, em um nanorrobô camuflado e direcionado, os pesquisadores restauraram um equilíbrio mais saudável entre inflamação e reparo na medula lesionada de ratos. Embora ainda falte muito trabalho antes que essa abordagem possa ser testada em humanos, ela oferece um roteiro promissor: em vez de apenas suprimir a inflamação de forma ampla, terapias futuras podem direcionar máquinas celulares específicas dentro dos macrófagos para criar um ambiente mais receptivo à regeneração neural após lesão medular.
Citação: Guo, Q., Wang, W., Jiang, X. et al. Camouflaged nanorobots target and regulate macrophage subcellular organelle crosstalk patterns to promote neural regeneration. Nat Commun 17, 1952 (2026). https://doi.org/10.1038/s41467-026-68636-5
Palavras-chave: lesão da medula espinhal, nanorrobôs, macrófagos, regeneração neural, nanomedicina