Clear Sky Science · pt
Caracterização metabólica das interações tumor-imune por imunofluorescência multiplexada revela mecanismos espaciais de resposta à imunoterapia no carcinoma de pulmão não pequenas células (CPNPC)
Por que esta pesquisa importa
A imunoterapia transformou o tratamento de algumas pessoas com câncer de pulmão avançado, mas a maioria dos pacientes ainda vê seu câncer progredir apesar desses medicamentos poderosos. Este estudo faz uma pergunta simples, porém crucial: podemos observar mais de perto o próprio tecido tumoral — onde diferentes células se localizam e quanta energia elas consomem — para prever quem realmente se beneficiará da imunoterapia? Ao transformar pequenas amostras de biópsia em mapas celulares detalhados, os pesquisadores pretendem aproximar o cuidado do câncer de pulmão de uma abordagem genuinamente personalizada.
Olhando dentro dos tumores pulmonares como um mapa de cidade
A equipe examinou tecido de 55 pessoas com carcinoma de pulmão não pequenas células (CPNPC) avançado tratadas com inibidores de pontos de controle imunológico, uma grande classe de drogas imunoterápicas. Antes do tratamento, as amostras tumorais foram coradas com um painel de 44 marcadores usando imunofluorescência multiplexada, permitindo visualizar muitas proteínas ao mesmo tempo. Um sistema de aprendizado profundo então identificou tipos celulares-chave — como células tumorais, células T, células B, macrófagos e fibroblastos — e classificou seu estado funcional (por exemplo, ativadas, em divisão ou exauridas), bem como seu perfil metabólico, ou seja, como produziam e utilizavam energia. Em vez de apenas contar células, os pesquisadores também mapearam onde as células estavam em relação umas às outras, criando regiões semelhantes a bairros dentro de cada biópsia.
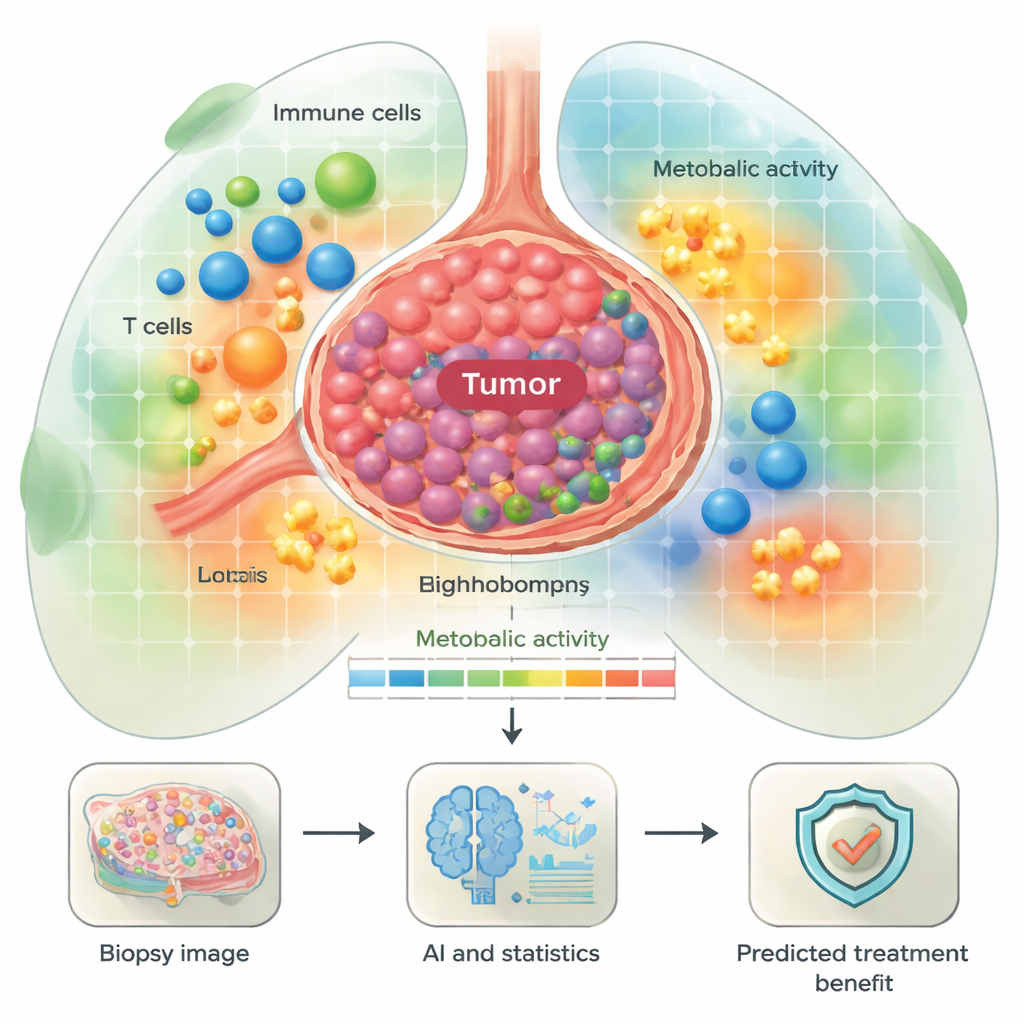
Tumores ávidos por energia e seu entorno imune
Um foco principal foi o metabolismo — as formas pelas quais as células geram combustível para crescer ou combater doenças. Os pesquisadores definiram "bairros metabólicos" com diferentes níveis e tipos de uso de energia, desde atividade baixa até zonas altamente ativas ricas em fosforilação oxidativa e glicólise. Eles descobriram que tanto as células tumorais quanto certas células imunes, como macrófagos, frequentemente exibiam vias de produção de energia intensas. Alguns desses padrões se relacionaram com desfechos dos pacientes. Por exemplo, tumores com alta atividade em vias que os ajudam a utilizar aminoácidos e executar o ciclo do TCA tenderam a pertencer a pacientes que recaíram precocemente após a imunoterapia. Em contraste, alguns plasmócitos (células B produtoras de anticorpos) com vias energéticas ativas dentro do tumor eram mais comuns em pacientes que tiveram melhor evolução, sugerindo que nem todas as células energéticas são prejudiciais — algumas podem apoiar uma imunidade antitumoral eficaz.
Jogadores imunes bons e ruins na paisagem tumoral
Além da simples abundância, o tipo e o comportamento das células imunes também importaram. Macrófagos que carregavam a molécula citotóxica granzima B se associaram fortemente a pior sobrevida livre de progressão, especialmente quando encontrados em bairros metabolicamente baixos ou inativos. Essas regiões podem representar áreas pobres em nutrientes ou dormentes onde o ataque imune é enfraquecido. Em contraste, certos arranjos de células T reguladoras (Tregs) e fibroblastos na fronteira entre o tumor e o tecido circundante pareceram estar ligados a melhores desfechos, possivelmente refletindo um padrão em que células supressoras ficam retidas nas bordas em vez de infiltrarem profundamente o tumor. Razões entre diferentes células imunes, como granulócitos em relação a células T CD8, também se correlacionaram com a resposta, ressaltando que o equilíbrio e o posicionamento imune, e não apenas contagens totais, são importantes.
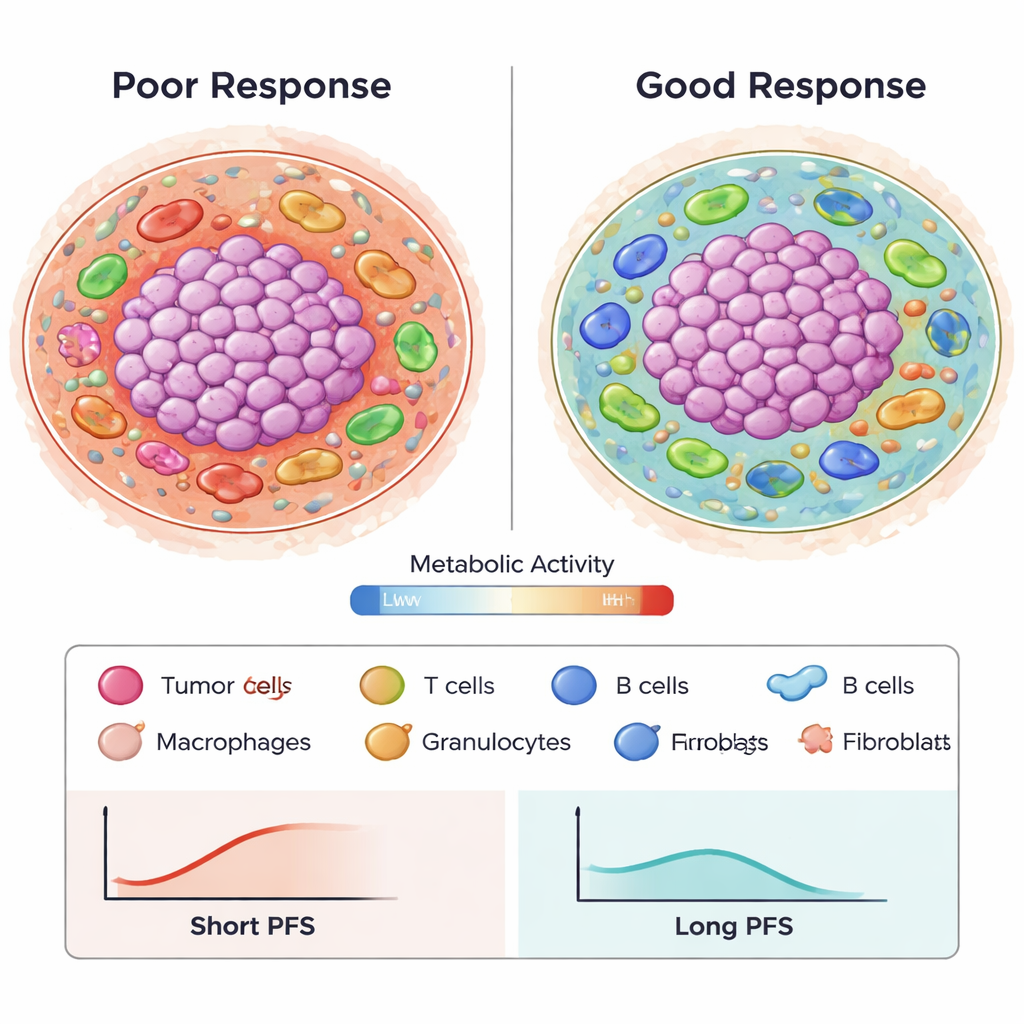
De imagens complexas a padrões preditivos
Para interpretar mais de um milhão de características espaciais engenheiradas descrevendo tipos celulares, distâncias e estados metabólicos, os autores usaram um método avançado de seleção de características (Stabl) e ferramentas de modelagem de sobrevivência. Eles identificaram 87 características-chave, muitas refletindo como células tumorais metabolicamente ativas interagem com macrófagos e células T, ou como tipos específicos de células imunes se agrupam perto de vasos sanguíneos e fibroblastos. Usando essas características em modelos de regressão de Cox, construíram um preditor que estimou a sobrevida livre de progressão com precisão (AUC) em torno de 0,8 ao longo de 24 meses, superando marcadores tradicionais únicos como coloração de PD-L1 ou carga mutacional tumoral em trabalhos publicados anteriormente. Importante, várias características foram reproduzíveis em duas coortes de pacientes independentes, sugerindo que os padrões não são apenas ruído aleatório.
O que isso significa para os pacientes
Para um leigo, a mensagem principal é que onde as células se situam em um tumor pulmonar e como elas se energizam pode ajudar a explicar por que alguns pacientes respondem bem à imunoterapia enquanto outros não. Este estudo mostra que informações espaciais e metabólicas ricas a partir de uma biópsia rotineira, combinadas com inteligência artificial e modelagem estatística, podem revelar assinaturas de provável benefício ou resistência. Embora o trabalho precise de validação em grupos maiores e em seções de tecido inteiras, ele traça um caminho rumo a futuros testes que poderiam dizer aos médicos, antes do início do tratamento, quais pacientes têm maior probabilidade de obter controle duradouro com imunoterapia e quais podem precisar de estratégias alternativas ou combinadas.
Citação: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Palavras-chave: resistência à imunoterapia, câncer de pulmão não pequenas células, microambiente tumoral, biologia espacial, metabolismo do câncer