Clear Sky Science · pt
H3K9me2 mediada por G9a orquestra a regeneração epitelial intestinal por meio do silenciamento epigenético de genes relacionados ao ciclo celular
Por que a autorreparação intestinal é importante
Todos os dias, o revestimento do intestino enfrenta condições agressivas: ácido estomacal, partículas de alimento e trilhões de microrganismos. Ainda assim, esse tecido não só sobrevive como se repara constantemente. Quando esse sistema de reparo falha — após radioterapia, na doença inflamatória intestinal ou durante infecções severas — as pessoas podem sofrer dor, sangramento e complicações potencialmente fatais. Este estudo revela um “interruptor” oculto dentro das células intestinais que as ajuda a decidir quando parar de repousar e começar a reconstruir, oferecendo pistas para novos tratamentos que possam reforçar a equipe natural de reparo do intestino.
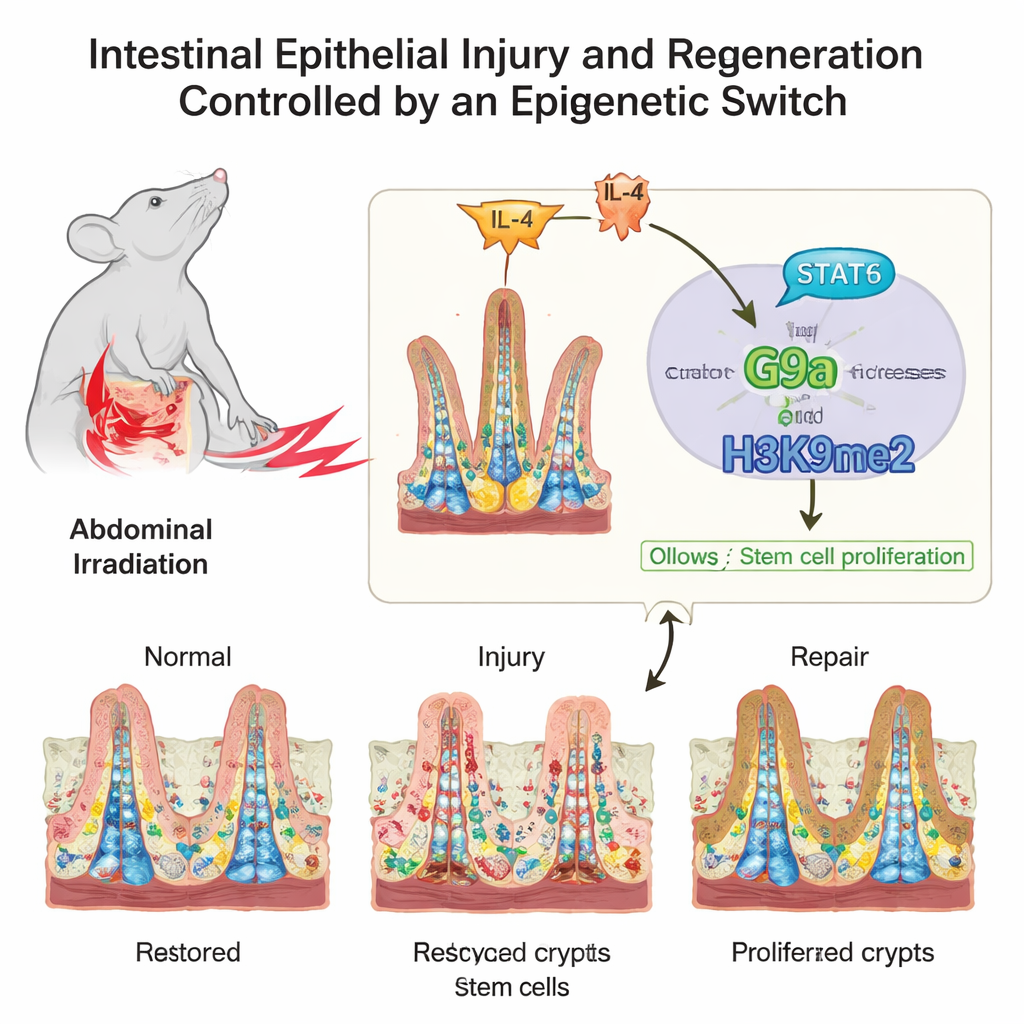
Uma arquitetura delicada sob estresse constante
A superfície interna do intestino parece um carpete felpudo ao microscópio, com vilosidades em forma de dedo que absorvem nutrientes e bolsas chamadas criptas onde vivem as células-tronco. Essas células-tronco e suas filhas de divisão rápida devem equilibrar renovação constante e reparo de emergência. Os autores concentraram-se em como marcas químicas nas proteínas que empacotam o DNA, chamadas histonas, influenciam esse equilíbrio. Essas marcas não mudam os genes em si, mas atuam mais como dimmers, regulando grupos de genes para cima ou para baixo à medida que o intestino passa da vida normal ao dano e volta à saúde.
Uma marca epigenética que acompanha dano e cura
Usando camundongos expostos à radiação — uma causa comum de lesão intestinal durante o tratamento do câncer — os pesquisadores mapearam várias marcas de histonas nas criptas ricas em células-tronco. Uma marca, conhecida como H3K9me2, aumentou acentuadamente quando o intestino transitou do dano para o reparo. Sua enzima escritora, uma proteína chamada G9a, seguiu o mesmo padrão. A equipe então examinou amostras humanas de pacientes que receberam radioterapia pélvica, assim como pessoas com doença de Crohn. Em ambos os contextos, níveis mais altos de H3K9me2 e G9a nas células intestinais correlacionaram-se com sinais melhores de reparo tecidual, sugerindo que esse sistema é conservado entre camundongos e humanos.
Quando o interruptor de reparo quebra
Para testar se essa marca é apenas coadjuvante ou realmente dirige a cicatrização, os cientistas removeram G9a especificamente do revestimento intestinal de camundongos ou bloquearam sua atividade com um fármaco. Em ambos os casos, os níveis de H3K9me2 caíram. Após radiação ou lesão química, esses camundongos perderam mais peso, tiveram intestinos mais curtos e danificados e mostraram menos criptas regenerativas e células-tronco do que animais normais. Mesmo sem lesão deliberada, o revestimento intestinal de camundongos deficientes em G9a parecia atrofiado: criptas mais rasas, vilosidades mais curtas e redução no número de células-tronco e seus descendentes especializados. Pequenos “mini-intestinos” cultivados a partir dessas células em placa também cresceram mal, destacando que esse sistema molecular é central para a renovação diária do intestino.
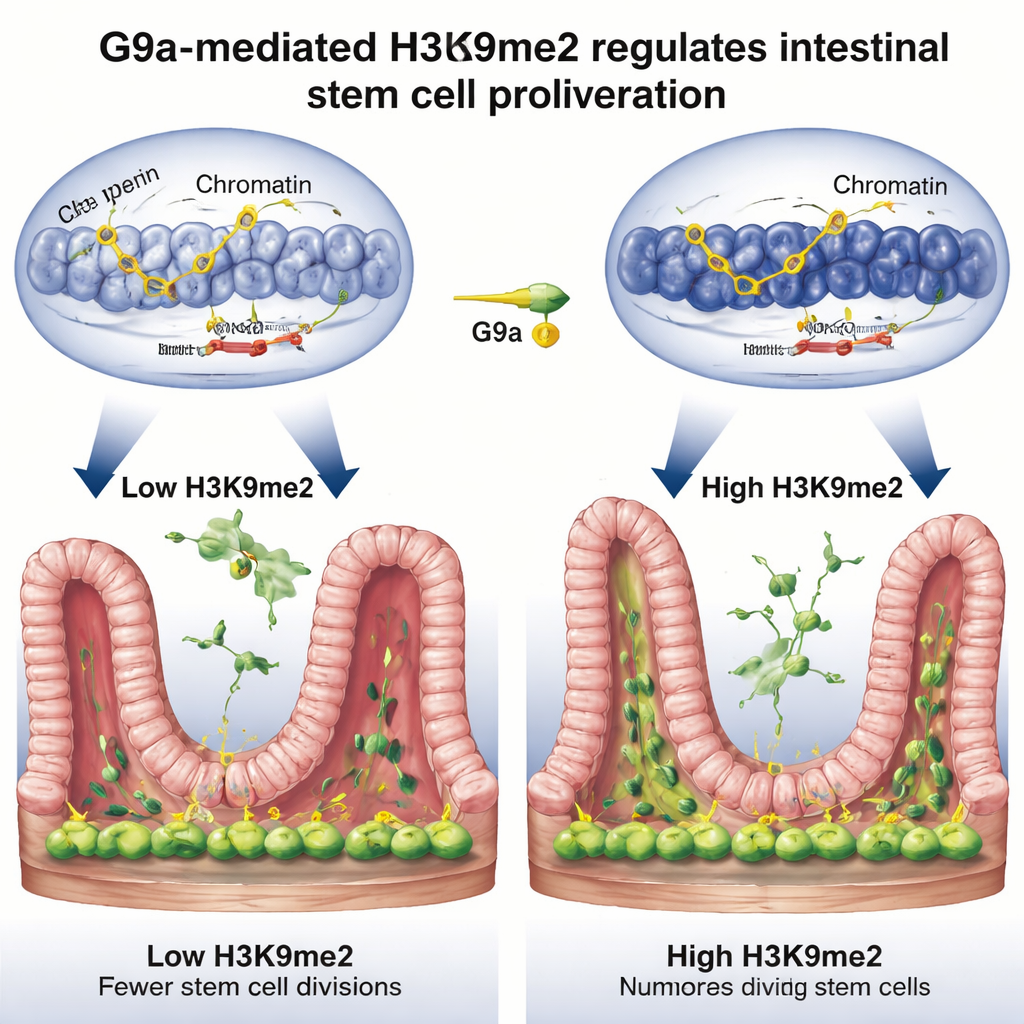
Soltando os freios da divisão celular
Aprofundando, a equipe investigou quais genes são controlados por esse interruptor de reparo. Ao combinar três poderosos métodos de genoma, eles descobriram que H3K9me2, instalada por G9a, tende a se localizar em trechos de DNA que normalmente atuam como freios do ciclo celular — genes como Rb1cc1, Rb1, Cdkn1a e Pten, que retardam ou interrompem a divisão celular. Quando G9a faltou, a marca química desapareceu dessas regiões, o DNA ao redor se abriu e esses genes-freio foram mais fortemente ativados, levando a uma proliferação mais lenta das células-tronco. Durante o reparo normal após lesão, os níveis de H3K9me2 nesses genes aumentaram, sua atividade diminuiu e as células-tronco ficaram mais livres para dividir-se e reconstruir o revestimento. Em essência, G9a e H3K9me2 silenciam temporariamente os sinais de “pare” para que o tecido possa regredir.
Uma cadeia de sinalização de pistas imunes ao reparo
O intestino não age sozinho; ele escuta continuamente sinais do sistema imune. Os pesquisadores rastrearam um desses sinais a montante de G9a. Após a lesão, os níveis do mensageiro imune IL‑4 aumentaram, desencadeando a ativação de uma proteína chamada STAT6 dentro das células intestinais. STAT6 ativado ligou-se diretamente à região de controle do gene G9a, aumentando sua produção. Isso criou uma cadeia de comando: IL‑4 ativa STAT6, STAT6 aumenta G9a, e G9a adiciona H3K9me2 para silenciar genes-freio do ciclo celular, permitindo que as células-tronco se expandam e restaurem o revestimento danificado.
O que isso significa para tratamentos futuros
Para um não especialista, essas descobertas mostram que o reparo intestinal é guiado não apenas pelos genes, mas por marcas químicas reversíveis que ajustam quando esses genes são usados. A via IL‑4–STAT6–G9a–H3K9me2 atua como um painel de controle interno que afrouxa os freios da divisão das células-tronco o tempo suficiente para curar e depois pode ser reajustada. No futuro, terapias que realcem suavemente essa via — como fármacos ou ferramentas baseadas em genes que elevem níveis de G9a no momento e local adequados — podem ajudar pacientes a se recuperar mais rapidamente de lesões por radiação, surtos de doença inflamatória intestinal ou outras condições que danificam o revestimento intestinal, minimizando os riscos de crescimento celular descontrolado.
Citação: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Palavras-chave: regeneração intestinal, epigenética, células-tronco, metilação de histonas, doença inflamatória intestinal