Clear Sky Science · pt
Sintetases de sinalização por quorum com dupla função DspII e DspI coordenam a mudança de virulência em Pseudomonas aeruginosa
Como um superbactéria hospitalar muda sua estratégia de ataque
Pseudomonas aeruginosa é um microrganismo notório em hospitais que pode causar infecções persistentes nos pulmões e em feridas, especialmente em pacientes vulneráveis. Ele sobrevive alternando entre dois estilos de vida: uma comunidade protegida e de crescimento lento chamada biofilme e uma forma móvel e agressiva que invade tecidos. Este estudo revela como a bactéria decide quando romper um biofilme de longa duração e desencadear um ataque agudo súbito, apontando potenciais pontos fracos para tratamentos futuros.
Uma vida microbiana entre se esconder e atacar
Muitas infecções bacterianas se desenvolvem em etapas. No início, células livres se espalham pelo corpo e usam armas potentes que danificam os tecidos do hospedeiro. Mais tarde, elas frequentemente se fixam em biofilmes — camadas espessas e viscosas aderidas a superfícies como cateteres, tecido pulmonar ou feridas. Nessas comunidades, as células ficam envoltas por uma matriz protetora que as torna difíceis de eliminar com antibióticos ou com defesas imunes. Ainda assim, biofilmes não são um beco sem saída. Células podem sair, recuperar motilidade e desencadear novas rodadas de infecção aguda em outros locais. Até agora, não estava claro como Pseudomonas aeruginosa coordena ativamente essa transição da persistência crônica de volta à doença agressiva.
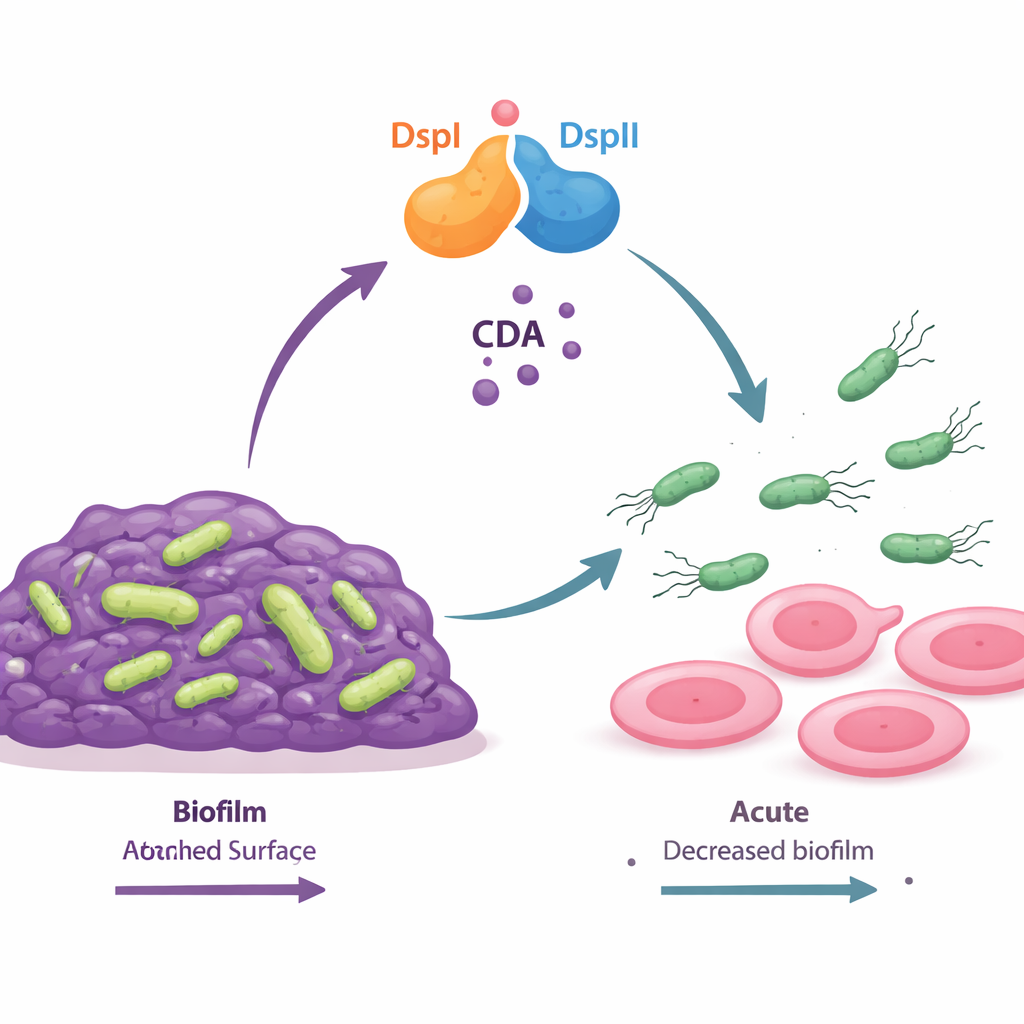
Um interruptor de duas proteínas que produz um sinal químico de “vai”
Os autores descobriram que duas proteínas bacterianas, chamadas DspI e DspII, atuam em conjunto como uma espécie de interruptor molecular. Ambas são enzimas do mesmo tipo geral e estão adjacentes no genoma bacteriano, sendo ativadas ao mesmo tempo conforme a população se densifica. Quando formam um par, elas produzem um pequeno ácido graxo sinalizador chamado cis-2-decanoico (CDA), parte de um grupo mais amplo de moléculas de comunicação conhecidas como sinais DSF. Bactérias mutantes sem DspI ou DspII não conseguiam mais produzir CDA, formavam biofilmes anormalmente espessos e perdiam a capacidade de se espalhar pela superfície. Apenas quando ambas as proteínas eram restauradas juntas as células recuperavam a produção normal do sinal, a dispersão do biofilme e a motilidade, mostrando que as duas enzimas funcionam como uma equipe interdependente.
Do sinal químico ao movimento e à fuga
CDA não age isoladamente; ele se conecta à rede interna da bactéria. A equipe mostrou que CDA reduz os níveis de outra molécula mensageira, o di-GMP cíclico, ao aumentar a atividade de uma enzima específica chamada RbdA, que degrada esse mensageiro. Altos níveis de di-GMP cíclico normalmente incentivam a formação de biofilmes ao estimular a produção de matriz rica em açúcares e suprimir os flagelos, as pequenas hélices que impulsionam a natação. Quando CDA está presente, os níveis de di-GMP cíclico caem, um regulador chamado FleQ muda o modo de atuação, a produção de polímeros pegajosos diminui e os flagelos são estendidos e reforçados. Como resultado, os biofilmes afrouxam e as células recuperam a capacidade de se mover, colonizando novos territórios.
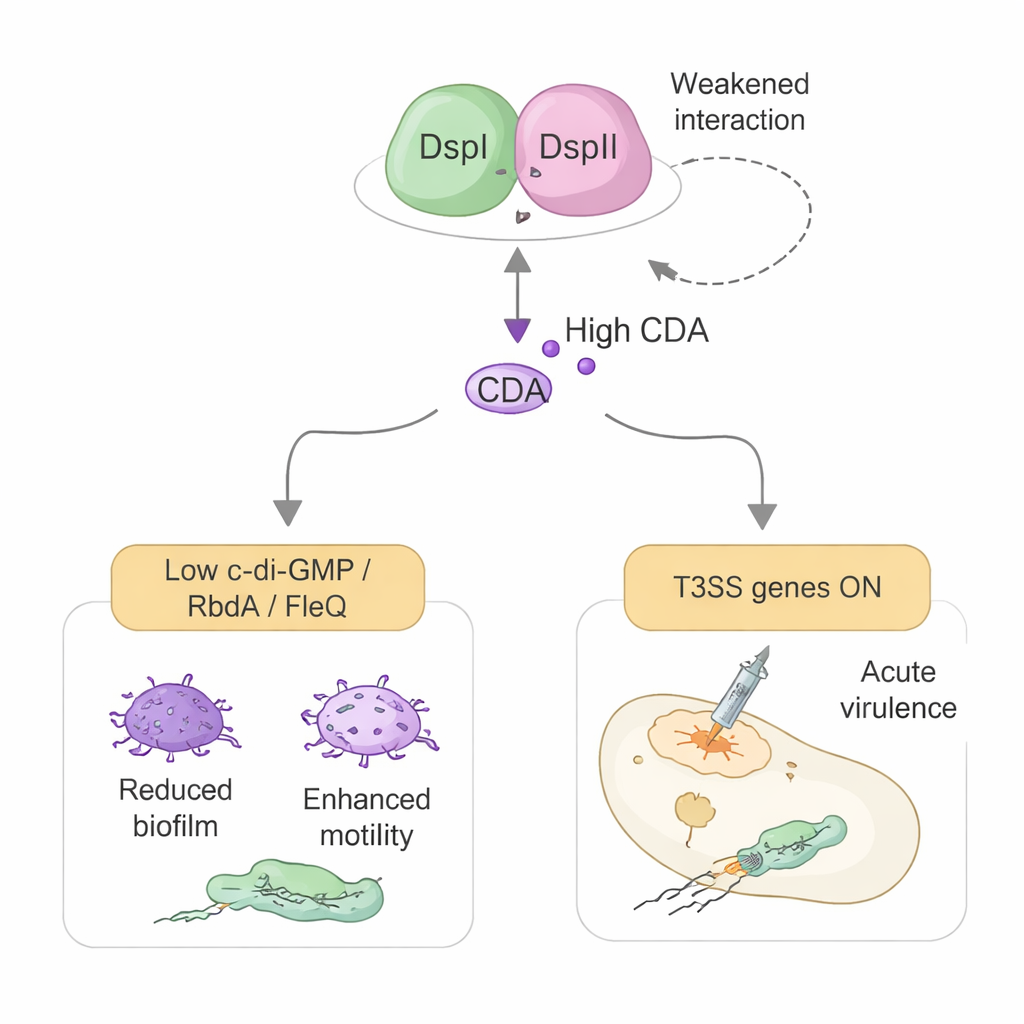
Reprogramando o sistema de armas bacteriano
O estudo também revela uma segunda função inesperada para DspI e DspII que vai além da química. O mesmo par de proteínas ajuda a ativar o sistema de secreção tipo III (T3SS) da bactéria, um aparelho em forma de seringa usado para injetar toxinas diretamente em células do hospedeiro. Em vez de atuar por meio do CDA, esse efeito ocorre por controle direto de chaves genéticas. DspI e DspII atenuam a produção de dois pequenos RNAs reguladores, RsmY e RsmZ, que normalmente reprimem a síntese de proteínas do T3SS. Eles fazem isso ligando-se à região de controle do DNA de um desses RNAs e interagindo fisicamente com um regulador mestre chamado GacA. Quando RsmY e RsmZ ficam sob controle, um ativador a montante chamado RsmA é liberado, e os genes do T3SS e seu controlador mestre ExsA são ligados, aumentando a citotoxicidade em cultura celular e a letalidade num modelo de infecção em inseto.
Um sistema autoajustável com alvos farmacológicos
Curiosamente, a força da parceria DspI–DspII e seu controle sobre a virulência são regulados pelos próprios níveis de CDA. Em concentrações baixas — como as esperadas em células prestes a sair de um biofilme — o CDA reforça a interação entre as duas proteínas e promove mais produção do sinal e ativação do T3SS. Em concentrações altas no interior de biofilmes densos, o CDA enfraquece essa interação e reduz a afinidade delas pelo DNA, limitando a síntese adicional do sinal e a produção cara de armas em células que permanecem no biofilme. Esse papel dual faz do complexo DspI–DspII um núcleo central que conecta o tamanho populacional, a fuga do biofilme e a virulência aguda. Como interromper o complexo pode bloquear tanto a produção do sinal quanto a ativação do sistema de toxinas, ele oferece um alvo atraente para futuros fármacos que poderiam manter Pseudomonas em um estado crônico menos nocivo e prevenir surtos perigosos.
Citação: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Palavras-chave: Pseudomonas aeruginosa, dispersão de biofilme, quorum sensing, mudança de virulência, cis-2-decanoico