Clear Sky Science · pt
Um atlas espacialmente resolvido do câncer gástrico caracteriza uma região agregada por linfócitos
Por que o bairro ao redor de um tumor importa
O câncer não é apenas um aglomerado de células descontroladas; ele vive em um bairro movimentado de células imunes e estruturais que podem tanto ajudar a combater o tumor quanto permitir que ele cresça sem controle. Este estudo mapeia esse bairro no câncer gástrico com detalhes sem precedentes, mostrando como pequenos pontos quentes e frios imunes dentro do mesmo tumor podem influenciar se um paciente responde às imunoterapias modernas.
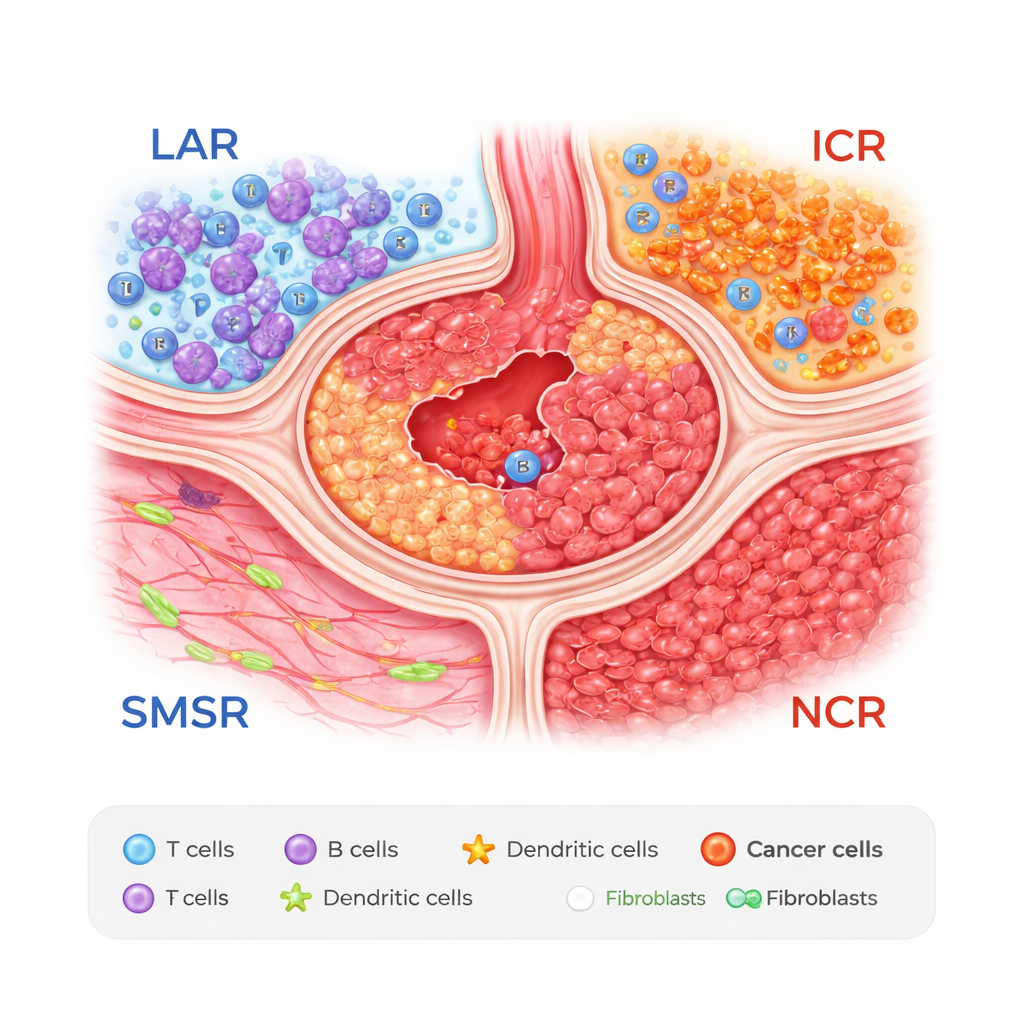
Quatro zonas dentro de um tumor estomacal
Os pesquisadores combinaram duas ferramentas poderosas: sequenciamento de RNA de célula única, que lê a atividade gênica em células individuais, e transcriptômica espacial, que registra onde essas células estão em cortes de tecido. Estudando amostras de 27 pacientes, eles descobriram que os tumores estomacais podem ser divididos em quatro zonas recorrentes. Uma é uma região agregada por linfócitos, ou RAL, rica em aglomerados de células T e B que lembram minúsculos linfonodos. Outra é uma região de músculo liso e estroma (RMSE), dominada por músculo e tecido conjuntivo. As duas zonas restantes são áreas densas em câncer: uma região de câncer imunogênico (RCI), onde células tumorais se misturam com alguns tipos protetores de células gástricas, e uma região de câncer negativo-imunogênico (RCNI), repleta de células malignas e relativamente poucas células imunes defensivas.
Pontos quentes imunes relacionados a melhores desfechos
A equipe constatou que a zona RAL é enriquecida em genes normalmente vistos em linfonodos, onde as células imunes são treinadas e ativadas. Isso inclui sinais que ajudam a recrutar linfócitos e organizá-los em estruturas chamadas estruturas linfóides terciárias. Ao examinar grandes bancos de dados públicos de câncer, tumores com maior expressão de genes associados à RAL tendiam a apresentar melhor sobrevida dos pacientes e uma probabilidade um pouco maior de responder a terapias com bloqueio de checkpoints imunológicos que liberam os freios das células T. Em contraste, assinaturas gênicas de regiões ricas em músculo ou fortemente cancerosas estavam geralmente associadas a piores prognósticos em vários tipos de câncer.
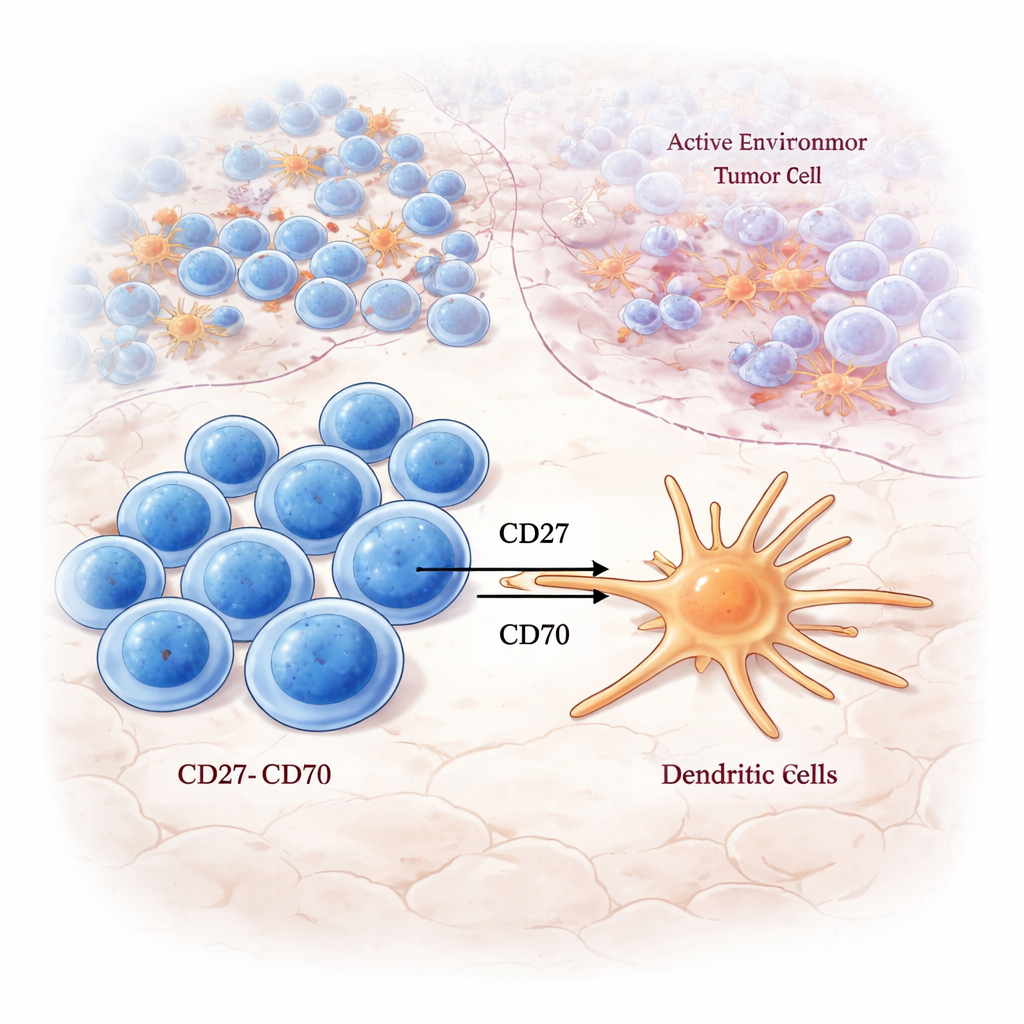
Onde células T naïvas aprendem a combater
Ao aprofundar-se na RAL, os autores observaram forte atividade em vias de sinalização centrais para ativar células T: sinalização do receptor de células T, vias de coestimulação e processamento de antígenos. Células CD8 T naïvas — células que ainda não se comprometeram totalmente a atacar um alvo específico — estavam especialmente associadas a esses sinais de ativação dentro da RAL, mas não em outros locais. Usando coloração multicolorida, detectaram células CD8 T na RAL que exibiam marcadores tanto de renovação quanto de proliferação, sugerindo que essa região atua como uma zona local de treinamento e expansão onde novas células combatentes do tumor são preparadas.
Dois sabores de vizinhança imune
Nem todas as RALs eram iguais. Quando os pesquisadores agruparam os pacientes segundo a composição celular de suas RALs, descobriram dois padrões. Em tumores do “Grupo A”, as RALs se assemelhavam fortemente a linfonodos clássicos, ricas em células B especializadas e células dendríticas, e as regiões tumorais adjacentes a essas RALs estavam repletas de linfócitos ativados e prontos para a batalha. No “Grupo B”, as RALs eram menos desenvolvidas, e o tecido tumoral adjacente continha mais células T em repouso, menos engajadas. Análises computacionais avançadas de imagens de tecido confirmaram que células imunes ativadas se agrupavam fisicamente próximas a essas RALs mais maduras, sugerindo que a arquitetura local pode orientar quão vigorosamente o sistema imunológico ataca o tumor.
Sinais de checkpoint no espaço
O estudo também rastreou onde os “interruptores” imunes conhecidos como moléculas de checkpoint são expressos. Pares estimuladores como CD27–CD70 estavam concentrados na RAL, particularmente em tumores do Grupo A, conectando células CD8 exauridas mas reativas ao tumor com células dendríticas que poderiam potencialmente aumentar ainda mais sua atividade. Em contraste, muitos pares de checkpoints inibitórios, como TIGIT–NECTIN2 e LAG3–LGALS3, estavam enriquecidos na RCNI, a zona mais carregada de câncer. Isso sugere que, mesmo quando a sinalização do receptor de células T está presente, a paisagem de checkpoints ao redor pode inclinar a imunidade local para ataque ou supressão, dependendo da região do tumor.
O que isso significa para os pacientes
Para um não especialista, a mensagem chave é que onde as células e sinais imunes se situam dentro de um tumor pode importar tanto quanto quantas existem. Este trabalho mostra que os cânceres gástricos contêm vizinhanças imunes distintas, e que regiões robustas, semelhantes a linfonodos, próximas ao tumor estão associadas a células T mais ativas, melhor posicionadas e a desfechos mais favoráveis. Ao aprender a reconhecer e possivelmente reforçar essas regiões agregadas por linfócitos, terapias futuras poderiam ser mais bem ajustadas — escolhendo fármacos, combinações ou até abordagens de entrega direcionada que explorem os próprios redutos imunes internos do tumor.
Citação: Gao, S., Qin, S., Wang, D. et al. A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region. Nat Commun 17, 2059 (2026). https://doi.org/10.1038/s41467-026-68612-z
Palavras-chave: câncer gástrico, microambiente tumoral, estruturas linfóides terciárias, transcriptômica espacial, imunoterapia contra o câncer