Clear Sky Science · pt
Envelhecimento divergente de mamas nulíparas e páras revela células epiteliais híbridas IL33+
Como a gravidez pode remodelar o risco de câncer de mama ao longo da vida
Por que ter um bebê cedo na vida reduz o risco vitalício de câncer de mama, enquanto apenas envelhecer o aumenta? Este estudo usa camundongos para perscrutar o “ecossistema” celular da mama ao longo do tempo, comparando animais que nunca gestaram com aqueles que gestaram. Ao acompanhar como células individuais mudam com a idade e a reprodução, os pesquisadores descobriram um tipo raro de célula mutável que pode ajudar a explicar a proteção de longo prazo conferida pela gravidez.
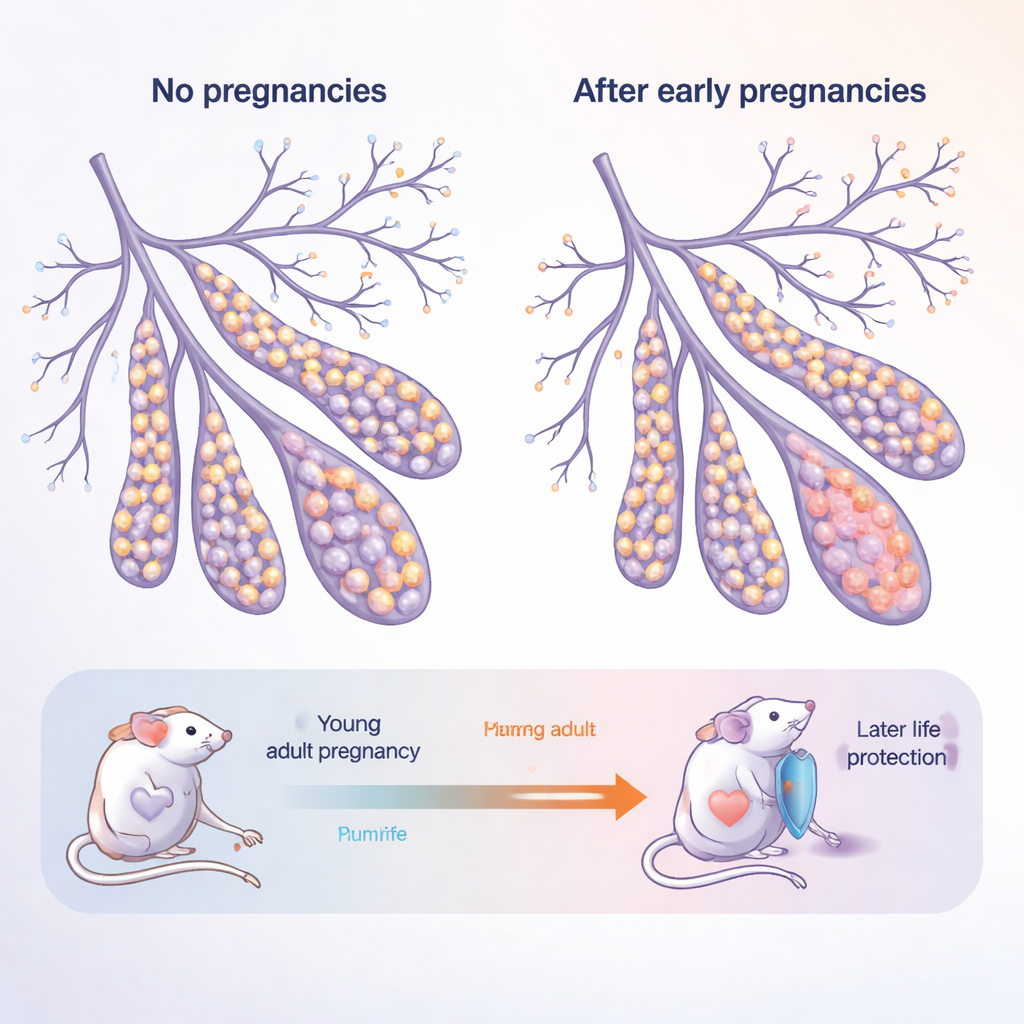
A mama como um tecido vivo e em transformação
A glândula mamária não é um órgão estático: ela cresce e se remodela dramaticamente na puberdade, durante a gravidez e novamente quando a produção de leite cessa. É composta por duas camadas principais de células epiteliais que revestem os ductos: as células “luminais” internas, que entram em contato com o leite e hormônios, e as células “basais” externas, que dão estrutura e abrigam células de tipo‑tronco. Os autores estudaram camundongos jovens adultos e camundongos mais velhos, “pós‑menopáusicos”, cada grupo composto por animais nunca grávidos (nulíparos) ou por animais que passaram por múltiplas gestações (páras). Esse desenho imita uma mulher que dá à luz aos vinte e poucos anos e depois envelhece até os cinquenta e além.
Como envelhecimento e gravidez puxam o tecido em direções diferentes
Quando os camundongos envelheceram sem nunca engravidar, suas glândulas mamárias se deslocaram para uma maior proporção de células basais e menos células luminais. Essas glândulas mais velhas e nunca grávidas também geraram muito mais organoides — estruturas 3D em miniatura cultivadas a partir de células individuais — indicando que suas células estavam incomumente prontas para proliferar. Em contraste, camundongos que tiveram gestações exibiram um equilíbrio “normalizado”: o aumento relacionado à idade no número de células basais foi atenuado, e suas células formaram menos organoides. Isso sugere que a gravidez deixa uma marca duradoura que tanto altera como as células escolhem seu destino quanto freia seu potencial regenerativo e, possivelmente, propenso a câncer.
A descoberta de células híbridas e mutáveis
Para investigar mais a fundo, a equipe usou sequenciamento de RNA de célula única para ler quais genes estavam ativos em milhares de células mamárias individuais. Entre as esperadas células luminais, basais, imunes e do estroma, encontraram um grupo raro que não se encaixava claramente em nenhuma das camadas principais. Essas células expressavam marcadores de ambas as linhagens luminal e basal, ganhando o nome de células epiteliais “híbridas”. De forma marcante, esses híbridos se acumularam com a idade em camundongos nunca grávidos, mas eram muito menos comuns em camundongos igualmente velhos que haviam engravidado. Os híbridos expressavam fortemente um gene chamado Il33, que codifica a molécula de sinalização IL‑33, junto com marcadores ligados a estágios iniciais de desenvolvimento e alta plasticidade — a capacidade de mudar identidade ou comportamento.
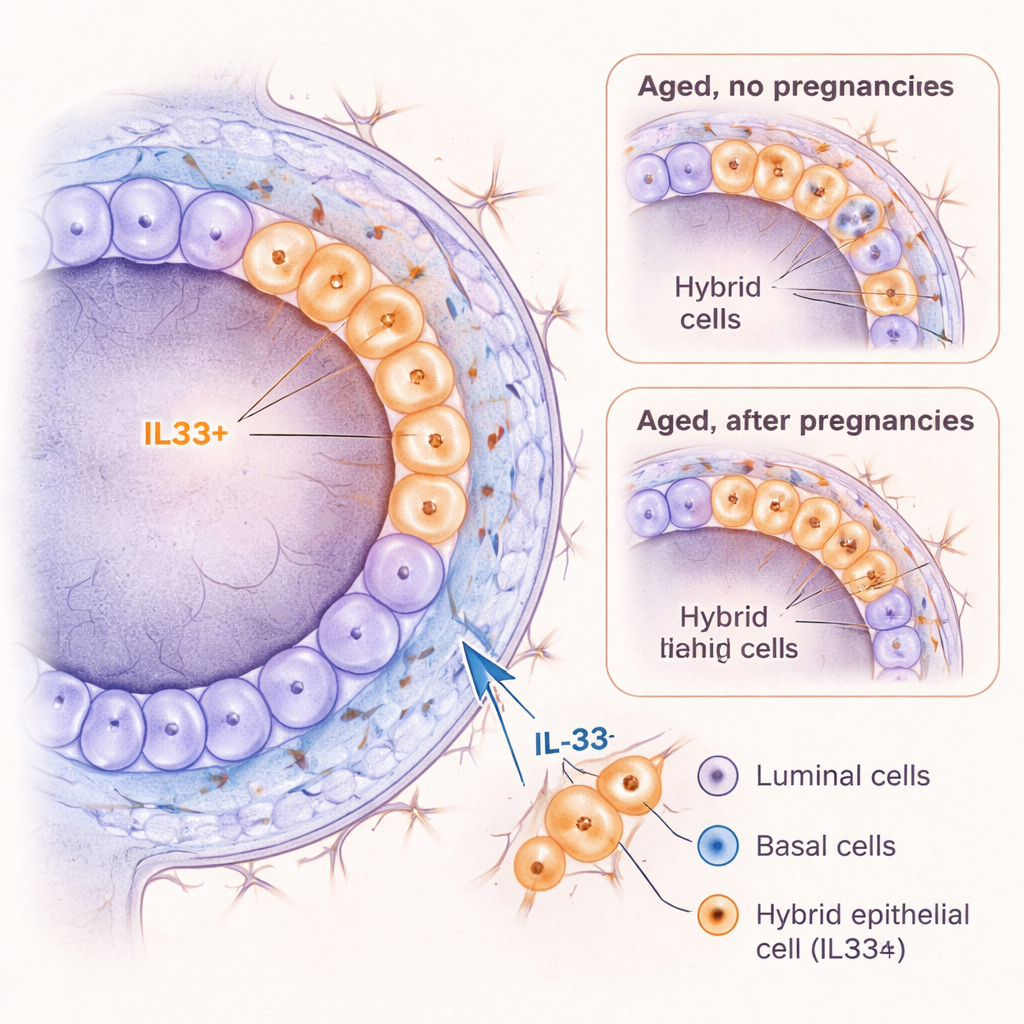
IL‑33 como motor de estados celulares arriscados
Como IL‑33 tem sido associado à inflamação e ao câncer em outros órgãos, os pesquisadores perguntaram se ele pode ativamente empurrar células mamárias para um estado tipo‑híbrido. Quando trataram células mamárias jovens de camundongos com IL‑33 em cultura 3D, células da camada basal formaram mais organoides, mantiveram uma identidade mais primitiva e produziram mais células com o marcador híbrido KRT6A. Em camundongos jovens vivos, injeções de curto prazo de IL‑33 alargaram os ductos e desencadearam um surto de divisão celular, junto com um pico temporário de células híbridas KRT6A‑positivas e um deslocamento em direção a uma aparência mais basal. Importante, quando as células carregavam uma mutação ligada ao câncer (perda do gene supressor de tumor Trp53), o IL‑33 aumentou ainda mais seu crescimento. Em conjunto, esses achados sugerem que IL‑33 ajuda a criar um estado celular plástico e proliferativo que pode ser especialmente vulnerável à transformação cancerígena.
Pistas a partir do tecido mamário humano
Para testar se células semelhantes existem em humanos, os autores reanalisaram diversos grandes conjuntos de dados de célula única de tecido mamário humano normal. Identificaram uma pequena população de células epiteliais humanas que, como os híbridos de camundongo, exibiam características tanto luminais quanto basais e expressavam IL33 e genes relacionados. Células IL33‑positivas tornaram‑se mais comuns com a idade em múltiplos conjuntos de dados. Em células mamárias humanas primárias cultivadas em laboratório, o tratamento com IL‑33 aumentou a formação de organoides, deslocou as células para um perfil mais basal e enriqueceu células CD44‑positivas — um marcador frequentemente associado a células imaturas, de tipo‑tronco, no câncer de mama. Embora as amostras humanas disponíveis não permitissem testar de forma clara como uma gravidez precoce altera essa população, os paralelos com os achados em camundongos são notáveis.
O que isso significa para a compreensão da proteção contra o câncer de mama
Para um leitor leigo, a mensagem central é que a gravidez parece reconfigurar a forma como o tecido mamário envelhece. Em camundongos, uma gravidez precoce impede o acúmulo de células híbridas ricas em IL‑33 que borram a fronteira entre as principais camadas da mama e se comportam de maneira altamente flexível e pronta para proliferar. O próprio IL‑33 pode empurrar células para esse estado arriscado e mutável, especialmente quando estão presentes mutações relacionadas ao câncer. Ao reduzir o número ou a persistência dessas células híbridas, a gravidez pode diminuir as chances de que o tecido mamário envelhecido contenha o tipo “errado” de célula no momento “errado” — uma célula pronta para transitar para o câncer. Essa visão mecanística pode, eventualmente, orientar estratégias para mimetizar os efeitos protetores da gravidez precoce sem exigir uma gravidez.
Citação: Olander, A., Medina, P., Haro Acosta, V. et al. Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells. Nat Commun 17, 1898 (2026). https://doi.org/10.1038/s41467-026-68611-0
Palavras-chave: envelhecimento da mama, gravidez e câncer de mama, células‑tronco mamárias, sinalização IL‑33, células epiteliais híbridas