Clear Sky Science · pt
ZFP57 é um regulador do crescimento pós-natal e da saúde ao longo da vida
Como o leite precoce molda a saúde ao longo da vida
O que acontece nos primeiros dias de vida pode repercutir por décadas. Este estudo mostra que uma única proteína materna, chamada ZFP57, ajuda a determinar quão bem a glândula mamária se desenvolve, o que entra no leite materno e como a prole cresce e regula a energia pelo resto da vida. Ao rastrear a influência dessa proteína da mãe grávida aos filhotes em amamentação, os pesquisadores revelam uma camada genética oculta por trás dos benefícios bem conhecidos da nutrição precoce.
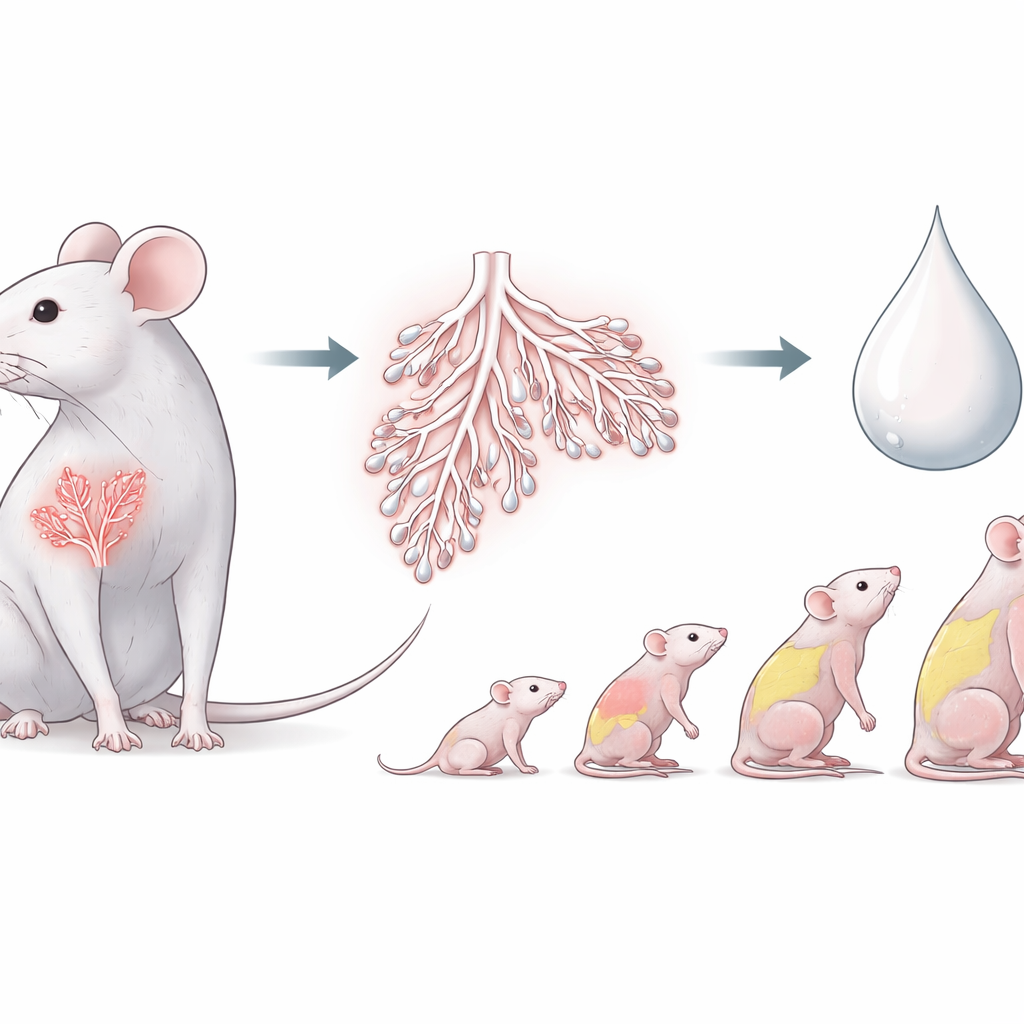
Uma guardiã do crescimento antes e depois do nascimento
ZFP57 já era conhecida como reguladora-chave do “imprinting genômico”, um sistema de marcação química que indica se certos genes vieram da mãe ou do pai. Essas marcas são cruciais para o crescimento normal antes do nascimento. O novo trabalho pergunta se ZFP57 também importa mais tarde, após o parto, quando as mães alimentam os jovens com leite. Usando camundongos, os autores mostram que ZFP57 está ativa não apenas em embriões e na placenta, mas também em tecidos adultos, incluindo o cérebro e a glândula mamária. Isso sugere que a mesma molécula que ajuda a controlar o crescimento fetal pode também ajudar a gerenciar a nutrição pós-natal.
Como a glândula materna é programada para alimentar
A equipe examinou glândulas mamárias de fêmeas normais e de fêmeas deficientes em Zfp57 em estágios chave: antes da gravidez, durante a gestação e no início da lactação. Eles separaram diferentes tipos celulares e mediram milhares de níveis de atividade gênica. Embora o desenvolvimento geral da glândula ainda prosseguisse, os detalhes finos estavam alterados quando ZFP57 estava ausente. Antes da gravidez, as glândulas mutantes exibiram ramificação incomumente densa e ativação precoce de genes normalmente ligados mais tarde para preparar a produção de leite. Durante a gestação, o padrão se inverteu: a ramificação e a atividade de genes relacionados ao leite caíram, e muitas células sofreram morte programada. Essas alterações desbalancearam os tipos celulares que constroem e mantêm um órgão produtor de leite saudável.
Qualidade do leite, padrões de crescimento e mães incompatíveis
Essas mudanças estruturais e moleculares se traduziram em leite alterado e em filhotes alterados. Mães deficientes em Zfp57 produziram leite com níveis mais altos de gorduras oxidadas e níveis mais baixos de certas fosfolipídios que ajudam a empacotar lipídios em gotículas. Filhotes amamentados por essas mães, independentemente de seu próprio genótipo, inicialmente cresceram mais devagar e alguns não prosperaram. Ainda assim, um grupo de descendentes, portando uma mutação específica em Zfp57 e que se desenvolveram em úteros deficientes em Zfp57, respondeu de forma muito diferente: apesar de problemas iniciais de sucção e ingestão de leite visivelmente atrasada, ganharam peso excessivo durante a lactação. Experimentos de cross-fostering, nos quais recém-nascidos foram trocados entre mães de genótipos diferentes, revelaram que o crescimento foi melhor quando o fundo genético da mãe que amamentava combinava com as condições experimentadas no útero. Quando filhotes adaptados a um ambiente materno foram alimentados por uma mãe geneticamente diferente, seu crescimento e metabolismo frequentemente foram empurrados para extremos.
Da alimentação precoce ao metabolismo adulto
A história não terminou ao desmame. Os pesquisadores acompanharam os camundongos por seis meses, o equivalente aproximado da juventude adulta humana. Descendentes que se desenvolveram em mães deficientes em Zfp57 e que carregavam a cópia alterada de Zfp57 mostraram alterações duradouras: maior percentual de gordura corporal, menor massa magra e uma maior dependência de queima de gorduras em vez de carboidratos, mesmo consumindo a mesma dieta padrão dos controles. Alguns também eliminaram glicose do sangue menos eficientemente, uma marca de baixa tolerância à glicose associada à síndrome metabólica. Notavelmente, esses problemas de longo prazo foram piores quando tais filhotes foram cross-fostered para mães normais, destacando como uma incompatibilidade entre o ambiente pré-natal e a nutrição pós-natal pode consolidar trajetórias de saúde prejudiciais.
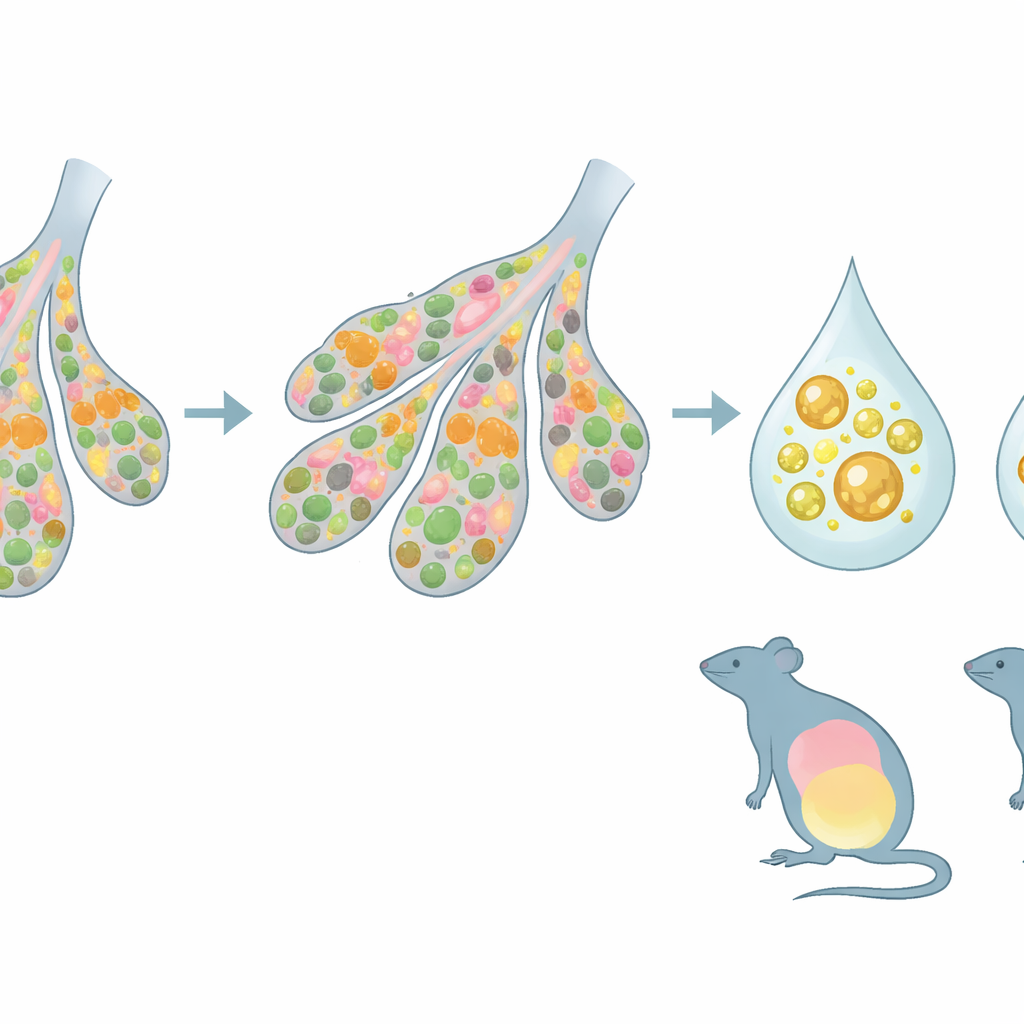
Por que isso importa para a saúde humana
Ao revelar um papel de ZFP57 na modelagem da função da glândula mamária e da composição do leite, independentemente de suas funções clássicas no imprinting, este trabalho liga um gene materno ao controle de recursos pré- e pós-natais. Sustenta a ideia de que mães e descendentes são co-adaptados geneticamente: o ambiente uterino e o suprimento de leite são ajustados entre si, e quebrar essa correspondência pode ter custos duradouros. Embora o estudo tenha sido realizado em camundongos, ZFP57 também é importante em humanos, onde mutações estão associadas a problemas metabólicos na primeira infância. As descobertas sugerem que alguns riscos ao longo da vida para obesidade e diabetes podem surgir não apenas da dieta em si, mas de como nossos genes organizam a nutrição precoce e de quão bem os ambientes pré- e pós-natais se alinham.
Citação: Hanin, G., AlSulaiti, B., Costello, K.R. et al. ZFP57 is a regulator of postnatal growth and life-long health. Nat Commun 17, 2080 (2026). https://doi.org/10.1038/s41467-026-68608-9
Palavras-chave: nutrição no início da vida, epigenética, glândula mamária, saúde metabólica, imprinting genômico