Clear Sky Science · pt
Ampliando o escopo de cargas úteis em conjugados anticorpo-droga por meio da entrega de fármacos com grupos hidroxila via fosforamidas auto-imolativas
Mísseis mais inteligentes contra o câncer
Os medicamentos contra o câncer podem ser extremamente potentes, mas frequentemente agem como bombardeio generalizado: atingem tecidos saudáveis quase tão intensamente quanto os tumores. Os conjugados anticorpo–droga (ADCs) foram criados para resolver esse problema ao ligar uma droga potente a um anticorpo que se dirige às células tumorais, transformando o tratamento em um míssil guiado. Este artigo explica um novo “conector” químico entre anticorpo e droga que torna esses mísseis mais precisos e flexíveis, abrindo caminho para muitos tipos de medicamentos oncológicos que os ADCs atuais não conseguem transportar.
Por que os fármacos direcionados de hoje ainda são limitados
Os ADCs são construídos a partir de três partes: um anticorpo que reconhece um marcador nas células cancerosas, um fármaco tóxico (a “carga útil”) e um ligante químico que os une. A maioria dos ADCs aprovados depende de apenas alguns tipos de cargas úteis que danificam o DNA ou bloqueiam a divisão celular de maneiras semelhantes. Uma razão importante é o ligante: ele deve manter a droga firmemente presa enquanto o ADC circula na corrente sanguínea e então liberá‑la de forma limpa uma vez dentro da célula tumoral. Os ligantes existentes funcionam bem apenas com certos grupos químicos nas drogas, especialmente aminas, e muitas vezes têm dificuldade com os numerosos fármacos que contêm grupos alcoóis (–OH). Isso deixa um grande número de agentes promissores de lado porque não podem ser entregues com segurança ou eficiência pelos desenhos atuais de ADCs.
Emprestando um truque de comprimidos antivirais
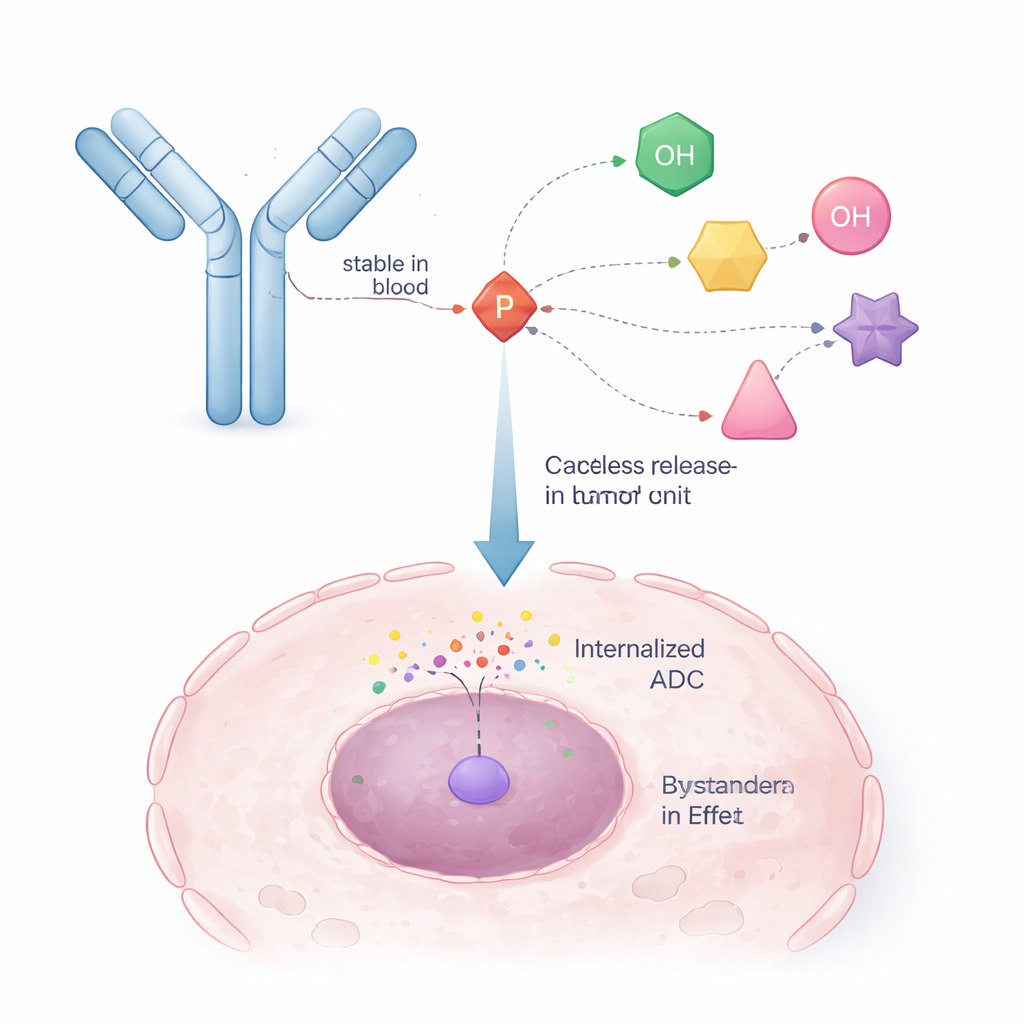
Os pesquisadores recorreram a uma estratégia já comprovada em antivirais chamada ProTides. Nesses medicamentos, uma unidade química à base de fósforo mascara temporariamente o grupo fosfato carregado de uma droga para que ela possa entrar nas células e depois se desmonta no interior para liberar a forma ativa. Os autores reconfiguraram esse conceito de modo que um braço do núcleo de fósforo seja usado para se ligar a um anticorpo, enquanto os outros braços alojam a droga contra o câncer. Isso cria um ligante “auto‑imolativo”: quando um gatilho interno (como uma enzima em uma célula tumoral) remove uma pequena parte da estrutura, a unidade de fósforo colapsa de maneira controlada e libera a molécula original da droga com seu grupo hidroxila restaurado e sem modificações.
Construindo um conector químico versátil
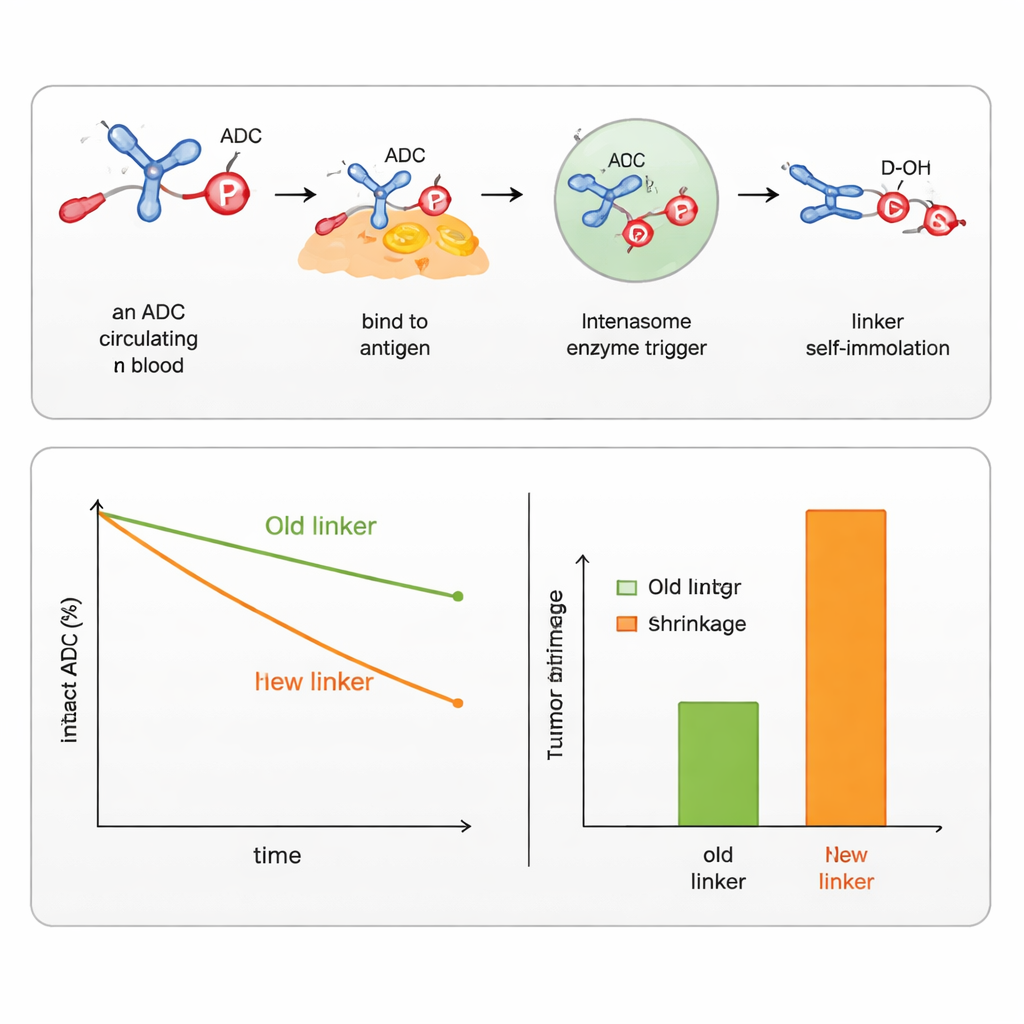
A equipe demonstrou que, ao ajustar os grupos ao redor do átomo de fósforo, era possível afinar a estabilidade do ligante no sangue e a rapidez com que ele se desmonta dentro das células. Projetaram versões que respondem a vários tipos de gatilhos comuns dentro de células tumorais, incluindo esterases e proteases (enzimas que cortam ligações específicas), além de enzimas que reconhecem grupos à base de açúcar ou condições redutoras em compartimentos celulares. Usando esses desenhos, eles conseguiram ligar e liberar tanto álcoois aromáticos (como a quimioterápica SN38) quanto álcoois alifáticos (como DXd, a carga útil de um ADC aprovado para câncer de mama). Em comparação direta com ligantes comerciais existentes para SN38 e DXd, os novos ligantes fosforamídicos mantiveram as drogas unidas por mais tempo no soro, entregaram mais droga aos tumores e produziram maior regressão tumoral em camundongos, ao mesmo tempo em que apresentaram menor impacto nas células saudáveis.
Desbloqueando muitas novas cargas úteis contra o câncer
Para testar a amplitude de aplicação do ligante, os pesquisadores montaram ADCs carregando dez fármacos diferentes que contêm pelo menos um grupo –OH, mas agem de maneiras muito distintas dentro das células tumorais. Isso incluiu inibidores da síntese de DNA, do dobramento de proteínas (HSP90), do metabolismo energético (NAMPT e DHODH) e da tradução de proteínas, além de agentes bem conhecidos como paclitaxel e gemcitabina. Apesar da ampla variedade de estruturas, eles conseguiram fabricar ADCs uniformes com alta carga de droga para todos eles. Em estudos celulares em múltiplos tipos de câncer, a maioria desses ADCs mostrou potência na faixa de nanomolar ou até sub‑nanomolar e clara seletividade por células que expressavam o alvo do anticorpo, confirmando que o ligante podia liberar consistentemente a droga ativa dentro das células corretas.
Gemcitabina como vitrine
A gemcitabina é uma quimioterapia amplamente usada, mas em sua forma convencional é eliminada do organismo tão rapidamente que os pacientes precisam receber doses repetidas e elevadas, o que limita o quanto pode ser administrado com segurança. Usando o ligante fosforamídico, os autores ligaram a gemcitabina a um anticorpo direcionado ao HER2 em uma de duas posições de álcool e mostraram que ambas as versões retomaram atividade plena uma vez dentro das células cancerosas. Em modelos murinos de tumores HER2‑positivos, uma única dose do ADC de gemcitabina — contendo cerca de mil vezes menos gemcitabina total do que regimes típicos de droga livre — produziu forte e seletivo controle tumoral. O comportamento do ADC na corrente sanguínea coincidiu de perto com o do anticorpo nu, e doses elevadas foram bem toleradas em ratos, sugerindo uma ampla margem de segurança.
O que isso significa para o tratamento futuro do câncer
Para não especialistas, a mensagem principal é que este trabalho entrega um novo conector químico altamente adaptável que permite aos anticorpos transportar um conjunto muito mais amplo de fármacos contra o câncer do que antes, e fazê‑lo com mais segurança. Ao garantir que as drogas permaneçam ligadas enquanto circulam e sejam liberadas de forma limpa somente depois que o ADC é internalizado por uma célula tumoral, os ligantes fosforamídicos melhoram a quantidade de droga que chega ao tumor e reduzem os danos colaterais aos tecidos saudáveis. Igualmente importante, eles permitem que fármacos pequenos e potentes já existentes — com formas e mecanismos muito diferentes — sejam reaproveitados como terapias direcionadas. Isso poderia ampliar consideravelmente o cardápio de ADCs disponíveis para pacientes e ajudar a combater tumores que se tornaram resistentes ao conjunto limitado de cargas úteis atual.
Citação: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
Palavras-chave: conjugados anticorpo–droga, administração de fármacos contra o câncer, ligantes auto-imolativos, química de fosforamidas, quimioterapia direcionada