Clear Sky Science · pt
Eletrólise de hidrogenação de CO2 sem membrana para gestão de precipitação de sais na redução eletroquímica ácida de CO2
Transformando a poluição climática em combustível líquido útil
Dióxido de carbono (CO2) de usinas e fábricas é um dos principais motores das mudanças climáticas, mas também é uma matéria-prima barata e abundante. Cientistas correm para converter CO2 em produtos químicos úteis usando eletricidade de fontes renováveis. Este estudo aborda um obstáculo prático que tem limitado silenciosamente essas tecnologias: o acúmulo de sais dentro de reatores em estilo industrial que, aos poucos, sufocam o desempenho. Os pesquisadores apresentam um novo projeto de reator sem membrana que mantém operação contínua por dias enquanto converte CO2 eficientemente em ácido fórmico, um líquido que pode ser usado como insumo químico, conservante ou porta-energia.
Por que os dispositivos atuais de CO2 entopem
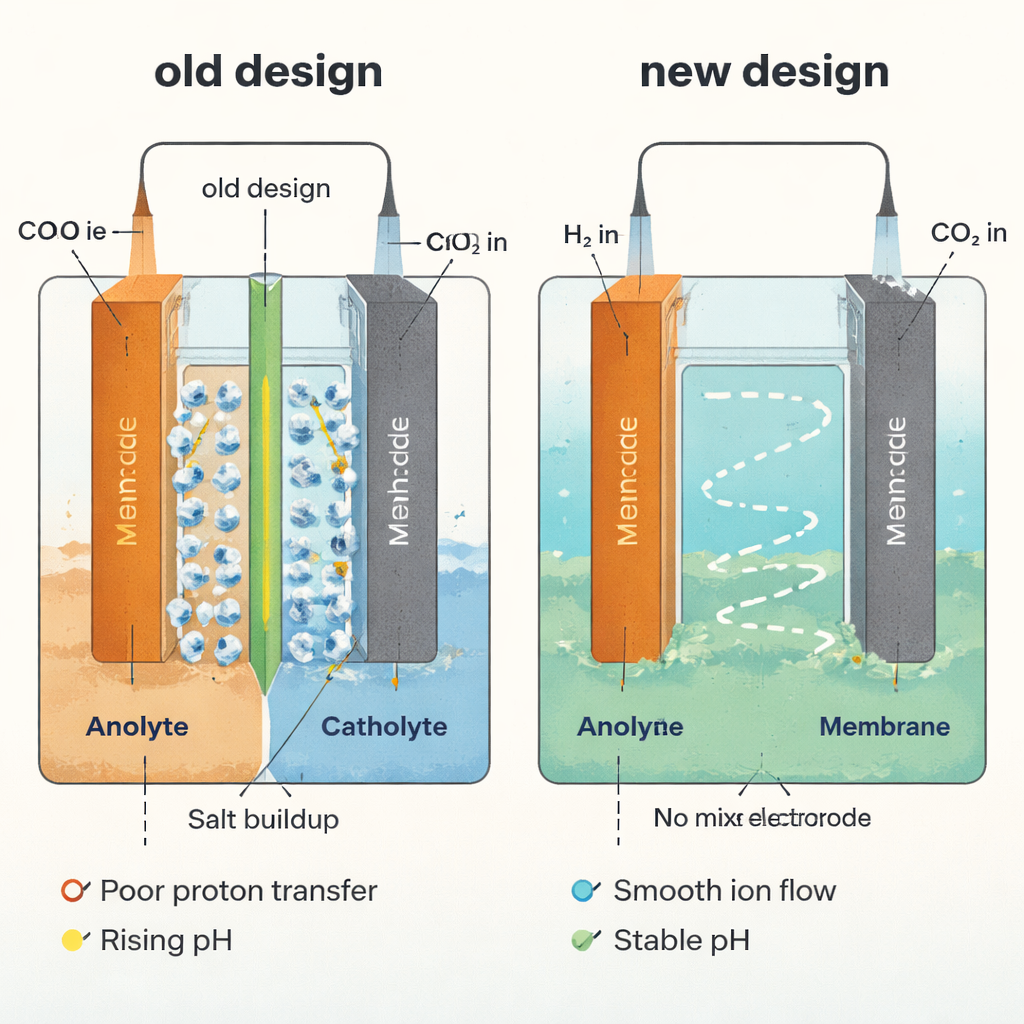
Muitos dispositivos que convertem CO2 em produtos lembram células a combustível compactas. CO2 é alimentado de um lado (o cátodo), onde é convertido em produtos, enquanto a água é dividida do outro lado (o ânodo) para fornecer as cargas positivas necessárias (prótons). Uma folha polimérica fina chamada membrana fica entre esses dois lados, permitindo a passagem de certos íons mas mantendo os líquidos separados. Em meios alcalinos ou neutros, grande parte do CO2 reage com hidróxido para formar sais de carbonato em vez de produtos úteis, desperdiçando carbono e exigindo reciclagem energeticamente custosa. Líquidos ácidos podem evitar isso, mas então o sistema depende da capacidade da membrana em fornecer prótons rápida e uniformemente. Quando a entrega de prótons fica lenta, a acidez local no cátodo sobe, carbonatos e bicarbonatos cristalizam, e sais sólidos gradualmente bloqueiam as vias de gás necessárias para o CO2 alcançar o catalisador.
Uma nova forma de mover prótons sem barreira
A equipe primeiro quantificou quão eficientemente os prótons se movem através de membranas em reatores ácidos típicos, introduzindo uma medida simples: o número de prótons que atravessam por elétron que passa pelo circuito. Usando teoria e simulações computacionais, mostraram que membranas reais raramente atingem a transferência ideal de prótons. Filmes mais espessos, menor seletividade a prótons e certas misturas iônicas retardam o movimento de prótons e criam acidez desigual entre os dois lados. Experimentos confirmaram isso: em uma célula padrão com membrana, o católito (líquido no cátodo) passou de fortemente ácido a quase neutro em poucas horas, favorecendo a formação de carbonato e a precipitação de sais profundamente dentro do eletrodo de difusão de gás.
Hidrogenação de CO2 sem membrana
Para escapar completamente do gargalo imposto pela membrana, os pesquisadores a removeram e deixaram um único líquido compartilhado fluir por ambos eletrodos. Isso por si só estabilizou o pH, mas criou um novo problema: o valioso ácido fórmico produzido no cátodo poderia ser destruído em um ânodo convencional que realiza a reação de evolução de oxigênio, a qual opera em voltagens relativamente altas onde muitas moléculas orgânicas são oxidadas. A solução foi substituir a evolução de oxigênio pela reação de oxidação do hidrogênio—essencialmente “queimar” hidrogênio em prótons a uma tensão muito baixa. Neste eletrólito de hidrogenação de CO2 sem membrana, hidrogênio é fornecido ao ânodo, CO2 ao cátodo, e o líquido em fluxo mistura rapidamente os prótons e hidróxidos produzidos em cada lado, evitando qualquer gradiente de pH duradouro e reduzindo drasticamente o acúmulo de sais.
Catalisador inteligente e desempenho de longo prazo
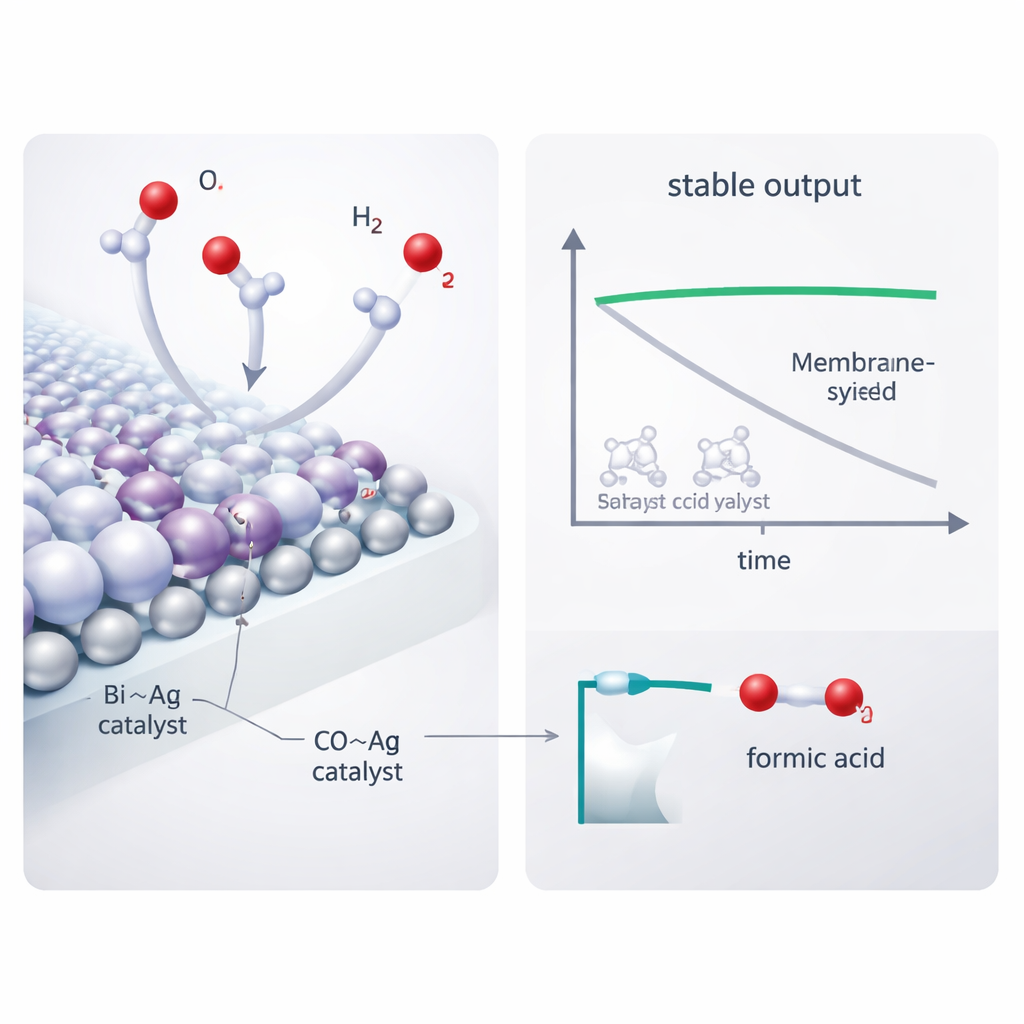
No coração do cátodo, os autores construíram um catalisador bismuto–prata (Bi–Ag) que combina a aptidão do bismuto para produzir formiato com a excelente condutividade elétrica da prata. Microscopia e espectroscopia revelaram nanopartículas de prata decorando nanosheets de bismuto e interações eletrônicas sutis entre os dois metais que melhoram a adsorção e ativação do CO2. Em solução ácida, esse catalisador converteu CO2 em ácido fórmico com mais de 90% de eficiência em uma ampla faixa de correntes. Quando colocado no reator acoplado ao hidrogênio sem membrana, entregou mais de 90% de eficiência a 100 miliamperes por centímetro quadrado usando apenas 1,7 volts—significativamente menor que projetos concorrentes—e operou de forma estável por 208 horas. Apenas traços de sal de carbonato foram detectados no eletrodo após dias de operação, mostrando que o problema de precipitação foi em grande parte suprimido.
Do laboratório ao aprimoramento prático do CO2
Além de demonstrar que o conceito funciona, a equipe avançou o projeto rumo à relevância prática. Ao reduzir o canal de líquido entre os eletrodos, diminuíram a resistência elétrica e mantiveram alto desempenho em voltagens menores. Alcançaram eficiência de conversão de CO2 em passagem única de até 77%, significando que a maior parte do CO2 que entra na célula foi transformada em produto em uma única passagem. Modelagem econômica sugeriu que remover a membrana, reduzir o consumo de energia e obter alta utilização de carbono pode reduzir significativamente o custo de produção do ácido fórmico, embora mais economias dependam de eletricidade mais barata, melhor separação do produto do líquido e operação em correntes mais altas. No geral, o trabalho demonstra uma rota prática para transformar CO2 residual em um produto químico líquido útil ao contornar um problema chave de durabilidade que tem prejudicado projetos de reatores anteriores.
Citação: Da, Y., Fan, L., Wang, W. et al. Membrane-free CO2 hydrogenation electrolyzer for salt precipitation management in acidic electrochemical CO2 reduction. Nat Commun 17, 1872 (2026). https://doi.org/10.1038/s41467-026-68600-3
Palavras-chave: eletrorredução de CO2, ácido fórmico, eletrólito sem membrana, oxidação de hidrogênio, utilização de carbono