Clear Sky Science · pt
Cianetação enantioseletiva e regiodivergente de C–H em aminas secundárias controlada por ligante
Por que mudar pequenas ligações importa para grandes medicamentos
Muitos medicamentos mais vendidos contêm pequenos blocos construtores à base de nitrogênio chamados aminas. Alterações sutis em como os átomos estão conectados ao redor dessas aminas podem transformar um fármaco fraco em um tratamento potente e preciso — ou em algo inativo ou até nocivo. Este artigo descreve uma nova maneira de modificar esses blocos de amina à vontade, permitindo que os químicos escolham exatamente onde na molécula reagir e qual forma imagem‑especular produzir, ambos cruciais para projetar medicamentos mais seguros e eficazes.
Escolhendo um ponto em uma molécula lotada
As aminas em medicamentos frequentemente têm vários enlaces carbono–hidrogênio (C–H) muito semelhantes que normalmente se comportam praticamente da mesma forma. Os químicos gostariam de trocar apenas um desses hidrogênios por um grupo útil, como um grupo ciano (–CN), sem perturbar o restante da molécula. Isso é difícil porque reações padrão tendem a ocorrer no sítio mais reativo definido pela estrutura da molécula, não pela escolha do químico. Aqui, os autores trabalham com aminas secundárias simples e flexíveis que carregam duas cadeias de carbono diferentes no nitrogênio. Eles mostram que, a partir da mesma amina, podem dirigir a reação para uma de duas posições vizinhas — ou ao lado de um pequeno grupo N‑metil (o chamado sítio α′) ou um carbono mais distante na outra cadeia (o sítio β) — simplesmente mudando o ligante que envolve um catalisador de cobre.
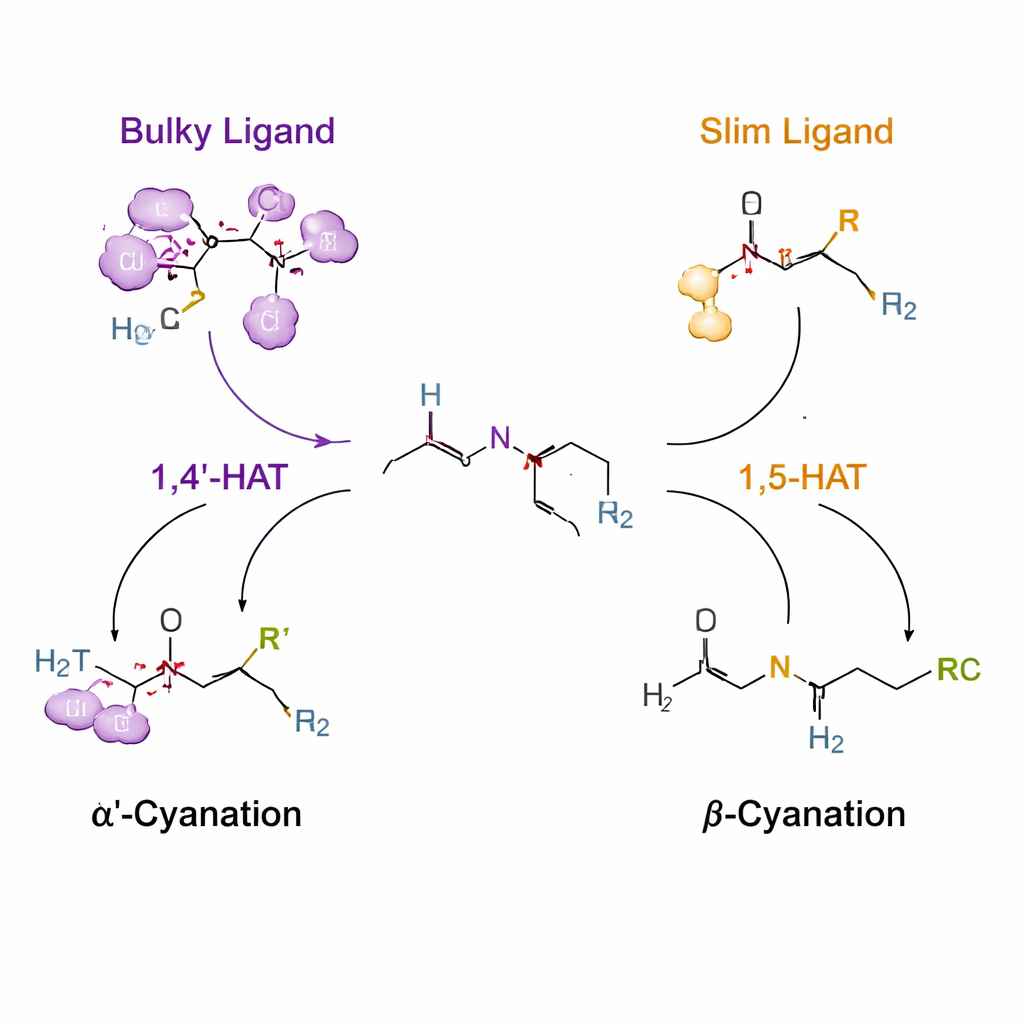
Usando “saltos” controlados de hidrogênio para guiar a reatividade
O truque chave baseia‑se em um processo chamado transferência de átomo de hidrogênio, em que um radical centrado no nitrogênio de vida curta arranca um hidrogênio de um carbono próximo. Normalmente, tais radicais preferem uma distância particular, favorecendo um “alcance” de seis membros conhecido como 1,5‑HAT. Os autores anexam uma alça temporária de ureia e cloro à amina para que, sob catálise por cobre, este radical nitrogenado se forme e possa capturar hidrogênio tanto da posição α′ quanto da posição β. Ao projetar ligantes — moléculas orgânicas que envolvem o cobre — eles remodelam o ambiente do radical. Um ligante muito volumoso (denominado L14) empurra o sistema para um passo incomum de 1,4′‑HAT que mira no grupo N‑metil, fornecendo cianetação seletiva no sítio α′. Ligantes mais esbeltos (como L8) permitem o caminho convencional 1,5‑HAT, direcionando a reação para o sítio β.
Do controle da posição ao controle da mão
Além de escolher onde reagir, a equipe também busca controlar a “mão” da molécula, ou quiralidade, o que é vital porque muitos fármacos existem em formas levógira e dextrógira que se comportam de modo diferente no organismo. Para conseguir isso, eles introduzem ligantes quirais — moléculas que por si têm uma forma mão — no complexo de cobre. Dois desses ligantes, L24 e L41, conferem alta preferência por uma imagem‑espelho quando a reação instala um grupo ciano em posições β, incluindo sítios benzílicos (ao lado de anéis aromáticos) e alipáticos‑alílicos (ao lado de duplas ligações C–C). Em uma ampla variedade de aminas de partida, o método entrega produtos β‑cianetados com excelente seletividade tanto de sítio quanto de mão, e funciona em escala de gramas, mostrando que o processo é prático e robusto para síntese.
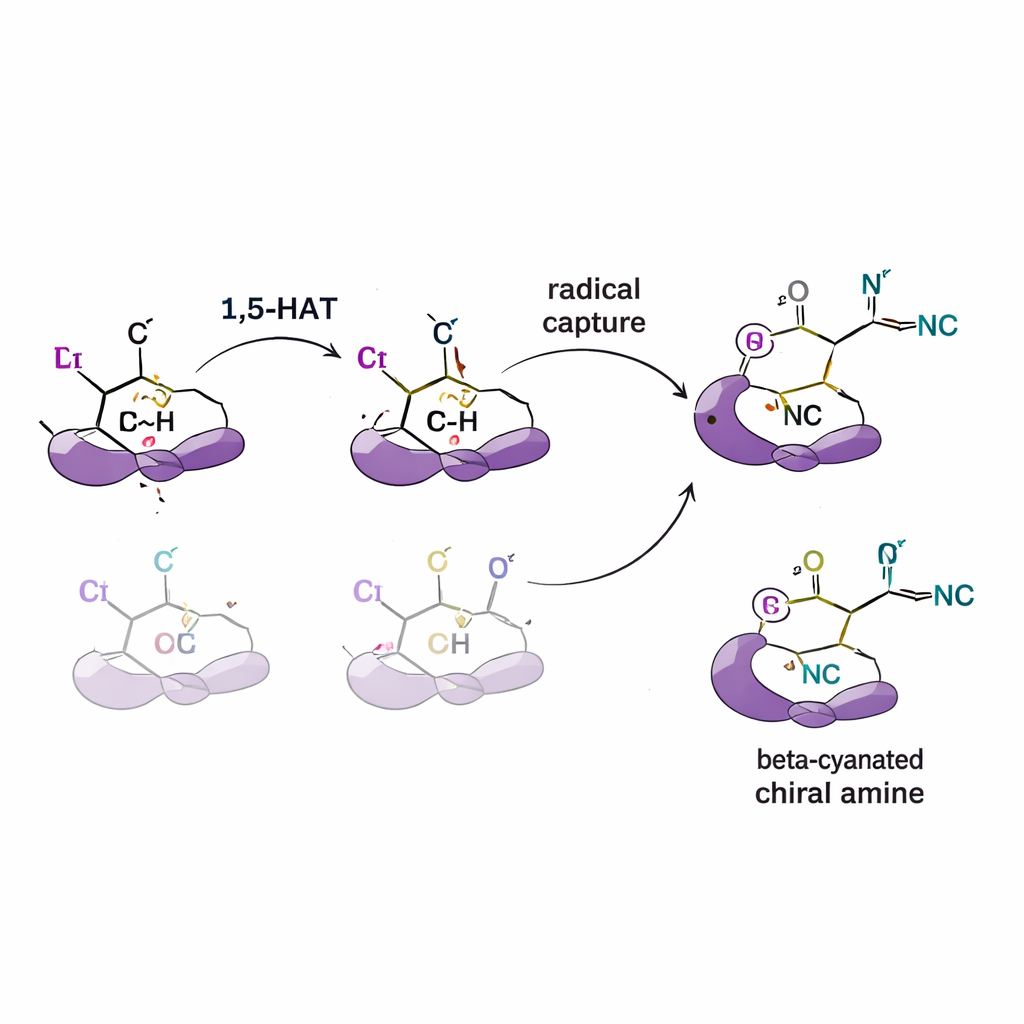
Testando o mecanismo por trás da seletividade
Para entender como esse controle surge, os autores realizaram uma série de experimentos mecanísticos. Ao adicionar “armadilhas” para radicais, eles confirmam que intermediários radicais reativos estão realmente envolvidos. Usando substratos nos quais certos hidrogênios são substituídos por deutério (uma forma mais pesada de hidrogênio), eles detectam efeitos isotópicos cinéticos que apontam para a etapa de transferência de hidrogênio como a etapa lenta que define a seletividade da reação. Experimentos de rotulagem também mostram que o hidrogênio se move em um único passo unidirecional em vez de transitar de um lado para outro entre posições. Simulações computacionais complementares (teoria do funcional da densidade) apoiam essas conclusões, indicando que a forma e o volume do ligante alteram a energia de vias concorrentes de transferência de hidrogênio e a maneira como o radical então se combina com o cobre e o cianeto para fornecer uma imagem‑espelho preferida.
O que isso significa para o futuro do desenho de medicamentos
No geral, este trabalho introduz uma estratégia flexível para reengenheirar grupos amina comuns em dois sítios intimamente relacionados, sob demanda, com controle refinado sobre a quiralidade molecular. Trocando apenas o ligante em um catalisador de cobre, os químicos podem escolher se colocam um grupo ciano em uma pequena unidade N‑metil ou no carbono vizinho de outra cadeia lateral, e podem fazer isso em muitas moléculas complexas semelhantes a fármacos. Como grupos ciano são valiosos degraus para muitos outros grupos funcionais, essa abordagem “ajuste‑o‑sítio” e “ajuste‑a‑mão” deve facilitar a exploração e otimização de novos medicamentos construídos a partir dos mesmos esqueletos básicos de amina.
Citação: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
Palavras-chave: funcionalização de aminas, transferência de átomo de hidrogênio, catálise por cobre, cianetação enantioseletiva, química medicinal