Clear Sky Science · pt
Duplas localizações genômicas e funções regulatórias do gene de MBD-2 com e sem NuRD em Caenorhabditis elegans que carece de metilação do DNA
Como vermes minúsculos reescrevem as regras do controle gênico
Nossas células usam marcas químicas no DNA e em proteínas para lembrar quais genes devem estar ligados ou desligados. Uma das marcas mais conhecidas, a metilação do DNA, está ausente em alguns animais — ainda assim eles crescem e se reproduzem normalmente. Este artigo investiga como um pequeno verme, Caenorhabditis elegans, gerencia o controle gênico sem metilação do DNA, revelando um sistema de backup surpreendentemente flexível que pode mudar a forma como pensamos sobre epigenética.
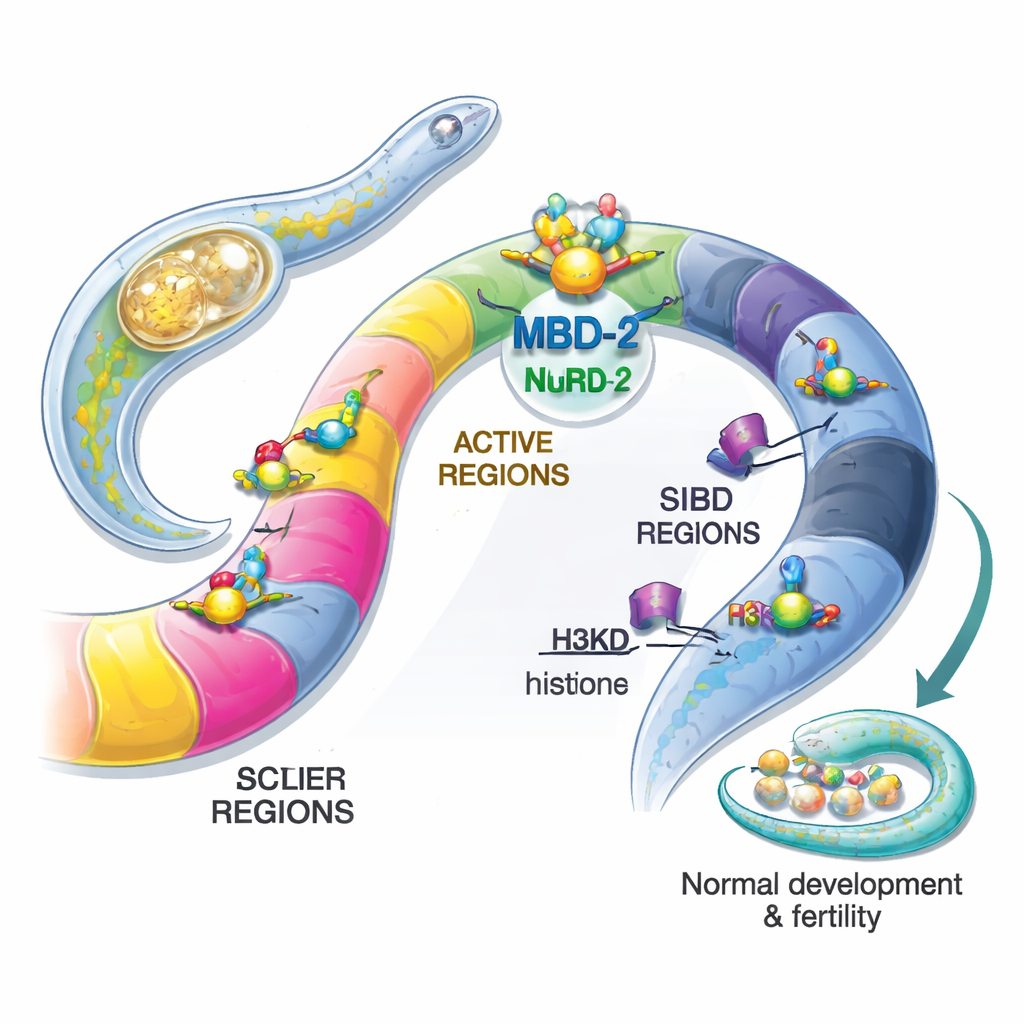
Uma marca de DNA ausente levanta uma grande questão
Em mamíferos, uma marca química chamada 5‑metilcitosina (5mC) ajuda a silenciar genes durante o desenvolvimento, na inativação do cromossomo X e na defesa contra elementos transponíveis. Proteínas chamadas MBD2 e MBD3 leem essas marcas e recrutam uma grande máquina proteica, o complexo NuRD, que pode remodelar e desativar trechos de cromatina. Estranhamente, muitos invertebrados, incluindo C. elegans e moscas-das-frutas, perderam a 5mC e as enzimas que a colocam — mas mantiveram uma proteína semelhante a MBD2/3. Isso levanta um enigma: por que conservar um “leitor de metilação do DNA” em um genoma que não usa mais metilação do DNA, e o que ele faz em vez disso?
Uma proteína andaime da qual os vermes não conseguem prescindir
Os autores focaram na versão do verme dessa proteína, chamada MBD‑2. Ao contrário de suas contrapartes em mamíferos, o MBD‑2 do verme perdeu o domínio clássico de ligação à metil‑citosina, mas manteve segmentos flexíveis e em espiral capazes de se conectar a outras proteínas. Ao marcar o MBD‑2 com marcadores fluorescentes, a equipe mostrou que ele se localiza nos núcleos de quase todas as células ao longo da vida do verme, consistente com um papel amplo na regulação gênica. Usando engenharia genética, eles então criaram vermes completamente desprovidos de MBD‑2, ou desprovidos apenas da região em espiral (coiled‑coil), que media o contato com o NuRD. Ambas as mutações causaram problemas severos: animais eram pequenos, se moviam mal, apresentavam estruturas reprodutoras malformadas e eram em grande parte estéreis. Isso demonstrou que o MBD‑2 é essencial para o desenvolvimento normal e para a fertilidade, mesmo na ausência de metilação do DNA.
Reconstruindo a máquina NuRD em um mundo sem metilação
Para verificar se o MBD‑2 do verme ainda atua com o NuRD, os autores purificaram MBD‑2 marcado de extratos de verme e identificaram seus parceiros por espectrometria de massa. A maioria dos componentes conhecidos do NuRD estava presente, confirmando que o MBD‑2 atua como um andaime central nesse complexo, assim como MBD2/3 faz em mamíferos. Quando a região coiled‑coil foi deletada, muitas dessas interações foram perdidas, especialmente as com proteínas que remodelam os nucleossomos. Ao mesmo tempo, um sequenciamento de RNA em larga escala revelou que mais de um quarto de todos os genes do verme alteraram sua atividade em mutantes para MBD‑2, com muito mais genes sendo ativados do que reprimidos. Esse padrão indica que o MBD‑2, frequentemente junto com o NuRD, age geralmente como um repressor para manter genes inadequados silenciosos, ao mesmo tempo em que ajuda a manter a atividade adequada de um subconjunto de genes fortemente expressos.
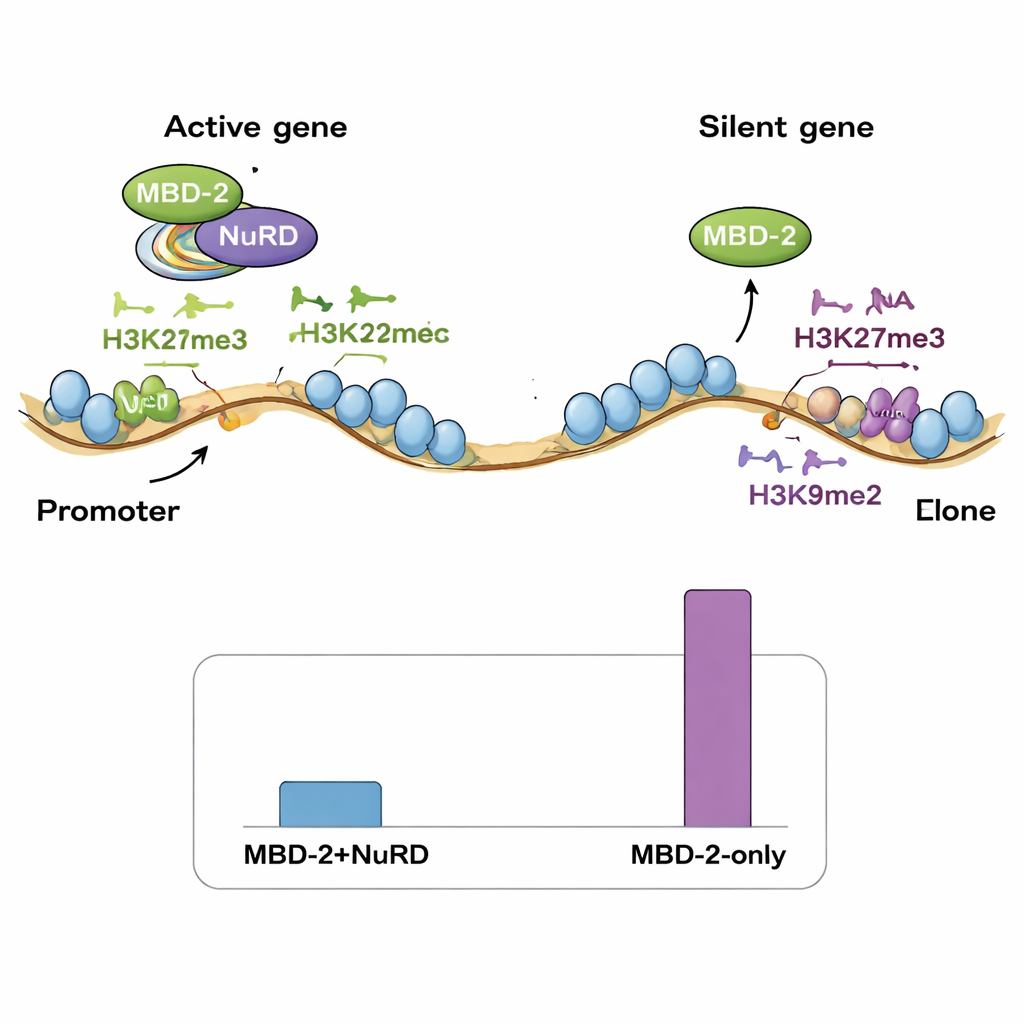
Dois modos de ligação ao genoma
Em seguida, a equipe mapeou onde o MBD‑2 se localiza ao longo do genoma usando ChIP‑seq, e comparou essas posições com mapas existentes de componentes do NuRD e várias marcas de histonas. Surpreendentemente, apenas uma pequena fração dos sítios de MBD‑2 se sobrepunha fortemente com proteínas do NuRD e marcas de cromatina aberta e ativa. A grande maioria dos sítios de MBD‑2 situava‑se em outros locais, nos “braços” cromossômicos ricos em marcas repressivas de histonas, como H3K27me3 e H3K9me2/3. Em outras palavras, o MBD‑2 mostra um comportamento duplo: em uma minoria de sítios ele viaja com o NuRD para afinar genes ativos, mas em muitos outros sítios ele se liga de forma independente em regiões que já estão silenciosas. O padrão de sua ligação dentro dos genes também importa — quando o MBD‑2 se concentra perto de inícios de genes, a perda da proteína tende a ativar esses genes, enquanto a ligação mais profunda nos corpos genéticos costuma estar associada à redução da expressão quando o MBD‑2 é removido.
Um backup evolutivo para a metilação do DNA perdida
Os autores propõem que, em espécies que perderam a metilação do DNA, marcas repressivas de histonas — especialmente H3K27me3 — podem ter se expandido para ocupar um nicho regulatório semelhante. O MBD‑2 do verme parece ter sido reaproveitado: em vez de ler 5mC no DNA, ele agora se associa a regiões de cromatina marcadas por modificações específicas de histonas, ao mesmo tempo em que ancora o complexo NuRD através de seus domínios conservados de interação proteica. Este trabalho mostra que um kit antigo de silenciamento gênico pode ser reconfigurado ao longo da evolução: a marca química no DNA pode desaparecer, mas a maquinaria proteica associada sobrevive ao mudar para sinais alternativos. Para não especialistas, a mensagem central é que a regulação gênica é notavelmente adaptável — as células podem perder uma marca epigenética importante e ainda assim manter o controle complexo de milhares de genes ao depender mais de outras marcas de cromatina e dos papéis versáteis de andaime de proteínas como o MBD‑2.
Citação: Tsui, H.N., Wong, C.Y.Y., Zheng, C. et al. Dual genomic localizations and gene regulatory functions of MBD-2 with and without NuRD in Caenorhabditis elegans which lacks DNA methylation. Nat Commun 17, 1875 (2026). https://doi.org/10.1038/s41467-026-68592-0
Palavras-chave: epigenética, cromatina, regulação gênica, C. elegans, modificação de histonas