Clear Sky Science · pt
Uma enzima mononuclear não‑heme altamente dinâmica para a biossíntese em dois passos de isonitrila
Como bactérias constroem ferramentas químicas exóticas
As isonitrilas são grupos químicos pequenos, mas potentes, que funcionam como canivetes suíços: podem sequestrar metais, reagir de várias maneiras diferentes e muitas vezes servem como “cabeça reativa” de antibióticos e toxinas naturais potentes. Algumas bactérias patogênicas, incluindo o agente da tuberculose Mycobacterium tuberculosis, adicionam isonitrilas a moléculas lipídicas para ajudá‑las a roubar metais do hospedeiro. Este artigo explora como uma de suas enzimas, chamada Rv0097, realiza essa transformação incomum e exigente em dois passos cuidadosamente coreografados.
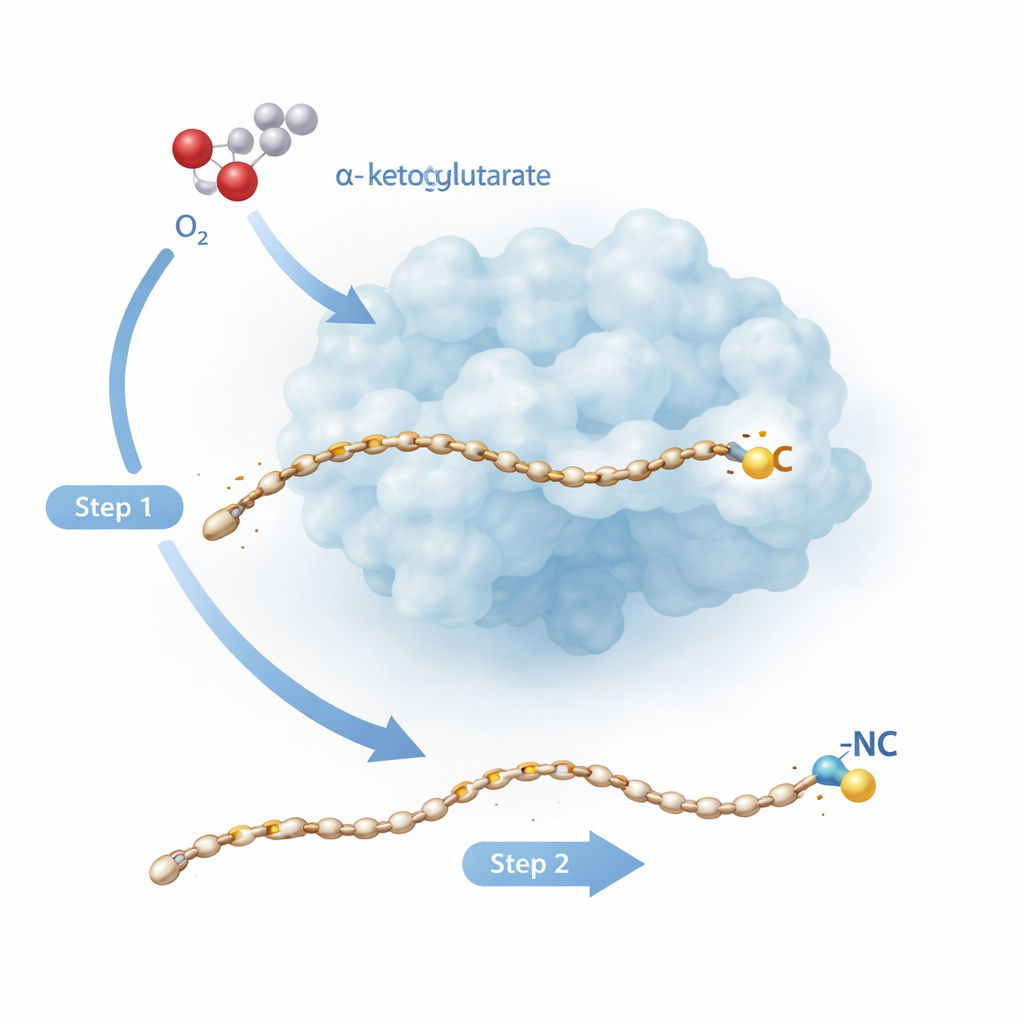
Uma reforma molecular em duas etapas
Rv0097 pertence a uma grande família de enzimas dependentes de ferro que normalmente executam tarefas mais simples, como adicionar oxigênio em um único ponto de uma molécula. Aqui, a tarefa é mais difícil: partindo de um bloco construtor “glicil–ácido graxo”, a enzima precisa criar um novo grupo isonitrila, com ambos os seus átomos-chave — o carbono e o nitrogênio — provindo do mesmo fragmento pequeno de glicina. Trabalhos anteriores com uma enzima relacionada, ScoE, sugeriram que isso não pode ser feito em um único passo. Em vez disso, são necessárias duas “meias‑ciclos” reacionais separados, cada um alimentado por uma espécie ferro–oxigênio formada quando a enzima rompe uma molécula assistente, o α‑cetoglutarato, e a combina com o oxigênio do ar. O novo estudo volta‑se para a enzima da tuberculose Rv0097 para observar, em resolução atômica, como uma enzima consegue encadear esses dois passos radicais no mesmo substrato sem perder o controle.
Congelando a enzima em ação
Usando cristalografia de raios X, os pesquisadores capturaram dezesseis instantâneos de alta resolução de Rv0097 em diferentes estados: vazia, ligada ao seu substrato gorduroso (uma molécula de dez carbonos chamada CADA), ligada ao auxiliador α‑cetoglutarato, e em combinações que imitam intermediários reacionais fugazes. Essas estruturas mostram que Rv0097 tem uma personalidade dupla. Em repouso, seu sítio ativo está em grande parte fechado, com um aminoácido chave (fenilalanina 102) alternando entre duas orientações que mantêm o bolso do longo rabo graxo seco e pronto para interação hidrofóbica. Quando o CADA se liga, esse resíduo se fixa em uma única orientação e a “cabeça” polar do substrato é ancorada por cadeias laterais carregadas, enquanto sua cauda oleosa se acomoda em um túnel apertado. Mutar esse par de resíduos que faz a vedação (F102 e uma glicina próxima, G204) ou bloqueia o bolso ou permite a entrada de água em excesso, reduzindo drasticamente a atividade e alterando quais comprimentos de cadeia a enzima prefere.
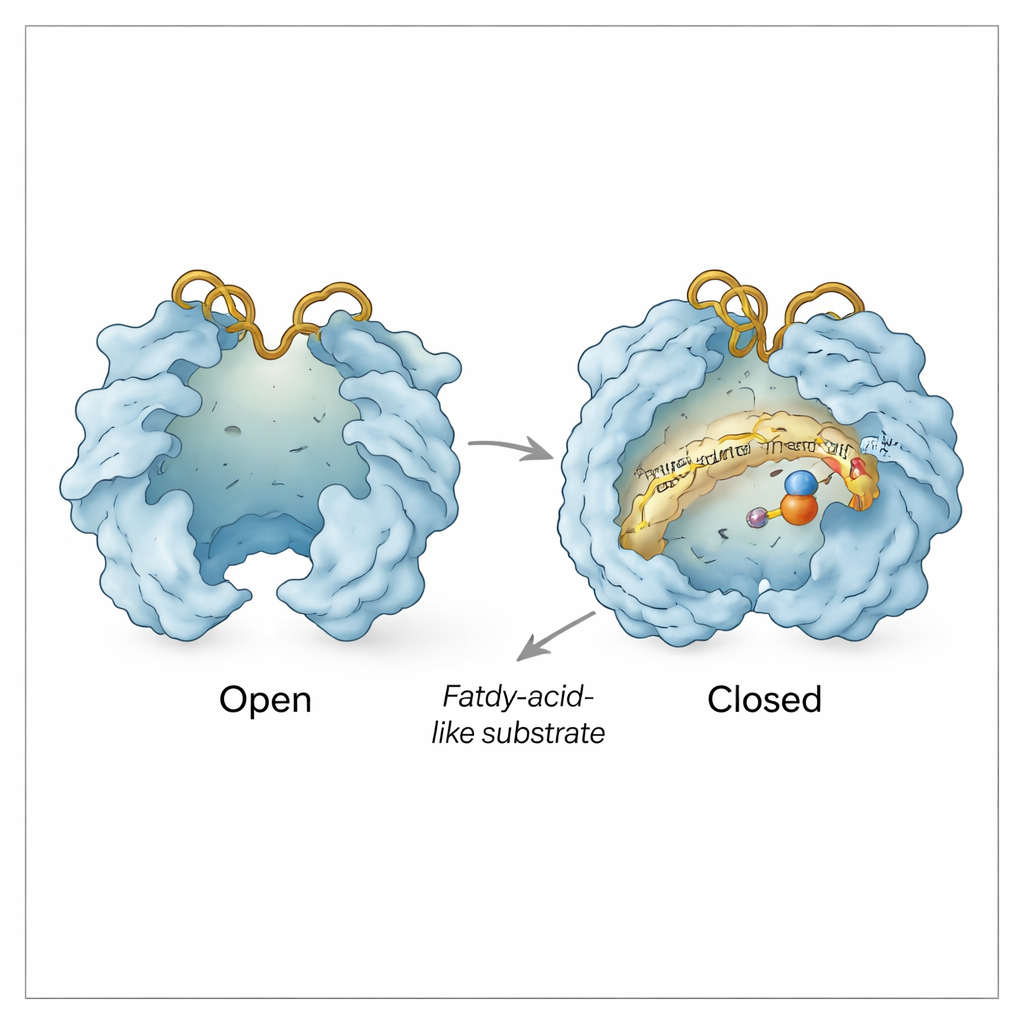
Tampas móveis e alças dinâmicas
Além do bolso do substrato, Rv0097 comporta‑se como uma pequena máquina com portas móveis. A equipe observou conformações “aberta” e “fechada” nas quais duas regiões em forma de tampa se abrem ou se fecham sobre o sítio ativo. A abertura expõe o centro de ferro e cria um caminho para o α‑cetoglutarato e o substrato entrarem; o fechamento protege a química da água circundante assim que a reação está em andamento. Duas alças flexíveis de superfície, chamadas de alça His e alça Arg, em referência à histidina e à arginina que carregam, atuam como uma trava adicional. Em algumas estruturas, essas alças se movem para dentro de modo que o resíduo de arginina possa capturar o α‑cetoglutarato; em outras, se afastam, aparentemente criando um canal lateral pelo qual fragmentos assistentes gastos (succinate e dióxido de carbono) podem sair e um novo α‑cetoglutarato pode entrar para a segunda etapa — tudo isso enquanto o intermediário derivado do substrato permanece preso no mesmo lugar.
Protegendo um intermediário frágil
Ensaios bioquímicos corroboram esse panorama estrutural. A primeira metade da reação converte CADA em um intermediário imina altamente reativo que rapidamente se degradaria se escapasse para a solução. Ao aprisionar quimicamente o produto de decomposição, os autores mostram que a maior parte desse intermediário só é detectada quando a enzima ainda está presente, o que implica que ele permanece ligado e protegido dentro de Rv0097 entre os dois meios‑reações. As estruturas explicam como: reposicionamentos sutis das alças His e Arg, juntamente com pequenos deslocamentos de resíduos vizinhos, parecem selar o intermediário em uma cavidade protegida enquanto ainda permitem que pequenas moléculas como α‑cetoglutarato, succinato e dióxido de carbono troquem através de canais controlados.
Por que isso importa para TB e além
Em conjunto, esses resultados revelam Rv0097 como uma linha de montagem de proteína única, altamente dinâmica, que usa química à base de ferro duas vezes seguidas no mesmo substrato sem nunca liberar um produto perigosamente intermediário. Para as bactérias causadoras da tuberculose, essa precisão sustenta a fabricação de moléculas decoradas com isonitrila que as ajudam a obter metais essenciais dentro do corpo, e estudos genéticos indicam que a via é importante para sua sobrevivência durante a infecção. Para químicos e projetistas de fármacos, o trabalho oferece um roteiro para a engenharia de enzimas relacionadas para construir novos compostos contendo isonitrila, e sugere que interferir nas tampas e portões móveis de Rv0097 pode ser uma estratégia para desenvolver novos antibióticos.
Citação: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Palavras-chave: biossíntese de isonitrila, enzima não‑heme de ferro, Mycobacterium tuberculosis, dinâmica enzimática, produtos naturais quelantes de metal