Clear Sky Science · pt
Disrupção da homeostase do ferro sensibiliza câncer pancreático à eletroporação irreversível
Usando Eletricidade e Ferro contra um Câncer Letal
O câncer pancreático é um dos mais difíceis de tratar e mesmo terapias locais agressivas frequentemente não impedem sua recidiva. Este estudo investiga uma nova maneira de tornar um procedimento já existente — a eletroporação irreversível, que elimina tumores usando pulsos elétricos curtos e poderosos — mais eficaz e seguro. Ao perturbar de forma inteligente como as células cancerosas lidam com o ferro, os pesquisadores mostram que é possível forçar as células sobreviventes a um tipo destrutivo de morte, potencialmente reduzindo a chance de o tumor voltar.
Por Que Só os Pulsos Elétricos Não São Suficientes
A eletroporação irreversível (IRE) trata tumores inserindo eletrodos finos no tecido tumoral ou ao redor dele e disparando pulsos rápidos de alta voltagem. Esses pulsos criam furos permanentes nas membranas das células, matando muitas células cancerosas e provocando uma resposta imune. Mas o campo elétrico não é perfeitamente uniforme. Áreas que recebem pulsos ligeiramente mais fracos podem deixar células cancerosas vivas, e esses sobreviventes podem originar um novo tumor. Quando a equipe examinou de perto células de câncer pancreático e tumores de camundongos expostos a um campo elétrico subletal, descobriram que, em vez de morrer por um processo dependente de ferro chamado ferroptose, essas células ativaram um amplo programa antioxidante. Genes protetores chave, incluindo aqueles que ajudam a neutralizar danos relacionados ao ferro, foram ativados, permitindo que as células resistissem à agressão e se recuperassem.
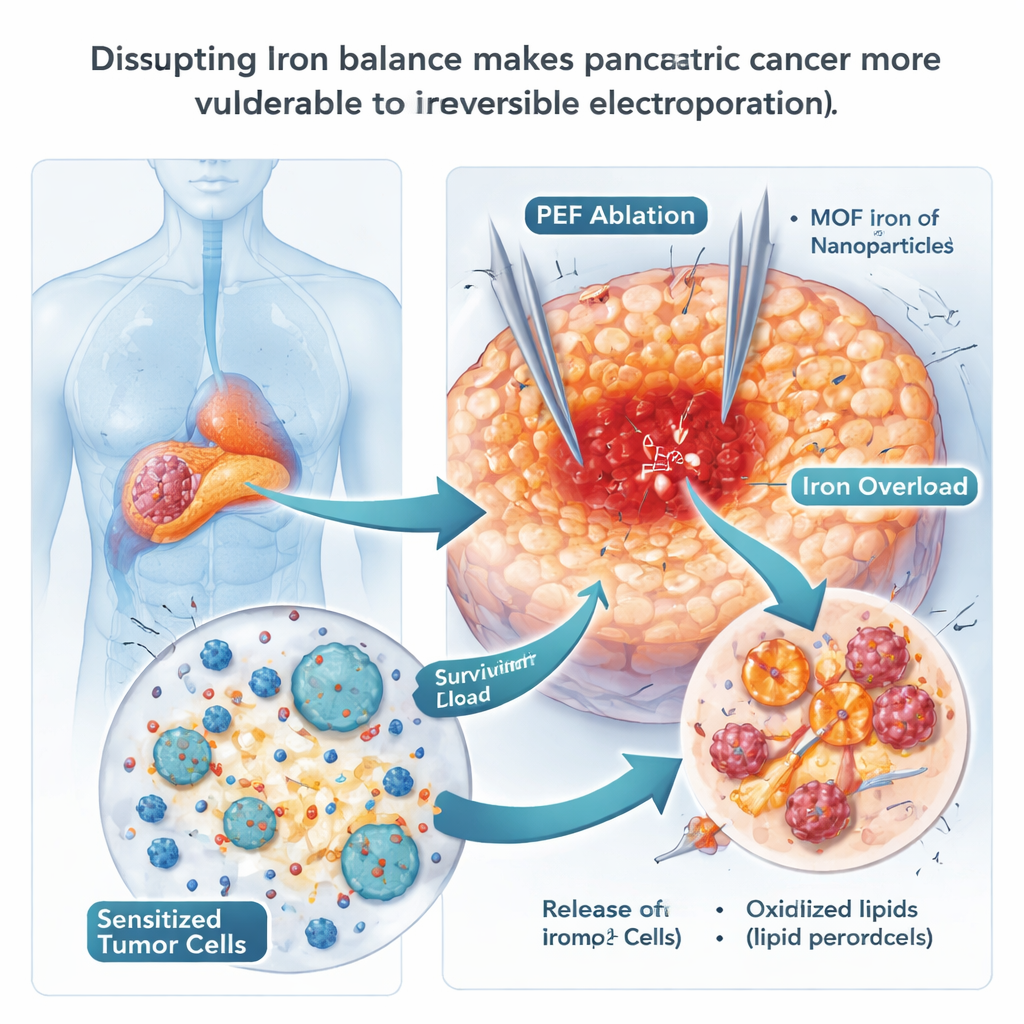
Usando Nanopartículas de Ferro para Empurrar as Células à Destruição
Como a ferroptose depende do ferro, os cientistas testaram se nanopartículas ricas em ferro poderiam forçar as células cancerosas além do limite. Eles usaram partículas de estrutura metal-orgânica contendo ferro (MOF-Fe), projetadas para liberar ferro rapidamente dentro dos compartimentos ácidos das células. Em culturas, células de câncer pancreático que incorporaram essas partículas acumularam ferro livre e lipídios oxidizados em suas membranas — sinais clássicos de ferroptose — e formaram muito menos colônias. Em camundongos, a combinação de MOF-Fe com IRE retardou a recidiva tumoral por mais tempo do que qualquer um dos tratamentos isolados, e os tumores mostraram mais sinais de dano oxidativo. Contudo, esse benefício foi temporário: após cerca de três semanas, os tumores começaram a se recuperar, sugerindo que o câncer encontrou uma maneira de se adaptar à sobrecarga de ferro.
Mirando no “Cofre” do Ferro da Célula
Para entender essa resistência, a equipe analisou quais proteínas mudaram após o tratamento com MOF-Fe. Um destaque foi a cadeia pesada da ferritina 1 (FTH1), parte do complexo de armazenamento de ferro da célula — o equivalente molecular de um cofre à prova de incêndio para o ferro em excesso. Quando os níveis de FTH1 foram aumentados experimentalmente, as células cancerosas ficaram mais resistentes à ferroptose; quando FTH1 foi reduzida, tornaram-se mais vulneráveis. Isso apontou a FTH1 como um escudo central contra a morte mediada por ferro. Os pesquisadores então criaram uma molécula desenhada, C20U4V, construída a partir do ácido araquidônico (um lipídio altamente oxidação-sensível) ligado a um arcabouço PROTAC que direciona proteínas específicas para a maquinaria celular de degradação. Na presença de MOF-Fe, C20U4V ligou-se à ferritina e recrutou sua marcação para destruição, reduzindo drasticamente os níveis de FTH1 e impedindo que a célula isolasse o ferro com segurança.
De Placas de Cultura a Mini-tumores e Camundongos
Quando MOF-Fe e C20U4V foram combinados, células de câncer pancreático mostraram maior estresse oxidativo, mais lipídios de membrana danificados, mitocôndrias mais comprometidas e capacidade muito reduzida de regrowth. Essa sinergia também apareceu em organoides tridimensionais derivados de pacientes — pequenas estruturas semelhantes a tumores cultivadas a partir de amostras humanas — onde a dupla farmacológica colapsou o tamanho e o número dos organoides. Como C20U4V é lipofílico e pouco solúvel em água, a equipe o encapsulou em micelas sensíveis a espécies reativas de oxigênio (M-C20U4V) que circulam na corrente sanguínea e podem liberar o fármaco em tecido tumoral estressado e danificado. Em modelos murinos com tumores pancreáticos implantados sob a pele e no próprio pâncreas, a combinação tripla de IRE, MOF-Fe e M-C20U4V encolheu tumores de forma muito mais eficaz e prolongou a sobrevivência em comparação com tratamentos singulares ou duplos. Os tumores tratados exibiram menos células em divisão, mais marcadores de ferroptose e maior infiltração por células T e outras células imunes, indicando que a estratégia não apenas mata células cancerosas diretamente, mas também ajuda o sistema imunológico a reconhecer e atacar o tumor.
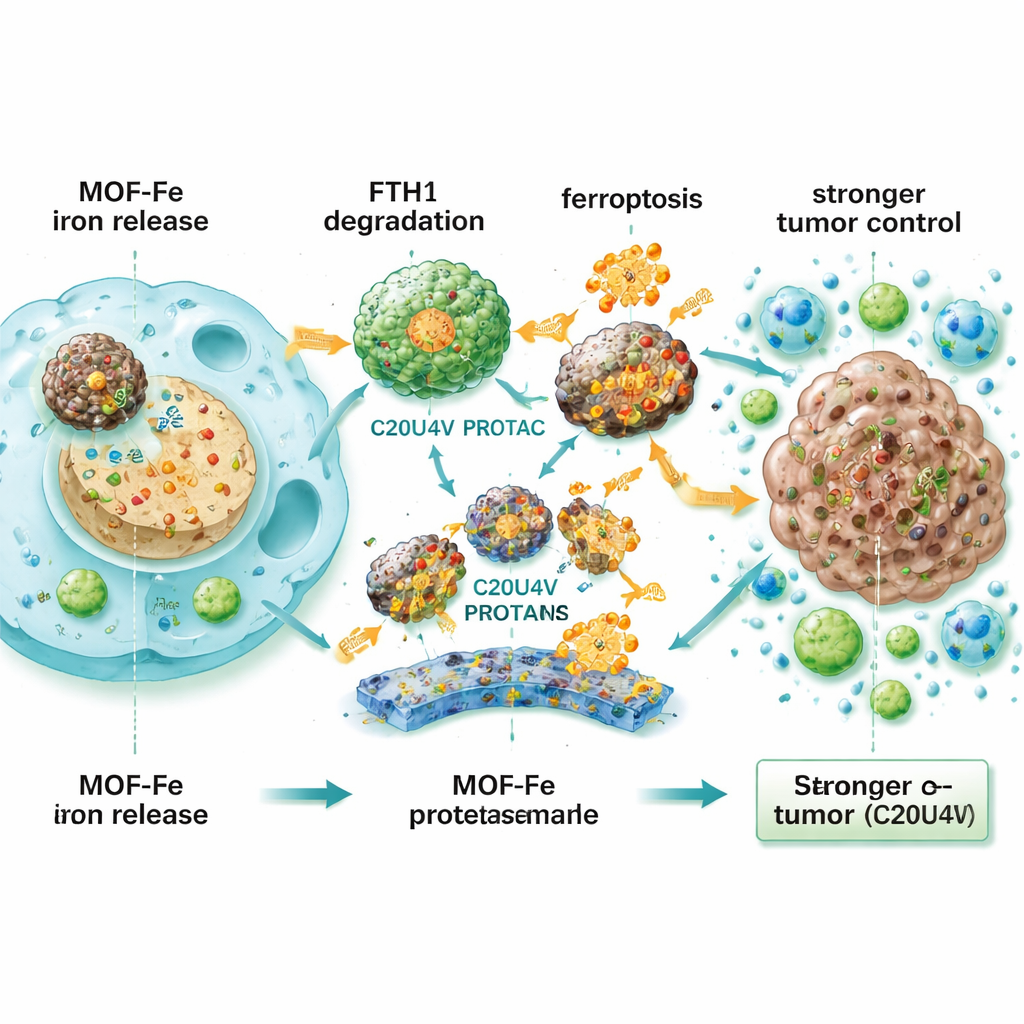
O Que Isso Pode Significar para Pacientes
Para um público não especializado, a ideia central é simples: tumores pancreáticos frequentemente escapam após ablação por pulsos elétricos porque algumas células cancerosas sobrevivem e rapidamente se adaptam. Este trabalho demonstra que sobrecarregar essas células com ferro e, simultaneamente, desabilitar seu “cofre” de segurança do ferro pode forçá-las a entrar em um estado autodestrutivo que têm dificuldade em resistir. Embora essa abordagem ainda esteja em fase experimental e exija testes extensivos de segurança e viabilidade em humanos, sugere que ajustar finamente como os tumores manejam um elemento básico como o ferro pode transformar um tratamento local imperfeito em um golpe mais decisivo contra um dos cânceres mais letais.
Citação: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Palavras-chave: câncer pancreático, eletroporação irreversível, ferroptose, nanopartículas de ferro, terapia PROTAC