Clear Sky Science · pt
HIF sustenta um circuito regulatório transcricional da expressão de EPAS1 em carcinoma de células claras do rim
Por que o câncer de rim merece atenção redobrada
O carcinoma de células claras do rim é a forma mais comum de câncer renal, e muitos pacientes hoje recebem medicamentos que bloqueiam uma proteína chamada HIF‑2α. Essas drogas podem reduzir tumores, mas não funcionam igualmente bem para todos. Este estudo faz uma pergunta simples, porém importante: o que faz com que alguns tumores renais produzam tanto HIF‑2α, e entender esse “interruptor” pode nos ajudar a prever quem se beneficiará mais do tratamento e como projetar novas terapias?
O sensor de oxigênio que sai do controle
Em células renais saudáveis, uma proteína de segurança chamada VHL mantém os fatores sensores de oxigênio, conhecidos como HIFs, sob controle rigoroso. Quando o oxigênio está disponível, VHL marca as proteínas HIF para destruição, impedindo que ativem genes que promovem a formação de vasos e a divisão celular. No câncer renal de células claras, o VHL geralmente é perdido ou danificado. Como resultado, um membro da família HIF, o HIF‑2α (codificado pelo gene EPAS1), escapa da destruição e se acumula. Trabalhos anteriores mostraram que alta atividade de HIF‑2α está ligada a crescimento tumoral mais rápido e piores desfechos, e que bloquear HIF‑2α pode retardar ou interromper tumores em alguns pacientes. Contudo, os passos moleculares que aumentam a atividade do gene EPAS1 em tumores renais não eram bem compreendidos.
Um interruptor de DNA oculto para um gene cancerígeno
Usando amostras tumorais de pacientes, dados de célula única e modelos de células cancerosas, os autores mostram que o RNA mensageiro de HIF‑2α é marcadamente maior em tumores renais de células claras do que em tecido renal normal ou outros tipos de tumor renal. Em seguida, eles escaneiam a região do EPAS1 no genoma buscando marcas químicas e estruturais que sinalizam DNA regulatório ativo. Isso revela um enhancer poderoso — uma espécie de interruptor gênico de longa distância — localizado cerca de 70.000 pares de bases upstream de EPAS1 que é especificamente ativo em tumores de células claras. Nas células tumorais, a cromatina nesse enhancer está aberta, decorada com marcas de ativação e fisicamente faz loop para contatar o promotor de EPAS1, enquanto em células do túbulo renal normal essa região é largamente silenciosa. A atividade desse enhancer se correlaciona com níveis mais altos de EPAS1 em grandes conjuntos de dados de câncer. 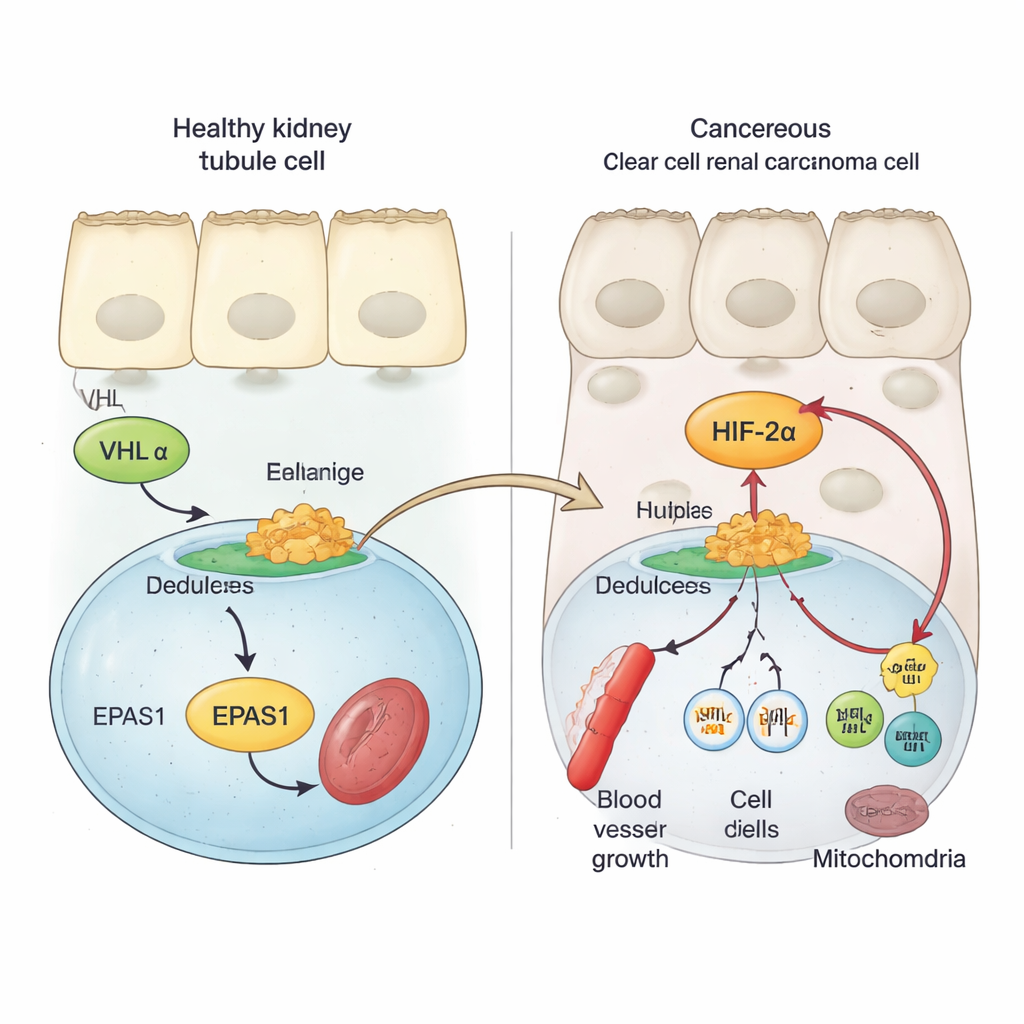
Um circuito autorreforçador impulsionado por fatores de identidade renal
O estudo mostra que as proteínas HIF fazem mais do que responder à falta de oxigênio — elas na verdade ajudam a impulsionar sua própria produção. Quando os pesquisadores restauram o VHL ou removem uma proteína parceira chave do HIF (HIF‑1β), os níveis de EPAS1 caem e o enhancer se torna menos acessível. Mapeamentos diretos das interações proteína–DNA mostram que HIF se liga a duas regiões do enhancer upstream de EPAS1, incluindo o enhancer específico de células claras. Em células tumorais renais, esse enhancer também é ocupado por PAX8 e HNF‑1β, fatores de transcrição que ajudam a definir a identidade das células renais e são conhecidos por sustentar o crescimento tumoral. Destruir PAX8 ou HNF‑1β, ou mutar seus sítios de ligação dentro do enhancer, reduz o RNA e a proteína de HIF‑2α e enfraquece a atividade do enhancer. Em conjunto, esses achados revelam um circuito autorregulador: HIF‑2α, atuando com fatores da linhagem renal, aumenta a atividade de um enhancer de EPAS1, que por sua vez impulsiona mais produção de HIF‑2α.
Risco genético e comportamento tumoral convergem no mesmo circuito
A região de EPAS1 há muito é apontada em estudos de associação genômica como um ponto quente para risco de câncer renal, com certas variantes herdadas ligadas a taxas mais altas de câncer e a mutações de VHL nos tumores. Ao combinar dados genéticos com medidas de expressão gênica, os autores mostram que indivíduos portadores da versão de alto risco de uma variante chave de EPAS1 tendem a apresentar níveis mais elevados de HIF‑2α em seus tumores — e mesmo em células do túbulo renal normal quando HIF é experimentalmente estabilizado. Isso sugere que diferenças herdadas no DNA podem ajustar quão fortemente o enhancer responde, predispondo alguns rins a aumentar HIF‑2α mais intensamente após a perda de VHL. Experimentos em células de glioblastoma mostram que o mesmo enhancer também pode ser ativado em certos tumores cerebrais, insinuando que esse módulo regulatório pode ser reutilizado em outros cânceres onde HIF‑2α é importante. 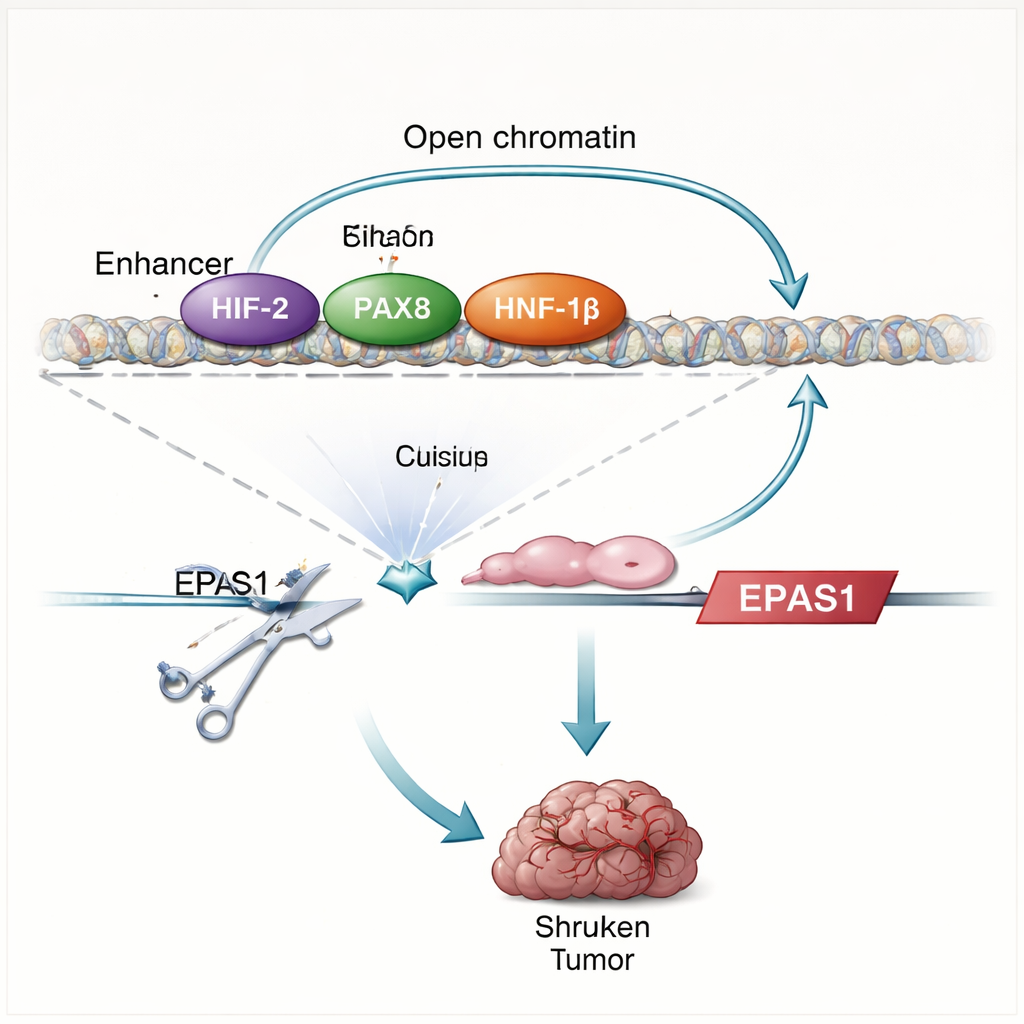
Quebrando o circuito para deter o crescimento tumoral
Para testar o quão essencial é esse enhancer, a equipe usa edição genômica por CRISPR para danificar os motivos de ligação de HIF dentro dele em linhagens de câncer renal e em células tumorais frescas de pacientes. Esse corte reduz o RNA de HIF‑2α em cerca de um terço a metade, diminui os níveis de genes-alvo bem conhecidos de HIF‑2α, como CCND1 e VEGFA, e enfraquece o programa gênico mais amplo de hipóxia. Quando células editadas são implantadas em camundongos, elas em grande parte não formam tumores, em nítido contraste com as células controle. O padrão de mudanças gênicas após a disrupção do enhancer espelha de perto os efeitos de bloquear diretamente HIF‑2α com um fármaco clínico, enfatizando que esse único elemento de DNA é um motor importante da via de HIF‑2α nesses cânceres.
O que isso significa para pacientes e terapias
Para o público não especializado, a mensagem central é que os autores descobriram um interruptor de DNA autoamplificador que mantém uma proteína promotora de câncer importante, HIF‑2α, ligada em tumores renais de células claras. Esse interruptor depende tanto da perda do freio de segurança VHL quanto de proteínas auxiliares específicas do rim, e é influenciado por variantes genéticas herdadas. Como o enhancer é altamente ativo em muitos tumores de células claras e está fortemente ligado à intensidade da via HIF‑2α, medir sua atividade — ou direcioná‑lo diretamente — poderia ajudar a identificar pacientes que se beneficiarão mais dos inibidores atuais de HIF‑2α e oferecer novas formas de desligar essa via quando os tumores se tornam resistentes aos medicamentos.
Citação: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Palavras-chave: carcinoma de células claras do rim, HIF-2α, enhancer de EPAS1, mutação de VHL, genética do câncer renal