Clear Sky Science · pt
Reação CuAAC interrompida atropoesletiva usando diaryliodônios cíclicos
Por que essa nova química importa
Há muito tempo os químicos contam com uma reação “click” simples para conectar blocos moleculares de forma rápida e limpa — um recurso que sustenta desde a descoberta de fármacos até materiais autorreparáveis. Este artigo descreve uma mudança inteligente nessa reação clássica que permite construir moléculas tridimensionais mais complexas com uma quiralidade definida — estruturas altamente valorizadas em medicamentos modernos e materiais avançados.
Dar uma nova função a uma reação click clássica
O ponto de partida é a cicloadição azida–alquino catalisada por cobre, frequentemente chamada simplesmente de CuAAC. Ela une dois componentes pequenos — uma azida e um alquino — formando um anel de cinco membros chamado triazol sob condições brandas e com notável confiabilidade. Tradicionalmente, uma vez que o cobre ajuda a formar o anel de triazol, a reação termina aí. Nos últimos anos, contudo, os químicos aprenderam a “interromper” esse processo, capturando um intermediário cobre–triazol fugaz com um terceiro parceiro para construir produtos mais elaborados. Até agora, essas interrupções não conseguiam controlar a quiralidade molecular de forma geral, limitando sua utilidade para montar moléculas quirais sofisticadas.
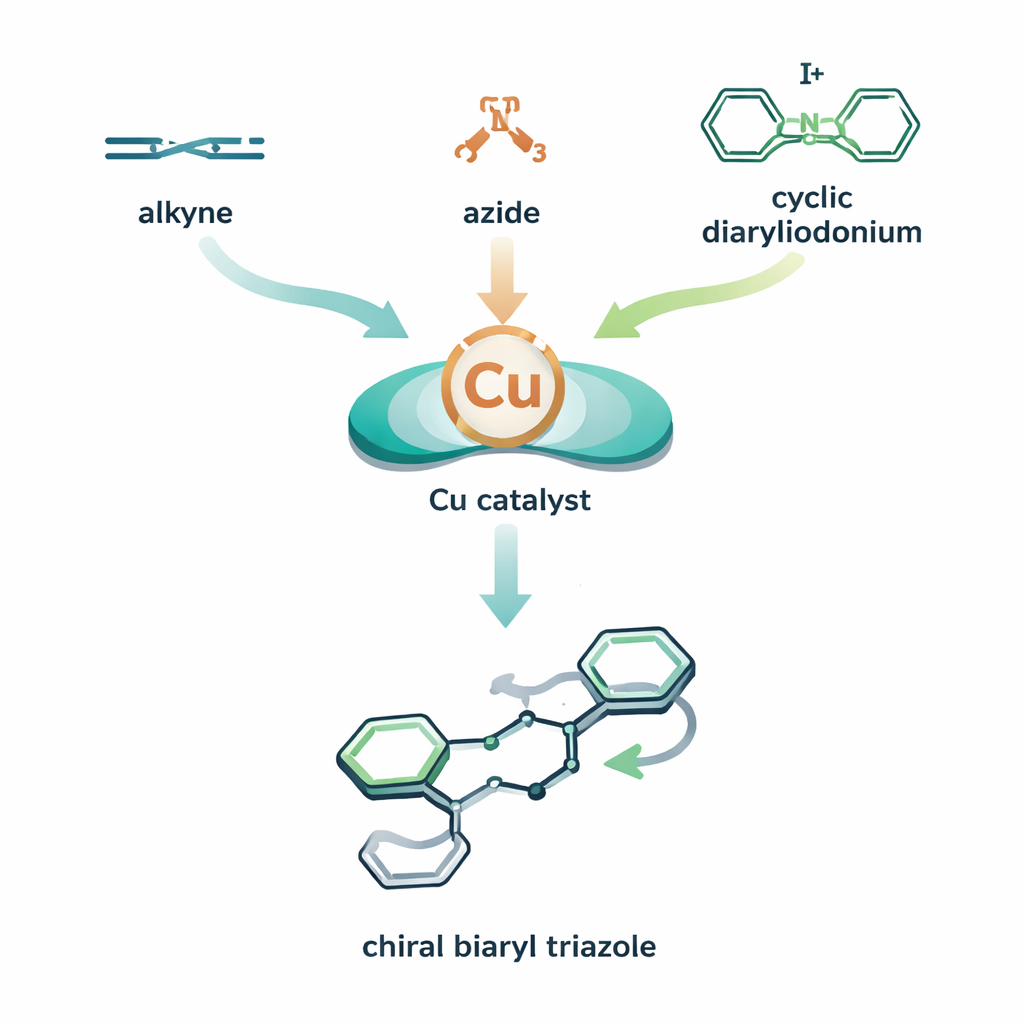
Um quebra-cabeça molecular de três peças com uma reviravolta
Os autores combinam dois ciclos de reação à base de cobre em um único processo orquestrado. Em seu plano, um catalisador de cobre primeiro ajuda o alquino e a azida a formarem um intermediário cobre–triazol. Antes que esse intermediário seja neutralizado, um terceiro componente — uma molécula em anel, altamente reativa e contendo iodo, chamada diaryliodônio cíclico — é introduzido. O cobre insere-se nesse anel e então o abre, costurando um de seus anéis aromáticos ao triazol. O resultado é um triazol bifenílico: dois sistemas em anel ligados por uma ligação que pode funcionar como um eixo quiral, semelhante a uma hélice que pode torcer para a esquerda ou para a direita. Ao parear o cobre com um ligante quiral cuidadosamente escolhido, a equipe viésa o processo para que uma torção seja formada muito mais que a outra, alcançando alta atropoesletividade (controle sobre qual “mão” axial é formada).
Testando quão flexível e confiável o método é
Para entender quão geral essa reação poderia ser, os pesquisadores variaram sistematicamente cada um dos três blocos de construção. Demonstraram que muitos alquinos diferentes, incluindo aqueles com anéis ricos em elétrons, pobres em elétrons e heteroaromáticos, podem participar mantendo bons rendimentos e forte preferência por uma forma quiral. Certas substituições volumosas melhoraram a seletividade, mas podiam reduzir o rendimento, revelando um compromisso entre estérica e eficiência. Os parceiros azida funcionaram melhor quando derivados de grupos éster ou amida simples ou de posições benzílicas, e uma variedade desses azidas entregou produtos quirais fortemente enriquecidos. O componente diaryliodônio cíclico também pôde ser afinado: algumas substituições preservaram tanto o rendimento quanto a seletividade, enquanto outras, especialmente próximas ao centro reativo de iodo, retardaram a reação ou reduziram seu desempenho. No geral, o estudo forneceu uma ampla coleção de novos triazóis bifenílicos atropoisoméricos acessíveis em uma etapa.
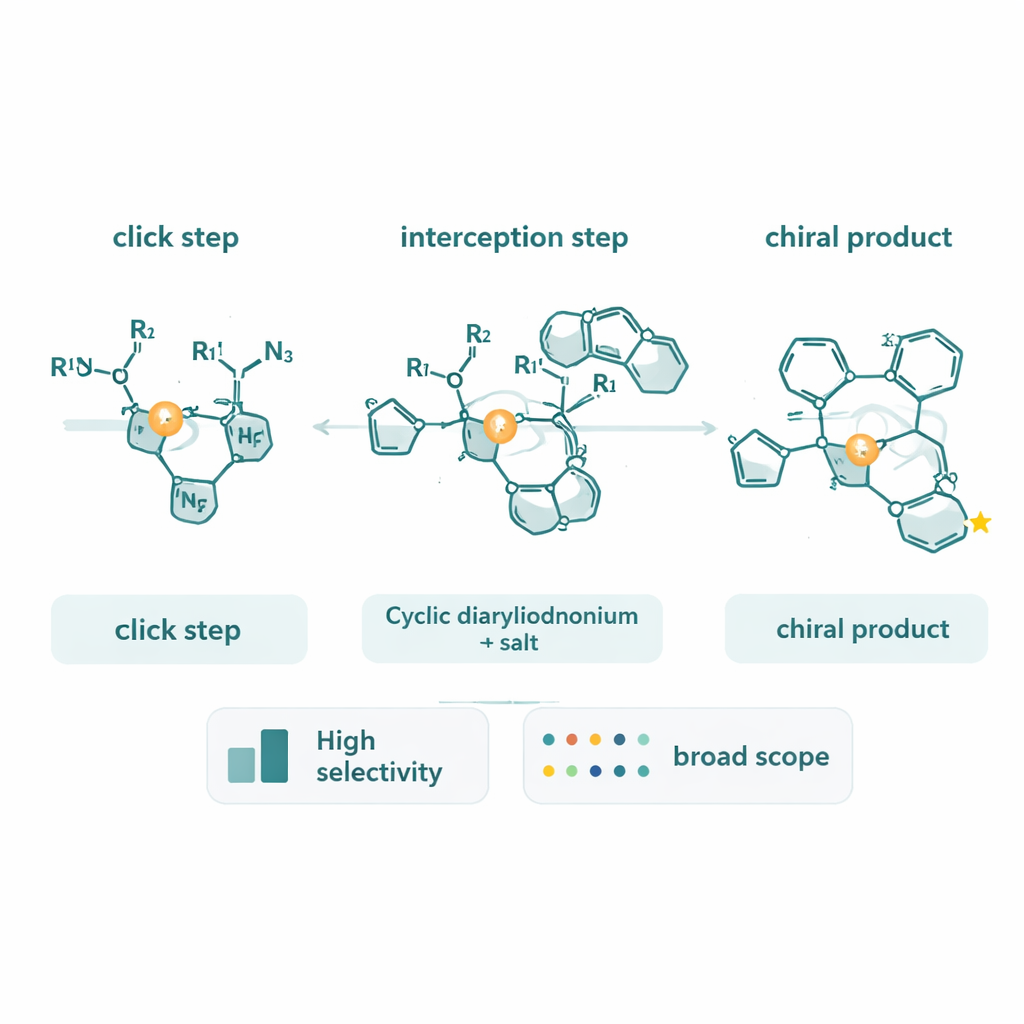
Espiando por dentro a reação
Além de sintetizar novas moléculas, a equipe dedicou esforço substancial para descobrir como a reação realmente funciona. Usando alcinos marcados com deutério, observaram um incomum efeito isotópico cinético inverso, que aponta para uma etapa determinante de velocidade na qual o carbono do alquino muda seu caráter de ligação em vez de simplesmente quebrar uma ligação C–H. Análises de progresso da reação baseadas em calorimetria mostraram que a velocidade da reação depende fortemente das concentrações do alquino e da azida, mas apenas fracamente do diaryliodônio cíclico. Essas medidas sustentam um quadro no qual a formação e transformação do complexo cobre–triazol, e sua adição oxidativa no anel do diaryliodônio, em conjunto determinam o ritmo da reação. Eles também descobriram que os próprios produtos triazóis quirais podem se ligar ao cobre e desacelerar o catalisador, sugerindo vias para otimizar ainda mais o sistema.
O que isso significa para o futuro
Em termos práticos, os pesquisadores ensinaram a uma reação click bem conhecida um novo truque: em vez de simplesmente juntar duas peças, ela agora ajuda a montar três componentes em moléculas complexas, semelhantes a hélices, escolhendo quase exclusivamente uma torção preferida. Isso fornece uma rota escalável para triazóis bifenílicos quirais, estruturas valiosas como potenciais fármacos, catalisadores e materiais funcionais. As percepções mecanísticas — especialmente sobre como o intermediário chave é interceptado e como o produto pode envenenar o catalisador — oferecem um roteiro para projetar versões ainda mais eficientes e seletivas dessa química. Para não especialistas, a principal conclusão é que uma ferramenta molecular tipo “Lego” já poderosa acaba de ficar mais versátil, permitindo aos químicos construir formas mais intrincadas e úteis com controle fino sobre sua forma tridimensional.
Citação: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
Palavras-chave: química click, catálise por cobre, bifeno quiral, atropoísomero, triazol