Clear Sky Science · pt
Biomarcadores de resposta ao palbociclib neoadjuvante mais anastrozol em câncer de mama receptor de estrogênio‑positivo/HER2‑negativo resistente à terapia endócrina: um ensaio de fase 2
Por que esta pesquisa importa para pacientes e famílias
Muitas mulheres com uma forma comum de câncer de mama respondem bem inicialmente a medicamentos que bloqueiam hormônios, mas seus tumores acabam se tornando resistentes e voltam a crescer. Este estudo investiga uma questão urgente: adicionar um medicamento mais recente que bloqueia o ciclo celular à terapia hormonal padrão pode ajudar nesses casos difíceis de tratar, e é possível identificar sinais no tumor que prevejam quem vai, ou não, se beneficiar?
Um olhar mais atento sobre cânceres de mama persistentes
O ensaio concentrou‑se em cânceres de mama receptor de estrogênio–positivo e HER2‑negativo, o subtipo mais frequente. As 34 pacientes já haviam recebido a terapia hormonal padrão pré‑operatória (um inibidor de aromatase) mas ainda apresentavam crescimento ativo das células tumorais, ou seja, o câncer era considerado “resistente à terapia endócrina”. Os pesquisadores então trataram essas pacientes antes da cirurgia com a combinação do hormônio anastrozol e do bloqueador do ciclo celular palbociclib. Mediram a velocidade de divisão das células tumorais usando um marcador chamado Ki67. Se o Ki67 caísse para níveis muito baixos após duas semanas, o tumor era considerado em “parada completa do ciclo celular”, indicando que a divisão das células cancerosas havia sido efetivamente interrompida.
Quem respondeu à combinação medicamentosa?
Entre as 33 pacientes cujos tumores puderam ser avaliados por completo, 57,6% atingiram parada completa do ciclo celular após apenas duas semanas do tratamento combinado. Quando se usou um limiar mais moderado — classificando os tumores como “sensíveis” se o Ki67 caísse abaixo de 10% — cerca de dois terços dos tumores foram considerados responsivos. Pacientes cujos tumores continuaram altamente ativos no Ki67 tendiam a ter cânceres mais agressivos: maior grau, tamanho maior e níveis iniciais de Ki67 mais altos. Elas também tinham maior probabilidade de pertencer a subtipos moleculares chamados “não‑luminais”, que geralmente se comportam de forma mais agressiva do que os tumores clássicos impulsionados por hormônio do tipo “luminal A”.
O que faz alguns tumores resistirem ao tratamento?
A equipe foi além das taxas simples de resposta e analisou profundamente as amostras tumorais usando sequenciamento de DNA, sequenciamento de RNA e perfil proteico. Tumores resistentes não foram definidos por uma única mutação; em vez disso, mostraram um padrão de “circuitaria hiperativa”. Em comparação com tumores sensíveis, os cânceres resistentes apresentavam sinalização do receptor de estrogênio atenuada, mas maior atividade em vias que impulsionam a divisão e o crescimento celular, como genes do ciclo celular, a via de crescimento mTOR e várias redes inflamatórias e relacionadas ao interferon. Também exibiam níveis mais altos de “freios” imunes, conhecidos como pontos de verificação imunológicos, incluindo genes como IDO1 e PD‑L1 que podem ajudar os tumores a escapar das defesas do organismo.
Das vias a possíveis novos tratamentos
Para testar se essas vias hiperativas poderiam ser usadas contra o câncer, os pesquisadores criaram modelos celulares em laboratório que se tornaram resistentes a inibidores de CDK4/6 como o palbociclib. Essas células resistentes mostraram a mesma assinatura de sinalização aumentada do ciclo celular e interferon/inflamatória observada nos tumores das pacientes. Quando expostas a drogas que bloqueiam a sinalização JAK‑STAT — uma rota chave a jusante do interferon — um medicamento, pacritinibe, foi particularmente eficaz em retardar o crescimento de células resistentes e de organoides tumorais derivados de pacientes. Isso sugere que combinar inibidores de CDK4/6 com certos medicamentos que visam JAK pode ser uma estratégia promissora para pacientes cujos cânceres driblaram as combinações atuais.
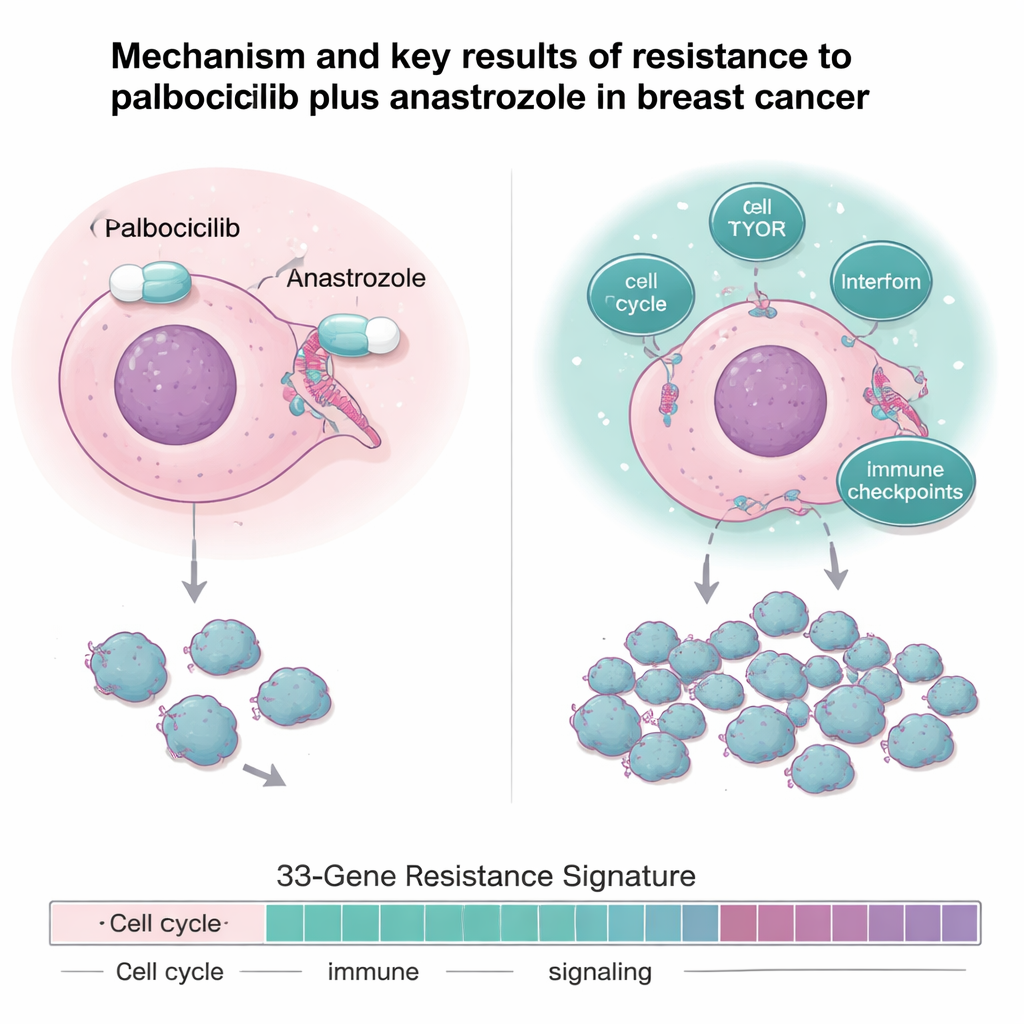
Uma impressão genética que prevê o resultado
Ao comparar tumores sensíveis e resistentes em dois ensaios relacionados, os investigadores construíram uma “assinatura de resistência” de 33 genes que captura genes envolvidos na divisão celular, reparo de DNA, sinalização de crescimento, metabolismo e respostas imunes/inflamatórias. Essa impressão genética foi muito precisa ao distinguir tumores sensíveis de resistentes no ensaio. Importante: quando o mesmo padrão de 33 genes foi aplicado a um grupo independente de 151 pacientes com câncer de mama metastático tratados na prática clínica com inibidores de CDK4/6 mais terapia hormonal, aqueles cujos tumores apresentaram pontuação alta para a assinatura de resistência tiveram tempo mais curto até a progressão da doença e sobrevida global reduzida. Em outras palavras, esse padrão genético medido antes do tratamento pode identificar pacientes menos propensos a se beneficiar por muito tempo dos regimes padrão baseados em CDK4/6.
O que isso significa para o cuidado futuro
Para pessoas enfrentando câncer de mama receptor de estrogênio–positivo resistente à terapia hormonal, este estudo oferece tanto tranquilidade quanto um roteiro. Mostra que adicionar palbociclib ao anastrozol ainda pode interromper o crescimento tumoral em mais da metade dos casos resistentes. Ao mesmo tempo, revela que alguns tumores dependem de vias alternativas de crescimento e de mecanismos imunes, tornando‑os mais difíceis de controlar. A nova assinatura de 33 genes e a descoberta de que drogas que visam JAK, como o pacritinibe, podem conter células resistentes apontam para um tratamento mais personalizado: identificar aqueles que provavelmente não responderão às combinações padrão e direcioná‑los mais cedo para ensaios que testem novos parceiros de drogas que atacam diretamente as rotas alternativas de sobrevivência do câncer.
Citação: Kong, T., Mabry, A., Highkin, M. et al. Biomarkers of response to neoadjuvant palbociclib plus anastrozole in endocrine-resistant estrogen receptor-positive/HER2-negative breast cancer: a phase 2 trial. Nat Commun 17, 949 (2026). https://doi.org/10.1038/s41467-026-68570-6
Palavras-chave: câncer de mama ER‑positivo, inibidores de CDK4/6, resistência endócrina, biomarcadores tumorais, palbociclib anastrozol