Clear Sky Science · pt
Três questões em aberto sobre a portabilidade de escores poligênicos
Por que prever saúde a partir do DNA é mais difícil do que parece
Médicos e pesquisadores esperam cada vez mais usar “escores poligênicos” baseados em DNA para prever o risco de uma pessoa desenvolver condições comuns, como diabetes, doenças cardíacas ou asma. Mas esses escores frequentemente funcionam bem apenas em pessoas que se parecem com os voluntários originais da pesquisa, geralmente de ancestralidade europeia. Este artigo pergunta por que essas predições deixam de “viajar” de forma confiável para pessoas com antecedentes genéticos ou circunstâncias de vida diferentes, e o que isso significa para usar escores de risco genético de forma justa na medicina.
O que os escores poligênicos prometem — e onde eles falham
Escores poligênicos combinam os efeitos ínfimos de muitas variantes genéticas ao longo do genoma em um único número destinado a predizer um traço, como altura ou pressão arterial. Eles são construídos a partir de grandes estudos de associação genômica ampla (GWAS) que associam marcadores de DNA a traços em centenas de milhares de voluntários. No entanto, quando esses escores são aplicados a novos grupos de pessoas, sua acurácia varia dramaticamente. Tipicamente, a predição piora quanto mais o novo grupo difere geneticamente ou socialmente dos participantes originais do GWAS. Isso é conhecido como o problema da portabilidade: um escore que funciona em um contexto pode enganar em outro, potencialmente aprofundando desigualdades em saúde se usado sem críticas.
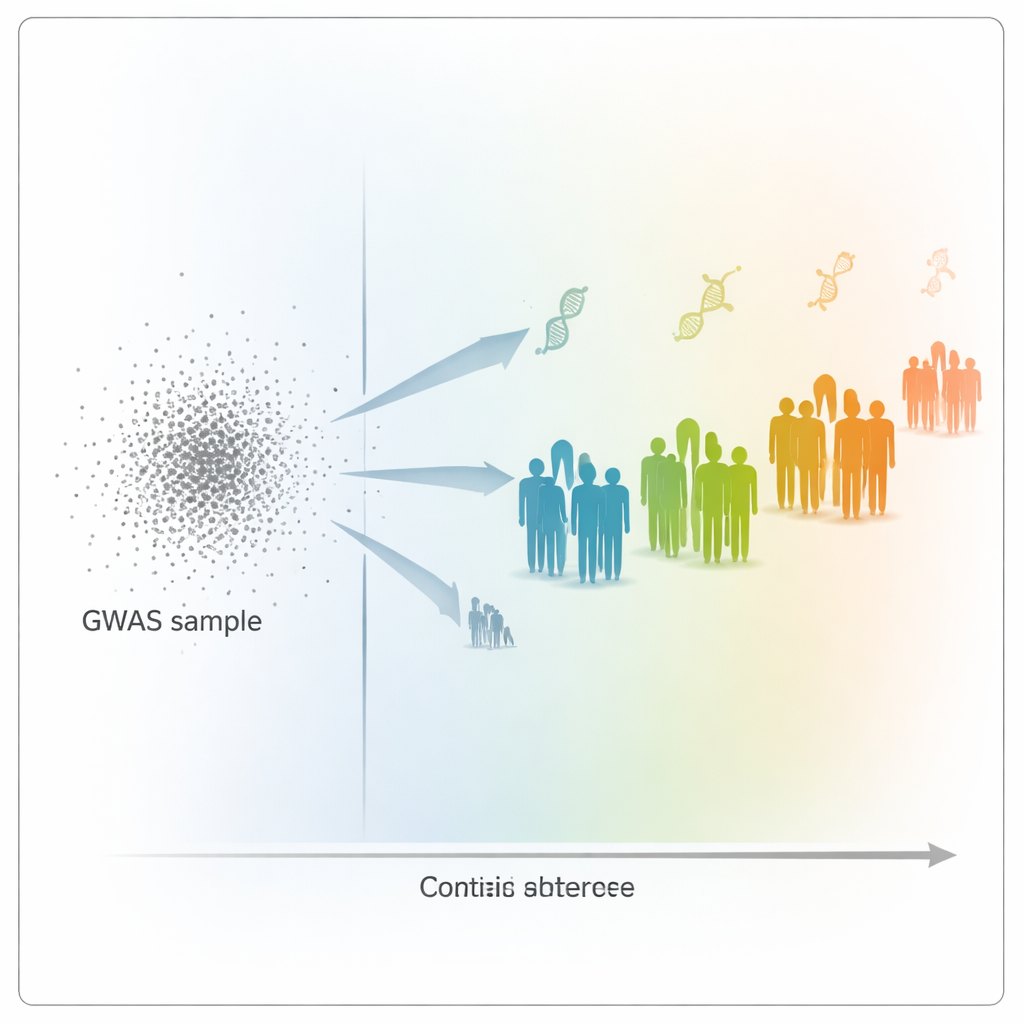
Olhando além da ancestralidade: distância no mapa genético
Para investigar esse problema, os autores usaram dados do UK Biobank, que inclui informações genéticas e de saúde de mais de 400.000 pessoas. Eles construíram escores poligênicos para 15 traços altamente hereditários, como altura, peso, contagens de células sanguíneas e níveis de colesterol, com base em um grande grupo de participantes principalmente britânicos brancos. Em seguida, testaram quão bem esses escores previam traços em 69.500 outros participantes, que abrangiam uma ampla gama de origens genéticas. Em vez de encaixar as pessoas em grandes caixas de ancestralidade, a equipe posicionou cada indivíduo ao longo de uma escala contínua de “distância genética”: quão distante o perfil de DNA de cada pessoa estava da média dos voluntários do GWAS quando projetado em um mapa genético baseado em componentes principais.
O poder de predição diminui — mas não de forma simples ou justa
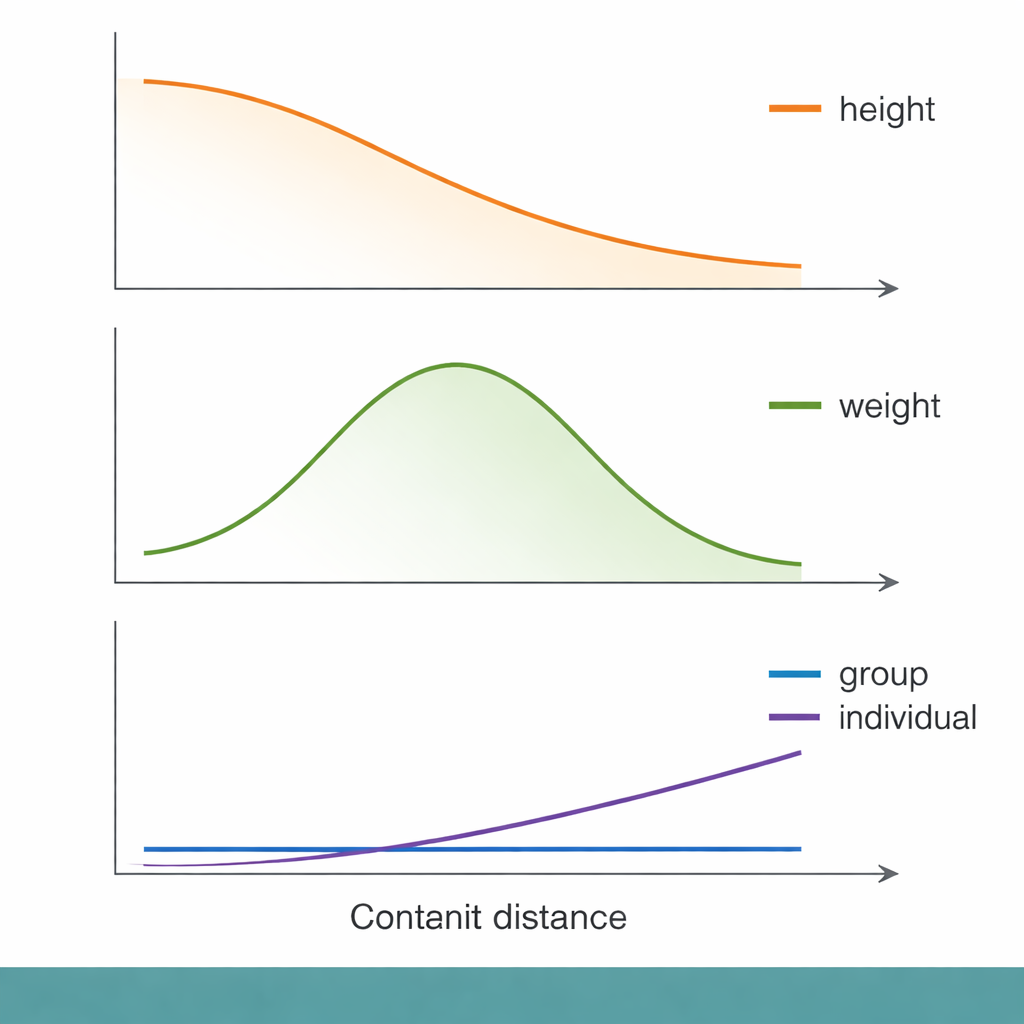
Ao longo dessa escala de distância genética, surgiram alguns padrões familiares. Para altura, por exemplo, a acurácia de predição a nível de grupo declinou de forma contínua à medida que as pessoas se tornavam mais distantes geneticamente do grupo do GWAS. Ainda assim, quando os pesquisadores ampliaram a análise para o nível individual, a distância genética explicou apenas uma fração minúscula de quão bem seus traços foram previstos. Medidas socioeconômicas, como o Índice de Privação de Townsend (um indicador em nível de bairro de desvantagem material), desempenharam papel semelhante — ou ligeiramente melhor — ao explicar quem recebeu previsões ruins. Em outras palavras, pessoas com menor status socioeconômico tendiam a receber predições genéticas menos precisas, mesmo dentro da mesma faixa de distância genética, destacando que o contexto social pode importar tanto quanto o DNA para a utilidade de um escore.
Traços diferentes, histórias diferentes, respostas diferentes
Nem todos os traços se comportaram da mesma forma. Para peso corporal e gordura corporal, a acurácia de predição na verdade atingiu um pico em distâncias genéticas intermediárias antes de decrescer, quebrando o padrão simples de “mais longe significa pior”. Traços ligados ao sistema imune, como contagens de glóbulos brancos e linfócitos, mostraram comportamento especialmente enigmático. Para alguns desses traços, a acurácia de predição a nível de grupo caiu para quase zero mesmo para pessoas que não eram geneticamente muito distantes da amostra do GWAS. Os autores sugerem que traços imunes podem ser moldados por pressões evolutivas que mudam rapidamente — como infecções passadas — que alteram quais variantes de DNA são relevantes em diferentes populações. Nesses casos, a própria arquitetura genética pode ter mudado o suficiente para que um escore baseado em um grupo se torne quase inútil em outro.
Como avaliamos desempenho pode inverter a história
O quadro fica ainda mais complicado quando mudamos a forma como “boa predição” é medida. Muito trabalho anterior baseou-se em uma única estatística chamada R², que captura quanta variação de um traço um escore explica em um grupo. Os autores mostram que outras métricas podem contar uma história diferente, especialmente para doenças. Para asma, tanto a precisão (quantas das previsões positivas são casos verdadeiros) quanto a sensibilidade (quantos casos verdadeiros são detectados) declinaram com a distância genética de forma similar. Mas para diabetes tipo 2, a precisão manteve-se relativamente constante enquanto a sensibilidade realmente aumentou com a distância — significando que o escore encontrou uma parcela maior de casos verdadeiros em grupos mais distantes, apesar de ter sido construído em um grupo mais próximo. Dependendo de o que uma clínica valorize mais — identificar todos os pacientes de alto risco ou evitar alarmes falsos — pode-se chegar a conclusões opostas sobre quão portátil é o escore.
O que isso significa para usar escores de DNA na vida real
No geral, o estudo argumenta que não podemos julgar a utilidade dos escores poligênicos olhando apenas rótulos amplos de ancestralidade ou um único número de acurácia. A qualidade da predição individual depende de uma mistura de fatores: padrões sutis de similaridade genética, a história evolutiva de cada traço, os ambientes e condições sociais em que as pessoas vivem, e a maneira particular como o escore e sua métrica de desempenho são escolhidos. Para que escores poligênicos sejam aplicados de forma justa e eficaz na medicina, pesquisadores precisarão de melhores formas de capturar estruturas genéticas finas, modelar influências sociais e ambientais e emparelhar métricas de avaliação às decisões do mundo real. Até lá, escores de risco genético devem ser usados com cautela, com atenção às pessoas — e aos contextos — para os quais eles funcionam mal, bem como aos que beneficiam.
Citação: Wang, J.Y., Lin, N., Zietz, M. et al. Three open questions in polygenic score portability. Nat Commun 17, 942 (2026). https://doi.org/10.1038/s41467-026-68565-3
Palavras-chave: escores poligênicos, predição genética, disparidades em saúde, ancestralidade genética, medicina de precisão