Clear Sky Science · pt
Quebrando a parede celular para entrega eficiente de DNA a diatomáceas
Algas como pequenas fábricas verdes
As diatomáceas — algas microscópicas que flutuam nos oceanos — produzem silenciosamente cerca de um quinto do carbono orgânico do planeta, ajudando a alimentar as teias alimentares marinhas e a sequestrar dióxido de carbono. Cientistas gostariam de transformar esses organismos resistentes e de rápido crescimento em pequenas fábricas verdes para produzir combustíveis, alimentos e produtos químicos especiais. Mas havia um grande empecilho: é surpreendentemente difícil introduzir novo DNA nas células de diatomáceas de forma confiável. Este estudo enfrenta esse problema prático de frente, descrevendo maneiras novas de levar instruções genéticas e ferramentas de edição do genoma através da dura parede externa das diatomáceas.
Amolecendo a casca de micróbios oceânicos
O trabalho se concentra na diatomácea modelo Phaeodactylum tricornutum, favorita em laboratórios porque seu genoma está bem mapeado e já existem algumas ferramentas genéticas básicas. Os autores supuseram que a parede celular, a primeira barreira física que qualquer DNA precisa atravessar, era um gargalo chave. Ao tratar as células com uma enzima chamada alcalase, eles removeram parcial ou totalmente essa parede, criando “esferoplastos” e “protoplastos” frágeis que são muito mais fáceis de penetrar. Quando então usaram eletroporação — pulsos elétricos breves que abrem poros temporários — o número de transformantes bem‑sucedidos subiu dramaticamente, em cerca de duas ordens de magnitude comparado com métodos anteriores. Mesmo quantidades minúsculas de DNA, tão pequenas quanto um nanograma, foram suficientes para recuperar células engenheiradas. 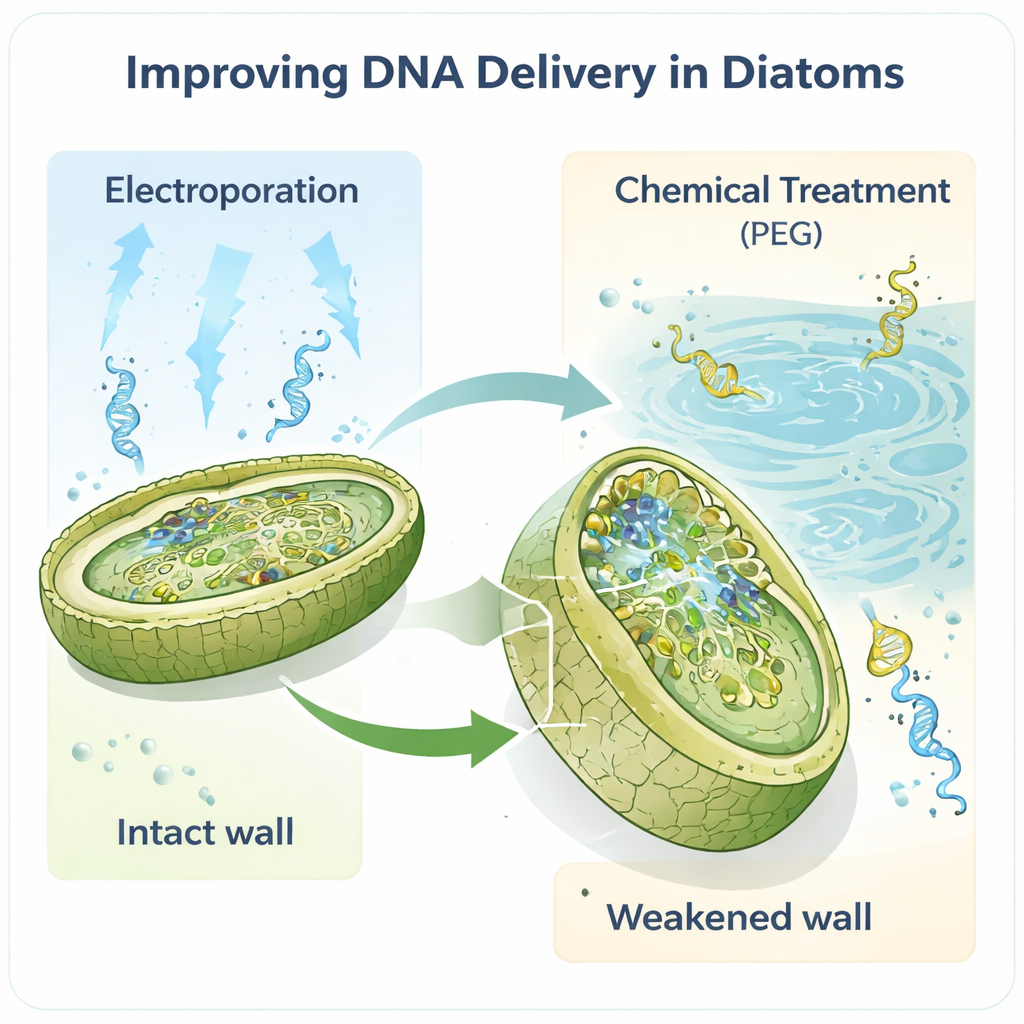
Entrega rápida de DNA sem desviar por bactérias
Maneiras tradicionais de modificar diatomáceas muitas vezes dependem de “correios” bacterianos para transportar grandes moléculas circulares de DNA, chamadas episomos, para as algas. Embora eficaz, essa abordagem é lenta, tecnicamente exigente e pode desestabilizar construções de DNA delicadas. Os novos protocolos mostram que tanto a eletroporação quanto um método químico refinado com polietilenoglicol (PEG) podem mover episomos diretamente para as diatomáceas, contornando a etapa bacteriana. Notavelmente, episomos de até 55,6 mil pares de bases foram entregues e recuperados intactos. As mesmas estratégias também funcionaram em uma segunda espécie, Thalassiosira pseudonana, que tem uma parede mais mineralizada, sugerindo que este é um conjunto de ferramentas de amplo uso, e não um truque específico de uma espécie.
Deixando a célula construir seus próprios círculos genéticos
Ao investigar como o DNA eletroporado se comportava dentro das células, a equipe tropeçou em um talento surpreendente: as diatomáceas conseguem unir fragmentos de DNA por conta própria. Fragmentos lineares de episomos entraram na célula e foram reparados em círculos seja por junção imprecisa “não homóloga”, seja por reparo mais preciso guiado por regiões sobrepostas, “direcionado por homologia”. Os autores batizaram esse processo de “montagem in vivo em diatomáceas”, ou DIVA. Ao projetar fragmentos sobrepostos, eles induziram as células a montar dois, três ou quatro pedaços em episomos completos com altas taxas de sucesso, às vezes até incorporando pequenos cassetes sintéticos que adicionam marcadores fluorescentes ou novas funções. Essa habilidade transforma o núcleo da diatomácea em uma oficina miniatura de DNA, potencialmente substituindo passos de montagem trabalhosos normalmente feitos em leveduras ou em E. coli.
Editando genomas apenas com complexos proteicos
Além de adicionar episomos, os pesquisadores mostraram que podiam entregar complexos proteína‑RNA prontos de CRISPR–Cas9 diretamente nas células de diatomáceas usando seu método de eletroporação otimizado. Mirando um gene chamado PtAPT, que controla a sensibilidade a um análogo tóxico de adenina, eles geraram milhares de mutantes resistentes sem introduzir nenhum DNA extra no genoma. Muitos desses mutantes apresentaram pequenas inserções ou deleções no sítio alvo; alguns até capturaram pedaços de DNA “veiculador” que haviam sido adicionados para amortecer o choque elétrico. A equipe então coentregou complexos CRISPR e episomos em um único passo, descobrindo que cerca de uma em cada dez colônias apresentava tanto uma edição genômica quanto um episomo selecionável — uma maneira eficiente de rastrear alterações genéticas que, de outra forma, seriam invisíveis. 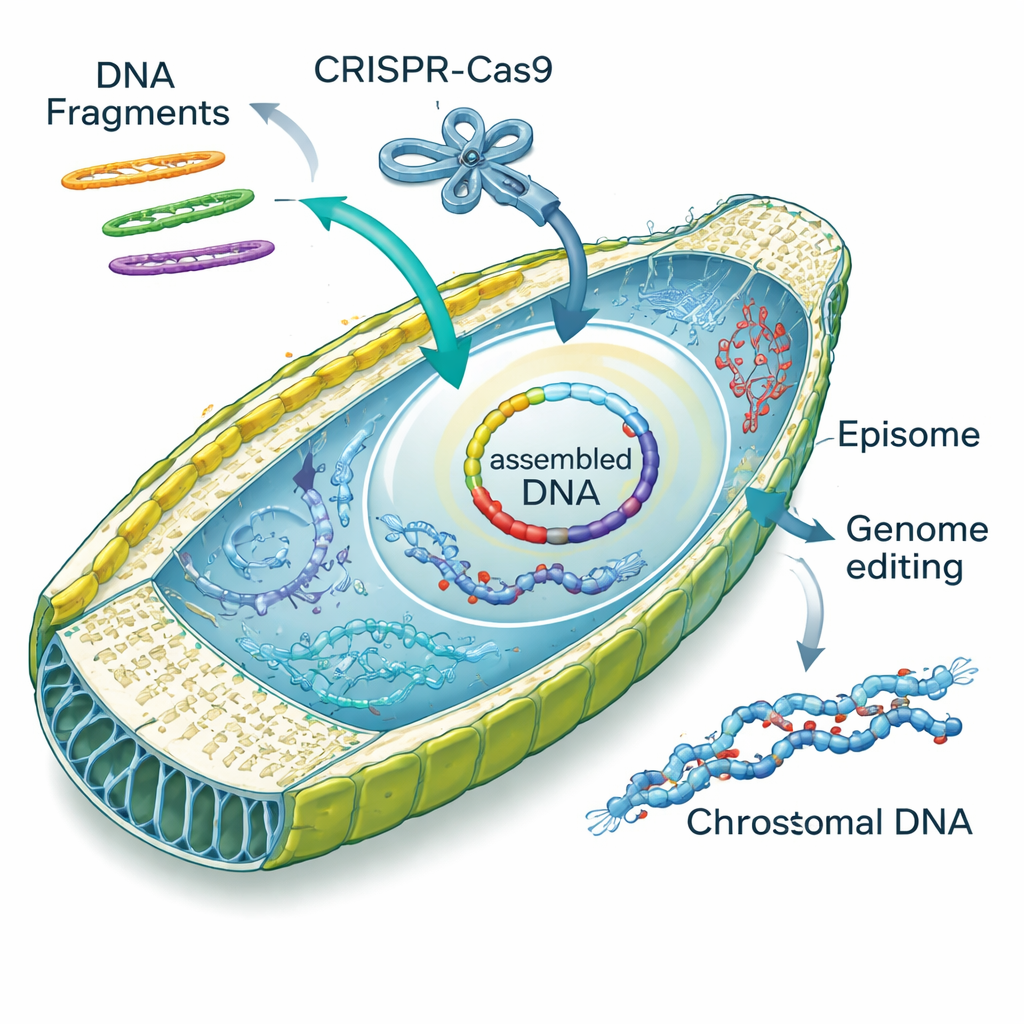
Rumo a diatomáceas projetadas para um futuro sustentável
Para não especialistas, a mensagem chave é que as diatomáceas estão muito mais próximas de se tornarem organismos práticos e programáveis. Ao romper ou amolecer suavemente a parede celular, os autores transformaram um processo caprichoso e de baixa eficiência em uma linha de trabalho robusta que usa pequenas quantidades de DNA, funciona com grandes construções genéticas e até permite que a própria célula monte e edite seu DNA. Esses avanços encurtam o caminho de uma sequência projetada em computador até uma linhagem viva e testada. A longo prazo, tais ferramentas podem acelerar esforços para construir diatomáceas com cromossomos inteiramente sintéticos e para aproveitar esses micróbios oceânicos para combustíveis mais limpos, química amiga do clima e novas descobertas biológicas.
Citação: Walker, E.J.L., Pampuch, M., Deng, L. et al. Breaking the cell wall for efficient DNA delivery to diatoms. Nat Commun 17, 1848 (2026). https://doi.org/10.1038/s41467-026-68562-6
Palavras-chave: biotecnologia de diatomáceas, transformação genética, edição genômica CRISPR, biologia sintética, engenharia de microalgas