Clear Sky Science · pt
Estruturas da telomerase humana ligada a nucleotídeos em vários passos do seu ciclo de adição de repetições de DNA telomérico
Por que as extremidades dos nossos cromossomos importam
Cada vez que uma célula se divide, as capas protetoras nas pontas dos nossos cromossomos — chamadas telômeros — ficam um pouco mais curtas. Se elas ficarem muito curtas, as células param de se dividir ou funcionam mal, contribuindo para o envelhecimento e para doenças. Uma máquina molecular chamada telomerase pode reconstruir essas capas e é incomumente ativa na maioria dos cânceres. Este estudo revela, com detalhes sem precedentes, como a telomerase humana agarra e alonga os telômeros passo a passo, oferecendo pistas de como poderemos um dia ajustar finamente essa enzima em distúrbios relacionados à idade e no câncer.
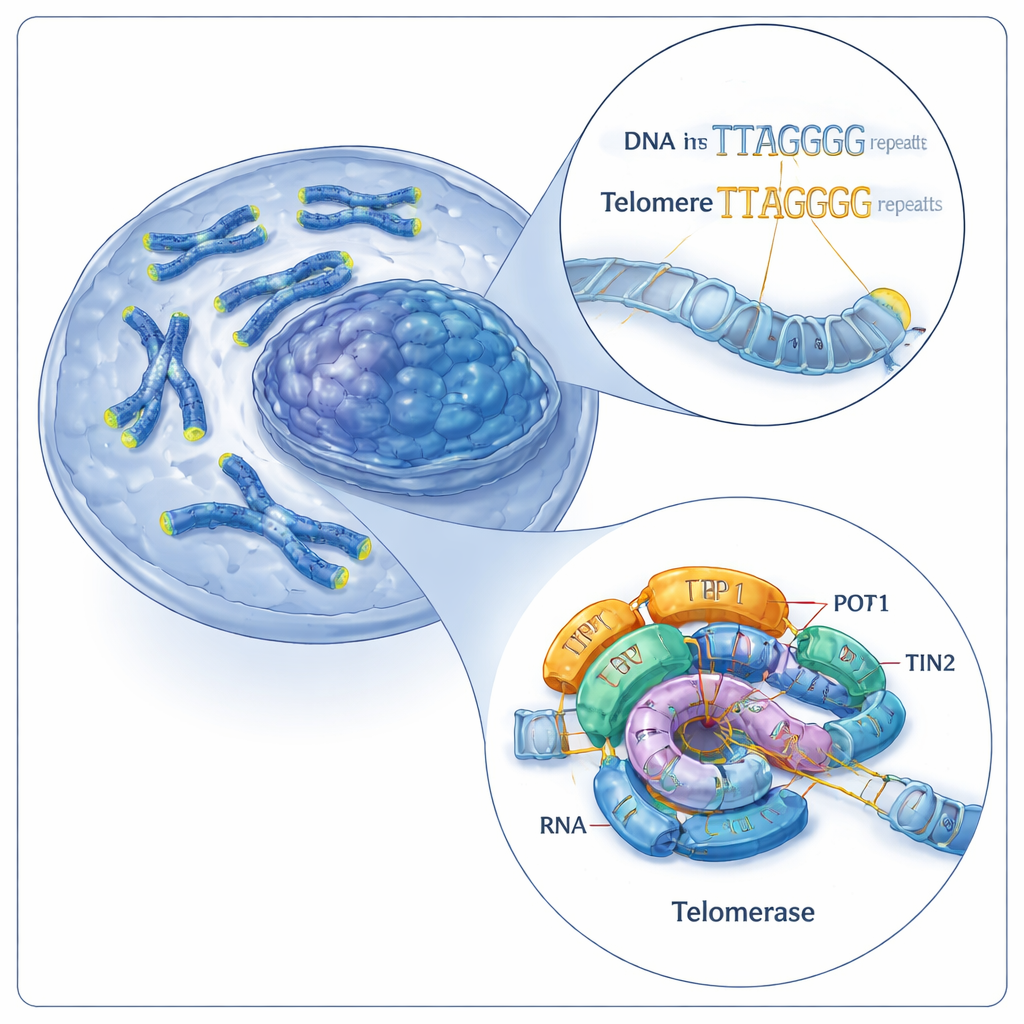
A equipe de reparo das capas cromossômicas da célula
Os telômeros são feitos de curtas sequências de DNA repetidas (em humanos, um padrão de seis letras: TTAGGG). A telomerase alonga os telômeros adicionando mais dessas repetições às extremidades dos cromossomos. Ela faz isso usando duas partes principais: uma proteína chamada telomerase reverse transcriptase (TERT) e uma molécula de RNA embutida (hTR) que funciona como molde. Juntos, esses componentes formam um núcleo catalítico, auxiliado por proteínas acessórias conhecidas como shelterin, incluindo um trio chamado TPP1–POT1–TIN2. Trabalhos anteriores haviam visualizado a telomerase humana em apenas um estado funcional, deixando uma grande questão em aberto: como essa máquina adiciona repetidamente novas repetições sem se desprender do DNA?
Congelando a telomerase em ação
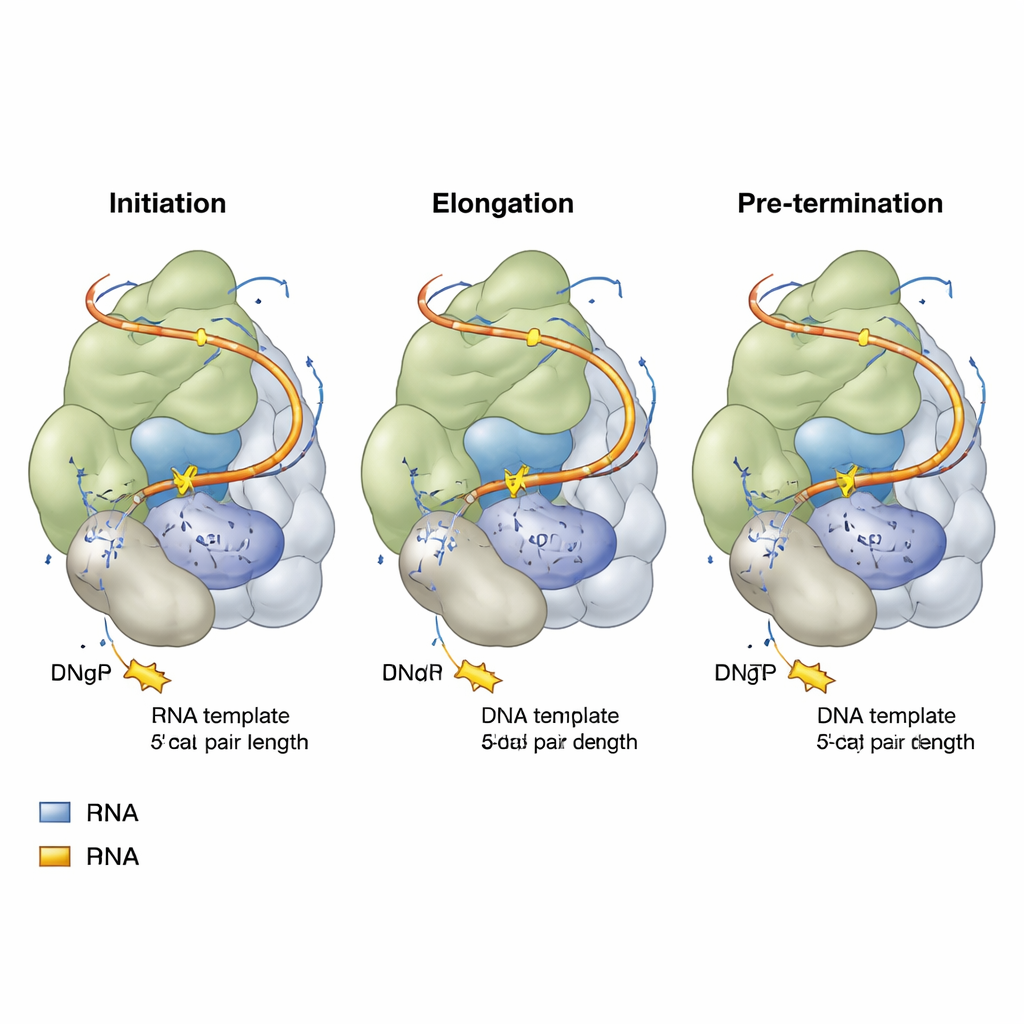
Os pesquisadores reconstruíram a telomerase humana em células humanas e então a montaram com pedaços cuidadosamente desenhados de DNA telomérico e análogos de nucleotídeos não reativos — moléculas que se parecem com as letras do DNA, mas não podem ser totalmente incorporadas. Usando microscopia crioeletrônica de alta resolução, capturaram instantâneos da telomerase em três estágios-chave do seu ciclo de adição de repetições: o início (iniciação), o meio da cópia (elongação) e logo antes de terminar uma repetição (pré-terminação). Cada instantâneo mostrou o núcleo catalítico da telomerase envolvendo um curto híbrido de DNA e RNA, com um nucleotídeo entrante posicionado no sítio ativo, pronto para ser adicionado à cadeia de DNA em crescimento.
Um pequeno zíper que controla um grande processo
Ao longo dos três estágios, emergiu um tema surpreendente: o híbrido DNA–RNA dentro da telomerase permanece essencialmente do mesmo tamanho — apenas quatro pares de bases, estendendo-se temporariamente para cinco quando um novo nucleotídeo entra. Um aminoácido específico em TERT, apelidado de “cabeça de zíper”, marca consistentemente o fim desse curto híbrido e impede que ele cresça mais. À medida que novas letras de DNA são adicionadas, um par de bases na extremidade distante se desnatura, de modo que o híbrido nunca se estende além dessa janela restrita de quatro a cinco pares. Esse desenho compacto provavelmente facilita a separação e o deslocamento das fitas, permitindo à enzima avançar e iniciar a próxima repetição sem soltar totalmente o DNA. Diferenças sutis em quais letras do DNA e do RNA ocupam esse curto híbrido explicam por que algumas sequências de extremidade telomérica se ligam mais fortemente à telomerase do que outras.
Conectores de RNA flexíveis e peças móveis
O molde de RNA dentro da telomerase não flutua livremente; ele é ancorado por trechos flexíveis em ambos os lados, chamados de conectores do molde 5′ e 3′. À medida que a telomerase progride da iniciação até a pré-terminação, o conector upstream (5′) é esticado como um elástico, eventualmente atingindo um estado totalmente tensionado que ajuda a sinalizar o fim de uma repetição. Enquanto isso, o conector downstream (3′) forma uma saliência e se aproxima de outra estrutura de RNA (a haste-loop P6.1) e de regiões proteicas próximas. Se esses conectores ficarem muito curtos ou muito longos, ou se o P6.1 for alterado, a capacidade da telomerase de adicionar repetição após repetição cai acentuadamente. Importante, certas regiões proteicas — o domínio TEN e um inserto específico da telomerase chamado cunha TRAP — atuam como guias ajustáveis, contatando tanto o DNA quanto esses conectores de RNA. Mutações que reduzem o volume da cunha TRAP podem, na verdade, tornar a enzima mais processiva, sugerindo que essa cunha normalmente age como uma barreira controlada que regula o movimento do molde.
Novos insights sobre um alvo terapêutico
Ao combinar instantâneos estruturais com testes funcionais de mutações específicas, o estudo propõe um modelo mecânico detalhado de como a telomerase humana estende repetidamente os telômeros. A enzima mantém um híbrido DNA–RNA muito curto, usa um resíduo em forma de zíper para impor esse comprimento e depende de conectores de RNA flexíveis e elementos proteicos móveis para avançar o molde e manter o DNA ancorado durante múltiplas rodadas de cópia. Para não especialistas, a mensagem-chave é que a telomerase não funciona como uma máquina de copiar estática, mas como um dispositivo finamente calibrado e carregado por molas, cuja geometria e partes móveis determinam o quão longa e quão eficientemente ela pode manter os telômeros. Entender essa coreografia abre a porta para fármacos que possam diminuir a atividade da telomerase em cânceres ou estabilizar sua função em doenças de envelhecimento prematuro.
Citação: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Palavras-chave: telomerase, telômeros, cryo-EM, estabilidade genômica, biologia do câncer