Clear Sky Science · pt
Metilação de DNA e lncRNA controlam replicação assíncrona do DNA em domínios gênicos imprintados específicos
Por que o calendário de cópia do DNA importa
Cada vez que uma célula se divide, ela precisa copiar todo o seu DNA, mas nem todas as regiões são duplicadas ao mesmo tempo. Alguns trechos são copiados cedo, outros tarde, seguindo um “horário” preciso do genoma. Este artigo investiga por que, em alguns agrupamentos gênicos especiais que lembram de qual dos pais foram herdados, as cópias maternas e paternas são replicadas em momentos diferentes. Entender esse tempo incomum esclarece como marcas químicas no DNA e RNAs longos não codificantes (lncRNAs) ajudam a organizar o genoma e podem influenciar o desenvolvimento e doenças.
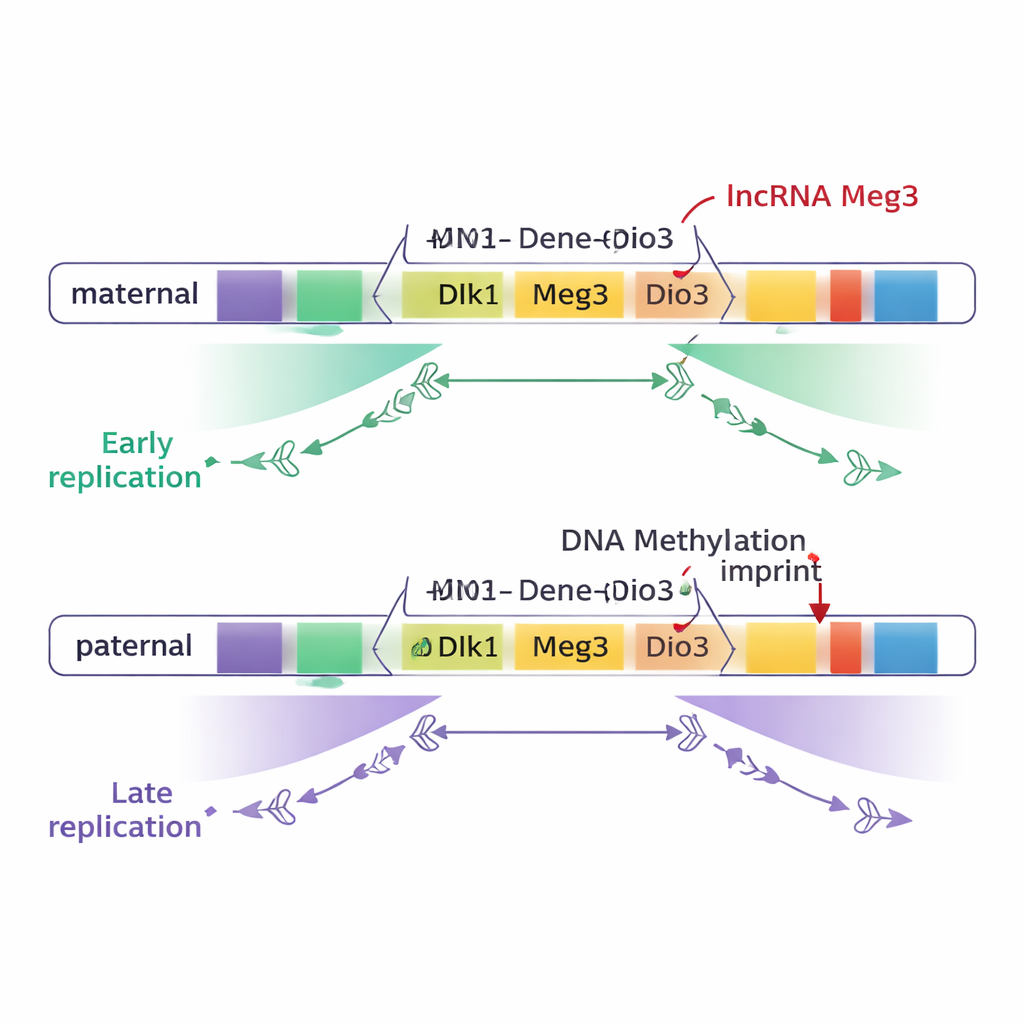
Memórias parentais escritas no DNA
Em mamíferos, um pequeno número de domínios gênicos “imprintados” se comporta de forma distinta dependendo se foi herdado da mãe ou do pai. Esse efeito de origem parental é controlado pela metilação do DNA — pequenas marcas químicas adicionadas a regiões específicas conhecidas como regiões diferencialmente metiladas (DMRs) — e por alterações no dobramento dos cromossomos. Os autores estudaram células-tronco embrionárias de camundongo, que se assemelham a células embrionárias muito precoces. Compararam células com apenas genoma materno, apenas genoma paterno e híbridos normais carregando um de cada. Ao rastrear quando trechos de DNA eram copiados durante o ciclo celular, mapearam o tempo de replicação pelo genoma e se concentraram em regiões imprintadas conhecidas.
Dois domínios imprintados quebram as regras
A maior parte do genoma, incluindo a maioria dos domínios imprintados, foi replicada ao mesmo tempo nos cromossomos maternos e paternos. Entretanto, dois grandes domínios imprintados se destacaram: o domínio Dlk1–Dio3 no cromossomo 12 e a região Snrpn no cromossomo 7. Nesses trechos, uma larga extensão de DNA — cerca de três quartos de milhão de pares de bases em Dlk1–Dio3 — foi copiada cedo em um cromossomo parental e tarde no outro. Crucialmente, essa diferença seguia a origem parental, não a linhagem: a cópia materna de genes-chave como Dlk1 e do gene lncRNA Meg3 replicava consistentemente cedo, enquanto as cópias paternas replicavam tarde.
Metilação de DNA define o interruptor de tempo
Para testar o que causa essa diferença de tempo, os pesquisadores modificaram células-tronco em que o padrão normal de metilação nas DMRs foi apagado ou forçado em ambos os cromossomos parentais. Quando ambas as cópias parentais das DMRs de Dlk1–Dio3 estavam metiladas, toda a região replicou tarde em ambos os cromossomos. Quando a metilação foi amplamente removida de ambas as cópias, a mesma região replicou cedo em ambos. Experimentos semelhantes em Snrpn também eliminaram as diferenças de tempo. Esses resultados mostram que a metilação do DNA específica de cada parental é essencial para criar o contraste cedo-versus-tarde entre cromossomos maternos e paternos, pelo menos nesses dois domínios.
Um RNA longo ajusta a replicação precoce
Porém, a metilação do DNA não era a história completa. A região Dlk1–Dio3 também produz um RNA longo não codificante chamado Meg3 como parte de um grande ‘policistron’ de RNA. No cromossomo materno, DMRs não metiladas permitem a expressão de Meg3; no cromossomo paterno, a metilação o mantém silenciado. Ao criar deleções precisas que desligavam Meg3 mantendo a metilação do DNA intacta, os autores mostraram que a perda do RNA Meg3 fez com que partes específicas do domínio materno mudassem de replicação precoce para tardia. Em outras palavras, o RNA Meg3 ajuda a promover a cópia precoce em trechos próximos do cromossomo materno, acrescentando uma segunda camada de controle além da metilação do DNA.
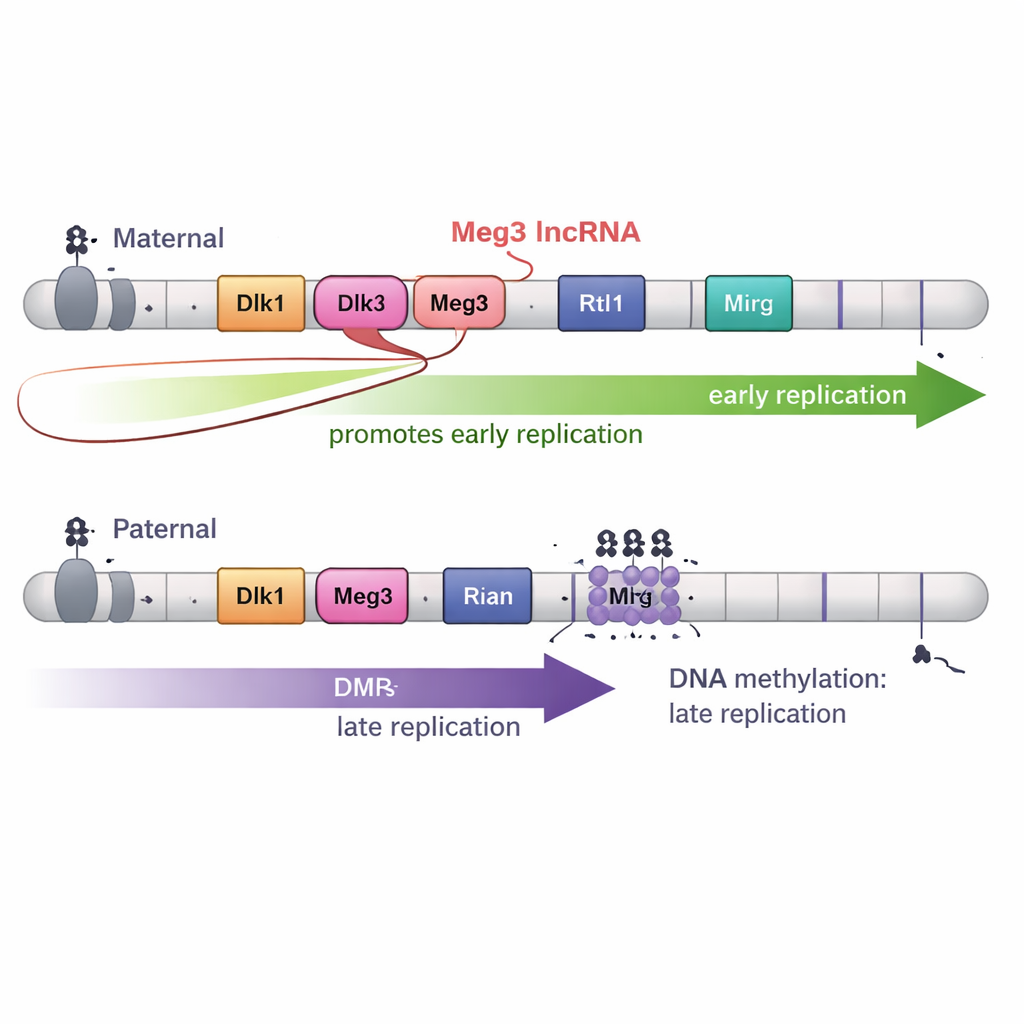
Dobramento 3D e desenvolvimento acrescentam reviravoltas
Como o dobramento do genoma costuma estar ligado ao tempo de replicação, a equipe também mapeou a arquitetura cromossômica 3D em alta resolução. Surpreendentemente, na região Dlk1–Dio3, as bordas dos domínios 3D não coincidiram com os limites da replicação precoce e tardia. Mesmo quando padrões de metilação foram alterados e o tempo de replicação mudou, as unidades básicas de dobramento — domínios de associação topológica — se deslocaram de formas diferentes. Finalmente, quando as células-tronco foram diferenciadas em progenitores neurais, as marcantes diferenças de tempo entre cópias maternas e paternas desapareceram em grande parte, embora marcas de imprinting e muitos aspectos da estrutura 3D tenham permanecido. Isso sugere que sinais do desenvolvimento podem sobrepor o padrão especial cedo-versus-tarde observado nas células-tronco.
O que isso significa em termos simples
Este estudo revela que, em alguns bairros gênicos especiais que lembram de qual pai vieram, o calendário de cópia do DNA da célula é controlado por uma combinação de marcas químicas no DNA e RNAs longos não codificantes. A metilação do DNA em regiões de controle imprintadas define um tempo básico de cedo-ou-tarde para cada cromossomo parental, e o lncRNA Meg3 impulsiona adicionalmente o DNA materno próximo a ser copiado mais cedo. Esses efeitos atuam em grande parte de forma independente de como o cromossomo se dobra em 3D. Durante o desenvolvimento, à medida que as células se especializam, esse tempo incomum desaparece, mostrando que é uma característica do estado pluripotente das células-tronco. Em conjunto, o trabalho explica como “memórias” epigenéticas parentais e RNAs não codificantes podem, localmente, sobrepor o cronograma habitual de replicação do genoma.
Citação: Imaizumi, Y., Charon, F., Surcis, C. et al. DNA methylation and lncRNA control asynchronous DNA replication at specific imprinted gene domains. Nat Commun 17, 1844 (2026). https://doi.org/10.1038/s41467-026-68558-2
Palavras-chave: imprinting genômico, metilação de DNA, tempo de replicação, RNA não codificante longo, células-tronco embrionárias