Clear Sky Science · pt
Ativação microbiana do GLP-2R mitiga a inflamação gastrointestinal
Por que uma proteína amigável ao intestino importa
Enquanto o mundo busca maneiras sustentáveis de alimentar uma população em crescimento, cientistas olham além de fazendas e campos para enormes tanques de aço onde micróbios são cultivados como alimento. Este estudo investiga se uma dessas proteínas derivadas de micróbios pode fazer mais do que apenas nos nutrir. Os pesquisadores perguntaram: uma proteína feita a partir de bactérias inofensivas pode tanto suprir necessidades dietéticas quanto proteger ativamente o intestino contra inflamação, um problema central em condições como doença inflamatória intestinal e danos intestinais induzidos por quimioterapia?
Um novo tipo de proteína vinda de micróbios
A proteína no centro deste trabalho provém de uma bactéria do solo chamada Methylococcus capsulatus Bath (McB). Em vez de ser consumida como bactéria viva, a McB é processada em um lisado microbiano — essencialmente um pó composto por células bacterianas rompidas — produzido comercialmente sob o nome FeedKind®. Camundongos receberam dietas nas quais esse lisado forneceu a maior parte da proteína, em uma dieta simples ou em uma dieta “complexa” mais semelhante à humana. A equipe então acompanhou como essa dieta alterou a composição dos micróbios intestinais, as células imunes que patrulham o intestino e a capacidade do intestino de resistir a diferentes tipos de lesão.
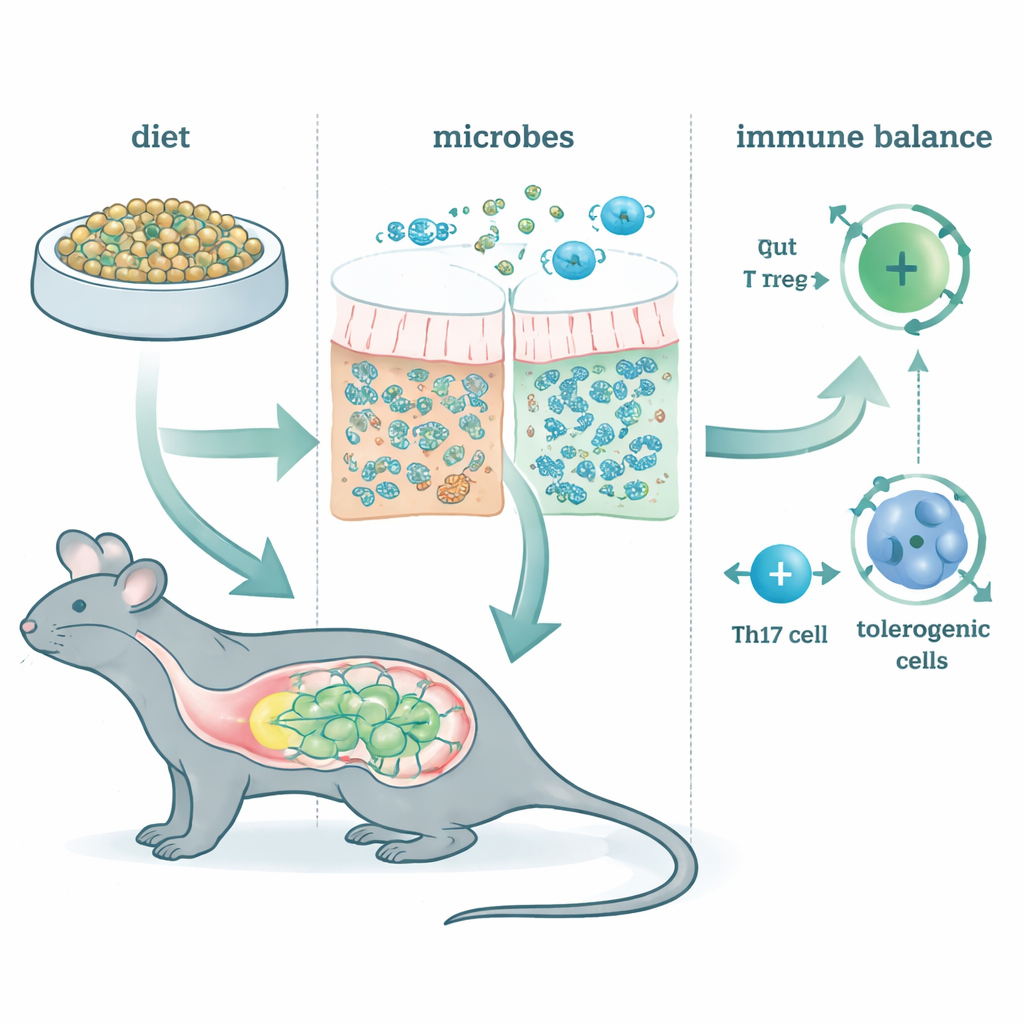
Redefinindo o bairro microbiano
Alimentar os animais com McB alterou de forma rápida e persistente o microbiota intestinal, independentemente da dieta de base dos animais. Apenas uma fração minúscula da própria McB apareceu nas fezes, o que significa que o material foi quase completamente aproveitado no intestino. Em vez disso, algumas espécies bacterianas de famílias como Lachnospiraceae e Bacteroidaceae prosperaram. Análises genéticas mostraram que essas comunidades estavam enriquecidas em vias de fermentação que produzem ácidos graxos de cadeia curta — pequenas moléculas já conhecidas por nutrir as células intestinais e influenciar a imunidade. Em outras palavras, a McB agiu menos como uma proteína convencional e mais como um combustível direcionado que remodela o que os micróbios residentes fazem.
Ensinando o sistema imune a tolerar
Os autores examinaram em seguida tipos-chave de células T que ajudam a decidir se o intestino reage com calma ou de forma agressiva ao que passa por ele. Um grupo, as células T reguladoras induzidas perifericamente (pTregs), ajuda a prevenir reações excessivas a alimentos e micróbios benignos. Outro grupo, as células Th17, pode tanto impulsionar inflamação prejudicial quanto ajudar a manter uma barreira saudável, dependendo do seu “estado”. A alimentação com McB aumentou fortemente as pTregs ao longo de todo o intestino, mesmo quando a maior parte dos micróbios intestinais foi eliminada com antibióticos. Por outro lado, os efeitos da McB sobre as células Th17 dependeram da presença e da função normal das bactérias intestinais. Em camundongos microbiana mente intactos, a McB inclinou as Th17 para um estado mais calmante, produtor de IL‑10 e menos inflamatório. Quando a fermentação foi bloqueada, essa mudança tolerogênica desapareceu, destacando que a McB atua em parte ao redirecionar as conversas entre micróbios e imunidade.
Protegendo o intestino durante lesões
Para avaliar se essas mudanças se traduzem em proteção no mundo real, os pesquisadores desafiaram camundongos com dois insultos intensos ao intestino. Um foi um fármaco de quimioterapia, 5‑fluorouracil, que causa danos generalizados e encurtamento das vilosidades — estruturas alongadas que absorvem nutrientes. O outro foi um químico (DSS) que desencadeia colite, um modelo de inflamação do intestino grosso. Camundongos na dieta com McB perderam menos peso, mantiveram vilosidades e comprimento do cólon maiores, apresentaram menos lesões hemorrágicas e tiveram escores microscópicos de dano mais baixos em ambos os modelos. Esses benefícios permaneceram mesmo quando células T CD4 foram removidas experimentalmente, sugerindo que as ações protetoras da McB no intestino não se devem exclusivamente às células imunes adaptativas, mas também envolvem efeitos diretos no revestimento intestinal.
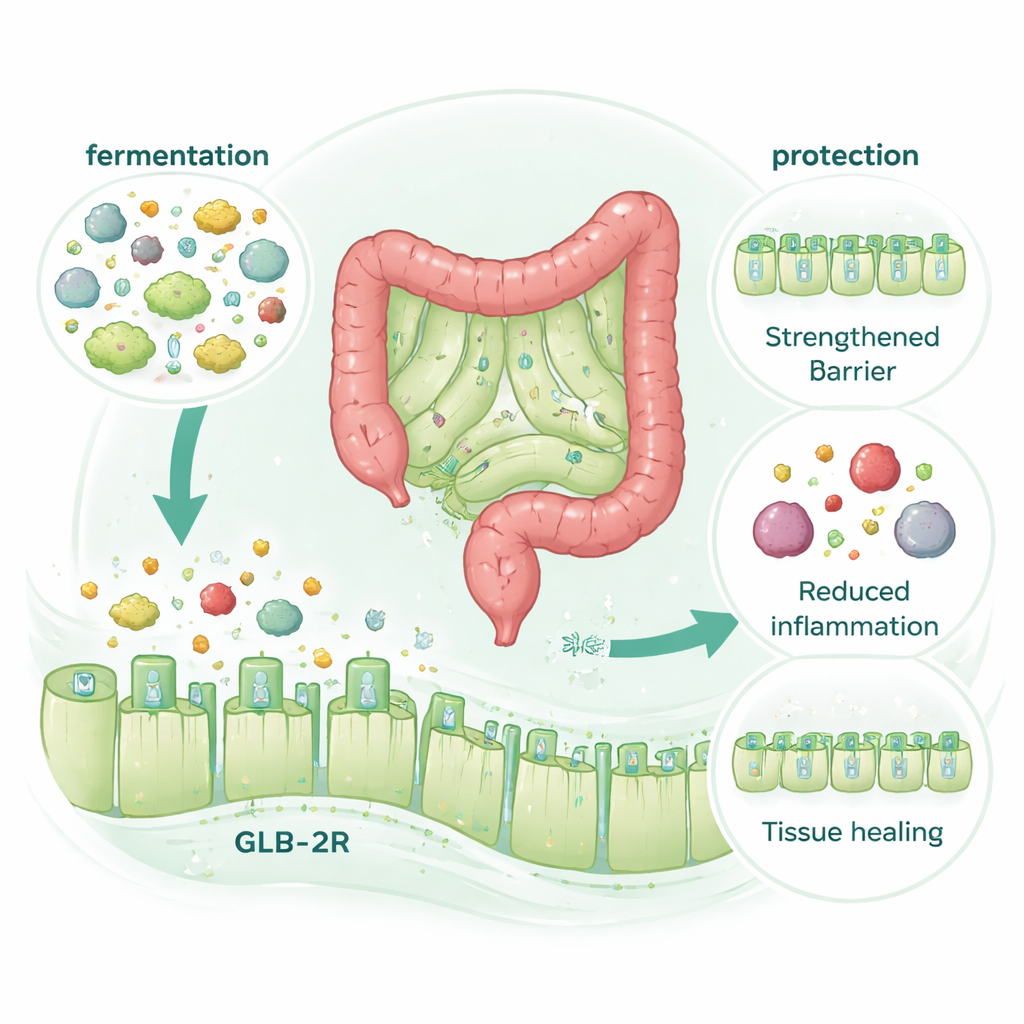
Um receptor hormonal, mas sem hormônio extra
Uma surpresa foi a descoberta de que o efeito protetor da McB exigia absolutamente o receptor intestinal para um hormônio promotor de reparo chamado GLP‑2 (o receptor GLP‑2, ou GLP‑2R), mas não o receptor relacionado GLP‑1. Quando os camundongos não tinham GLP‑2R, a McB deixou de protegê‑los dos danos da quimioterapia ou da colite. Ainda assim, a McB em si não elevou os níveis de GLP‑2 no sangue, mesmo quando a digestão e a degradação hormonal foram cuidadosamente controladas. Em vez disso, os benefícios desapareceram quando a fermentação microbiana no cólon foi bloqueada quimicamente, embora a composição geral do microbiota tenha mudado muito pouco. Isso aponta para um mecanismo em que a degradação microbiana da McB gera pequenos compostos que se comportam como “mímicos” do GLP‑2, ativando seu receptor para fortalecer a barreira e promover reparo sem a liberação extra do hormônio.
O que isso pode significar para alimentos futuros
Para um leitor leigo, a mensagem principal é que algumas fontes proteicas futuras podem ser projetadas não apenas para serem climática mente sustentáveis, mas também para apoiar ativamente a saúde intestinal. Em camundongos, um lisado de McB escalável comercialmente tanto reconfigurou a imunidade em direção à tolerância quanto ajudou o intestino a resistir a lesões severas, por duas vias parcialmente independentes: um impulso direto às células T reguladoras e uma ativação do receptor GLP‑2 dirigida pela fermentação que auxilia o reparo tecidual. Embora estudos em humanos ainda sejam necessários, o trabalho sugere que proteínas derivadas de micróbios poderiam formar uma nova classe de alimentos “inteligentes” — capazes de nos alimentar, colaborar com nossos próprios micróbios e reforçar discretamente as defesas naturais do intestino contra a inflamação.
Citação: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
Palavras-chave: inflamação intestinal, proteína microbiana, microbioma, receptor de GLP-2, células T reguladoras