Clear Sky Science · pt
FUNDC1 endotelial regula o reprogramamento metabólico e a transição obesidade-diabetes através do eixo SIRT3/GATA2/endotelina-1
Por que as células dos vasos sanguíneos importam para obesidade e diabetes
Obesidade e diabetes tipo 2 costumam ser atribuídos ao tecido adiposo, ao fígado ou ao pâncreas. Mas este estudo revela um culpado surpreendente: a fina camada de células que reveste nossos vasos sanguíneos, chamadas células endoteliais. Os pesquisadores mostram que uma pequena proteína mitocondrial nessas células, chamada FUNDC1, pode ajudar a empurrar o corpo da simples ganho de peso para um diabetes estabelecido ao alterar como os vasos se comunicam com os órgãos metabólicos.
Estresse na “pele” interna do corpo
As células endoteliais formam uma vasta e delicada rede que controla o fluxo sanguíneo, a entrega de nutrientes e os sinais para tecidos vizinhos. Em condições saudáveis, elas equilibram fatores relaxantes como o óxido nítrico com fatores constritores como a endotelina-1 (ET-1). Na obesidade e no diabetes inicial, esse equilíbrio se desloca em direção à ET-1, que não só estreita os vasos como também prejudica a maneira como células adiposas, musculares e hepáticas lidam com açúcar e gordura. Os autores começaram mostrando em camundongos que a disfunção vascular aparece já após apenas dois meses em dieta rica em gordura, antes do desenvolvimento claro de resistência à insulina, sugerindo que o endotélio lesionado pode ajudar a desencadear a doença metabólica em vez de simplesmente responder a ela.
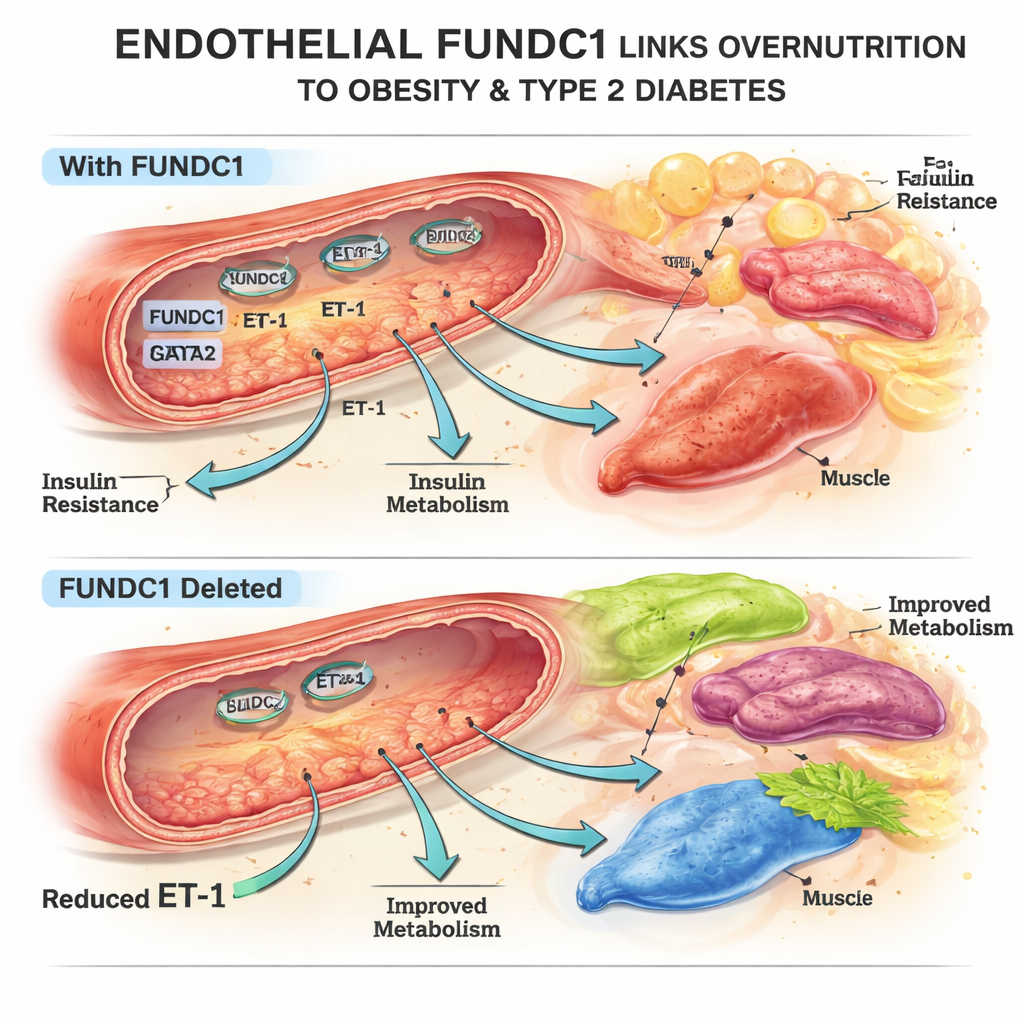
Um interruptor mitocondrial que molda a gordura corporal
A equipe concentrou-se na FUNDC1, uma proteína na superfície das mitocôndrias, as usinas de energia da célula. Em células endoteliais de camundongo e humanas expostas a excesso de gordura, os níveis de FUNDC1 mudaram ao longo do tempo: caíram inicialmente e depois aumentaram fortemente com a supernutrição prolongada. Usando camundongos geneticamente modificados que carecem de FUNDC1 apenas nas células endoteliais, os pesquisadores descobriram que esses animais estavam parcialmente protegidos do ganho de peso por dieta rica em gordura, tinham menos gordura corporal, adipócitos menores e melhor controle da glicemia. Seus tecidos adiposo, hepático e marrom responderam mais intensamente à insulina, embora os níveis de insulina em si não fossem maiores. Essas mudanças não puderam ser explicadas por diferenças na ingestão de alimento ou na atividade, apontando em vez disso para como a vasculatura influenciava o metabolismo.
Um mensageiro químico que impulsiona a resistência à insulina
Para descobrir como a FUNDC1 endotelial afeta órgãos distantes, os autores rastrearam várias substâncias secretadas pelas células endoteliais. Uma delas se destacou: a ET-1. Quando FUNDC1 foi deletada nas células endoteliais, a produção de ET-1 nos vasos e na corrente sanguínea caiu marcadamente, tanto em condições normais quanto em dieta rica em gordura. Experimentos em cultivos de adipócitos, hepatócitos e células musculares mostraram que a ET-1 promoveu o crescimento de pré-adipócitos, alterou o armazenamento e a quebra de gordura e piorou o acúmulo lipídico no fígado e no músculo expostos a alto teor de gordura — um padrão conhecido por favorecer resistência à insulina. Em camundongos vivos, a infusão de ET-1 no início de uma dieta rica em gordura eliminou os benefícios protetores da deleção de FUNDC1 endotelial: peso corporal, massa de gordura, controle glicêmico e função vascular deterioraram-se, ressaltando a ET-1 como um elo-chave entre o endotélio e a doença metabólica.
Um eixo de sinalização interno: FUNDC1, SIRT3 e GATA2
O estudo então mapeia uma cadeia molecular detalhada dentro das células endoteliais. Sob estresse por dieta rica em gordura, uma forma longa da enzima SIRT3 (SIRT3-L), que pode residir tanto no núcleo quanto nas mitocôndrias, desloca-se do núcleo para as mitocôndrias com a ajuda da FUNDC1 e de uma proteína chaperona chamada HSC70. Uma vez sequestrada nas mitocôndrias, menos SIRT3-L fica disponível no núcleo para remover grupos acetil de GATA2, um fator de transcrição que aumenta a atividade do gene da ET-1. GATA2 mais acetilado é mais estável e impulsiona maior produção de ET-1. Quando FUNDC1 está ausente, SIRT3-L permanece no núcleo, onde desacetila GATA2, levando à degradação de GATA2 e à menor produção de ET-1. Intrigantemente, SIRT3 por sua vez promove a degradação de FUNDC1, criando um circuito de feedback que normalmente restringe a via, mas que fica desregulado durante a supernutrição crônica.
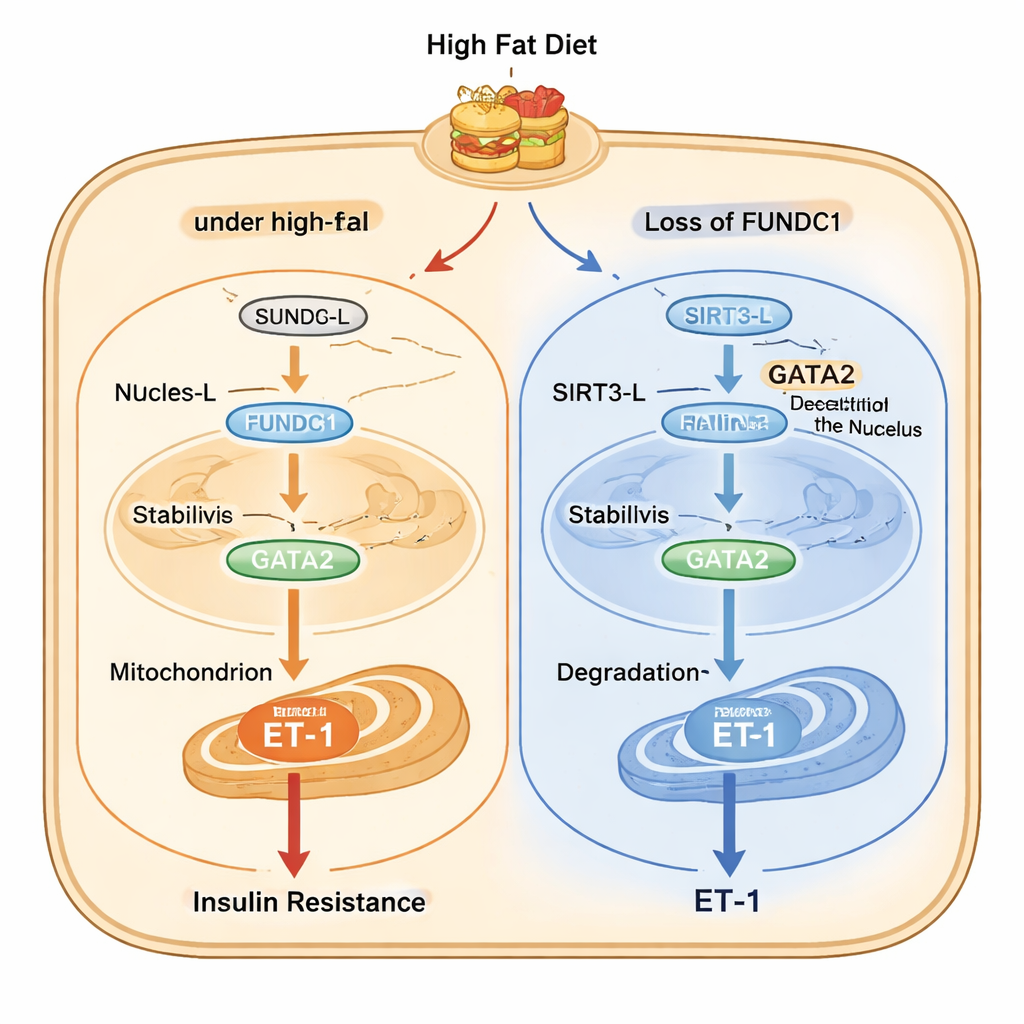
De modelos em camundongos à doença humana
Para testar se esse mecanismo importa em pessoas, os pesquisadores examinaram sangue e pequenas artérias de indivíduos com obesidade e diabetes tipo 2 e de voluntários saudáveis. Pacientes com ambas as condições apresentaram níveis sanguíneos mais altos de ET-1 e maior expressão de FUNDC1, GATA2 e do gene da ET-1 no endotélio vascular. A quantidade de ET-1 no sangue acompanhou de perto o índice de massa corporal e a glicemia de longo prazo (HbA1c), e os níveis do gene ET-1 nos vasos correlacionaram fortemente com FUNDC1 e GATA2. Esses padrões espelham as descobertas em camundongos e sustentam a ideia de que um eixo FUNDC1–SIRT3–GATA2–ET-1 hiperativo está em ação no tecido vascular humano sob estresse metabólico.
Um novo alvo na luta contra o diabetes
Para não especialistas, a mensagem central é que o dano por excesso de alimentação pode primeiro se manifestar nas células que revestem nossos vasos sanguíneos. Ali, uma proteína mitocondrial, FUNDC1, ajuda a redirecionar uma enzima reguladora, SIRT3, para fora do núcleo, permitindo que outro fator, GATA2, aumente a produção de ET-1, um sinal potente tipo hormônio que promove tanto enrijecimento vascular quanto resistência à insulina. Bloquear essa via — reduzindo a atividade de FUNDC1 endotelial ou diminuindo a ET-1 — pode ajudar a prevenir a transição da obesidade para o diabetes e proteger os vasos sanguíneos ao mesmo tempo.
Citação: Li, J., Li, D., Zhao, F. et al. Endothelial FUNDC1 regulates metabolic reprogramming and the obesity-diabetes transition through the SIRT3/GATA2/endothelin-1 axis. Nat Commun 17, 1836 (2026). https://doi.org/10.1038/s41467-026-68548-4
Palavras-chave: células endoteliais, mitocôndrias, endotelina-1, obesidade, diabetes tipo 2