Clear Sky Science · pt
Hidrogenação altamente seletiva e prática de (hetero)arenos funcionalizados
De Moléculas Planas a Blocos de Construção 3D
Medicamentos modernos, plásticos e muitos produtos químicos cotidianos são construídos a partir de pequenos “tijolos” moleculares. A maior parte desses blocos é plana, com estruturas anelares chamadas arenos, que os químicos apreciam por serem fáceis de sintetizar e modificar. Mas pesquisadores de fármacos e cientistas de materiais cada vez mais desejam formas mais tridimensionais, que frequentemente apresentam melhor comportamento no organismo e conferem propriedades superiores aos plásticos. Este artigo descreve uma maneira nova e prática de transformar anéis planos em estruturas 3D precisas usando um catalisador de platina robusto, abrindo um caminho mais simples para fármacos de próxima geração e aditivos plásticos mais seguros.
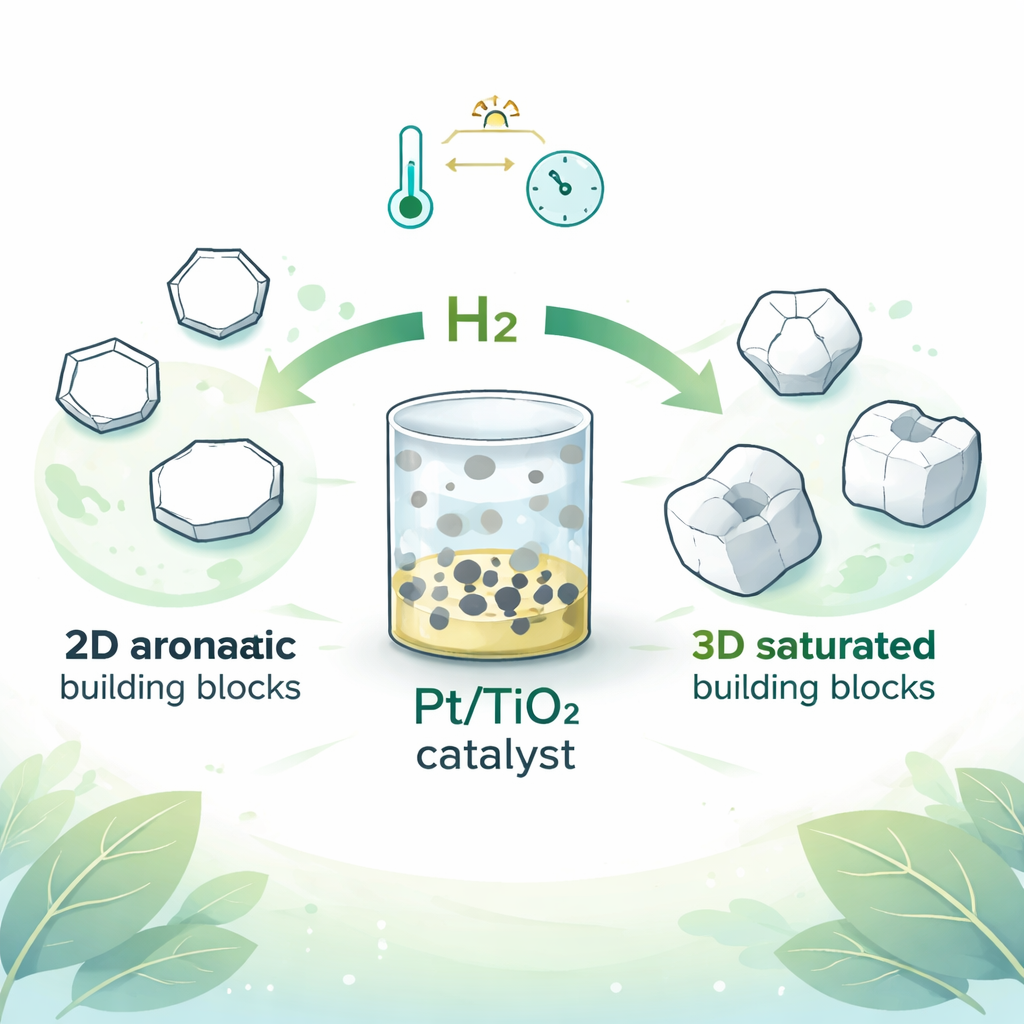
Por Que a Forma Importa nas Moléculas
Anéis aromáticos planos estão por toda parte: em produtos farmacêuticos, agroquímicos, vitaminas e polímeros. Sua popularidade significa que são baratos e amplamente disponíveis. Em contraste, seus equivalentes “saturados” — anéis cujas ligações duplas foram removidas — são muito menos comuns comercialmente, embora ofereçam vantagens importantes. Quando um anel se torna saturado e tridimensional, os químicos ganham controle muito mais fino sobre propriedades como o encaixe de um fármaco em um bolso proteico ou o comportamento de flexão e amolecimento de um plástico. Por exemplo, ao ajustar a proporção entre duas disposições 3D em espelho (chamadas formas cis e trans), os fabricantes de polímeros podem ajustar a temperatura de transição vítrea, que determina se um material é rígido ou flexível a uma determinada temperatura.
O Desafio de Curvar Anéis Planos
Converter um anel aromático plano em um anel saturado 3D soa simples — basta adicionar hidrogênio. Na prática, é muito difícil. Anéis aromáticos são extraordinariamente estáveis, de modo que romper sua “aromaticidade” exige muita energia. Ao mesmo tempo, moléculas do mundo real frequentemente carregam grupos químicos sensíveis, como ésteres ou amidas, que devem permanecer intactos durante o processo. Um catalisador precisa, portanto, cumprir três tarefas ao mesmo tempo: ativar anéis resistentes sob condições suaves, ignorar outras partes sensíveis da molécula e posicionar os novos átomos de hidrogênio de modo que uma forma 3D seja fortemente preferida em relação à outra. Catalisadores existentes que conseguem isso costumam ser complexos, sensíveis e difíceis de reciclar, o que os torna pouco atraentes para uso industrial em grande escala.
Um Catalisador de Platina Robusto sobre um Suporte Familiar
Os pesquisadores relatam um catalisador heterogêneo simples: pequenas partículas de platina depositadas em dióxido de titânio (Pt/TiO2). Com esse material, eles conseguem hidrogenar uma ampla variedade de arenos e heteroarenos multi-substituídos — anéis que também contêm átomos como nitrogênio ou oxigênio — sob condições relativamente brandas de temperatura e pressão de hidrogênio. Notavelmente, as reações favorecem fortemente uma disposição 3D, muitas vezes alcançando uma razão de diastereômeros de até 99 para 1 a favor da forma cis. Ao contrário de muitos sistemas anteriores, o catalisador é sólido, fácil de filtrar e reutilizável. Ele também preserva grupos delicados como ésteres, ésteres borônicos e amidas, o que é crucial quando o anel faz parte de um fármaco complexo ou de um material funcional.
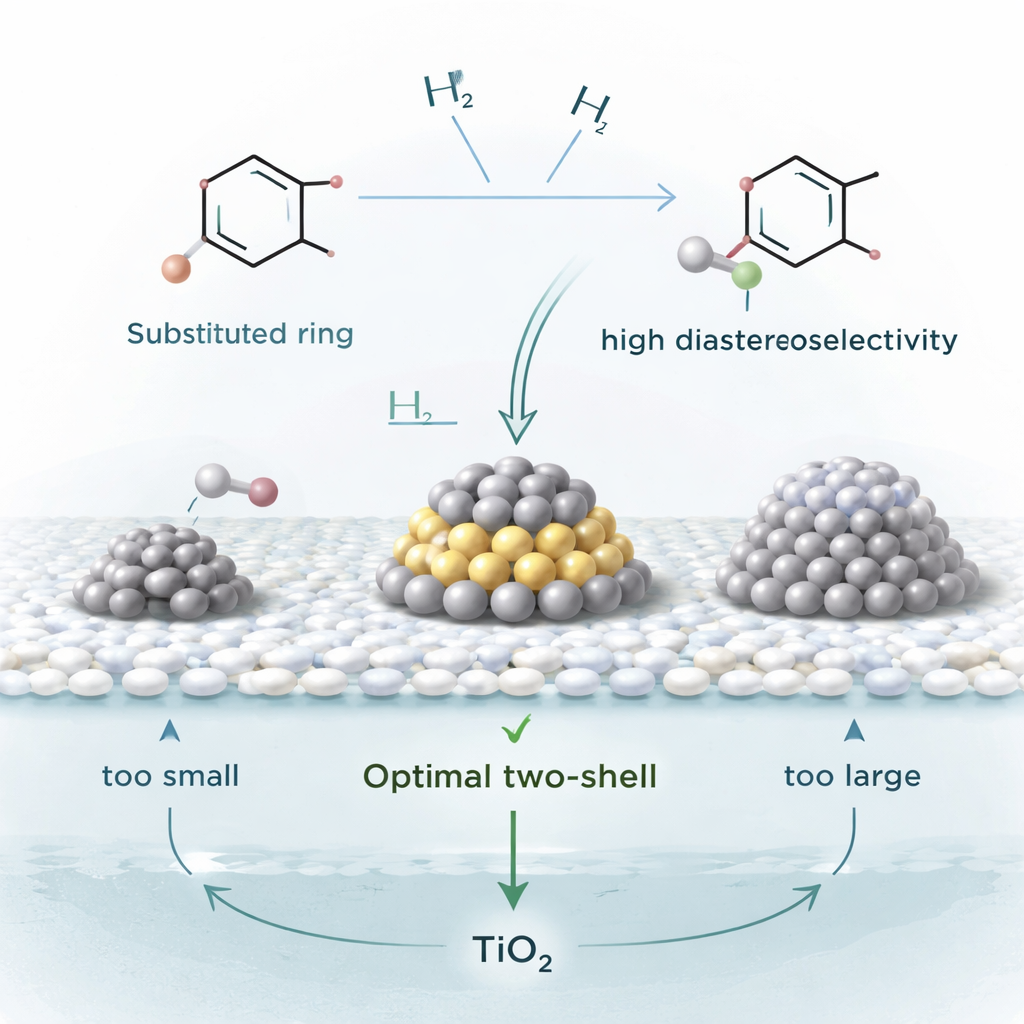
Aproximando-se do Ponto Ideal
Para entender por que esse catalisador funciona tão bem, a equipe estudou uma reação de referência: transformar ftalato de dimetila, um químico industrial comum, em seu correspondente saturado. Ao preparar Pt/TiO2 com diferentes carregamentos de platina e medir as taxas de reação, descobriram que a maior atividade ocorre quando as partículas de platina têm um tamanho intermediário muito específico. Imagens de microscopia eletrônica e simulações computacionais mostraram que partículas com uma chamada estrutura de duas camadas — grandes o suficiente para acomodar ao mesmo tempo o anel plano e o hidrogênio, mas não tão grandes a ponto de o anel se ligar de forma muito fraca — são o verdadeiro “ponto ideal”. Aglomerados menores ficam obstruídos pelo anel que adere fortemente, enquanto partículas muito maiores não prendem o anel com firmeza suficiente para reproduzir o comportamento observado.
De Reações Modelo a Produtos do Mundo Real
Munidos dessa visão, os cientistas exploraram a amplitude de aplicação do catalisador. Transformaram com sucesso muitos derivados do benzeno substituídos e sistemas de anéis fundidos ou tensionados, normalmente com altos rendimentos e forte preferência pelos produtos cis. Crucial para a química medicinal, eles também aplicaram o método a heteroarenos contendo nitrogênio que servem como blocos de construção para fármacos importantes, incluindo intermediários relacionados ao antibiótico moxifloxacino. Para demonstrar relevância industrial, realizaram uma reação em escala de quilograma que converte um plastificante ftalato comercial em uma alternativa sem ftalato sob condições sem solvente, obtendo quase exclusivamente a forma cis desejada e demonstrando que o catalisador pode ser reciclado várias vezes.
O Que Isso Significa para a Química do Dia a Dia
Em termos simples, este trabalho fornece aos químicos uma ferramenta robusta e reutilizável para remodelar anéis planos comuns em formas mais tridimensionais e bem definidas, sem longos desvios sintéticos. Ao identificar exatamente quais estruturas de platina realizam a transformação, o estudo abre a porta para projetar racionalmente catalisadores ainda melhores. O impacto imediato pode ser rotas mais rápidas para novos candidatos a medicamentos, plastificantes mais seguros e ajustáveis, e uso mais eficiente do hidrogênio na fabricação química — tudo alcançado com um catalisador sólido relativamente simples que se integra bem a processos industriais existentes.
Citação: Qu, R., Jena, S., Xiao, L. et al. Highly selective and practical hydrogenation of functionalized (hetero)arenes. Nat Commun 17, 2015 (2026). https://doi.org/10.1038/s41467-026-68537-7
Palavras-chave: hidrogenação de arenos, catalisador de platina, andaimes moleculares 3D, heteroarenos, síntese de plastificantes